Difenylkwik
| Difenylkwik | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||
| |||||
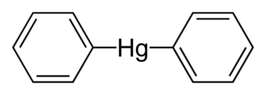
Structuurformule van difenylkwik
| |||||

| |||||
Molecuulmodel van difenylkwik
| |||||
| Algemeen | |||||
| Molecuulformule | C12H10Hg | ||||
| IUPAC-naam | difenylkwik | ||||
| Molmassa | 354,7978 g/mol | ||||
| SMILES | C1=CC=C(C=C1)[Hg]C2=CC=CC=C2
| ||||
| InChI | 1S/2C6H5.Hg/c2*1-2-4-6-5-3-1;/h2*1-5H;
| ||||
| CAS-nummer | 587-85-9 | ||||
| PubChem | 11488 | ||||
| Wikidata | Q2530372 | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H300 - H310 - H330 - H373 - H410 | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P260 - P264 - P273 - P280 - P284 - P301+P310 | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | vast | ||||
| Kleur | kleurloos | ||||
| Dichtheid | 2,318[1] g/cm³ | ||||
| Smeltpunt | 204[1] °C | ||||
| Goed oplosbaar in | benzeen, chloroform[1] | ||||
| Matig oplosbaar in | ethanol, di-ethylether[1] | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Difenylkwik is een kleurloze, kristallijne organokwikverbinding[2] met als brutoformule C12H10Hg. De notatie (C6H5)2Hg is meer in overeenstemming met de structuur van de stof. Afkortingen voor de notatie zijn afgeleid van de Engelse term voor fenyl (phenyl) of het gebruik van de Φ als symbool voor de fenylgroep: Ph2Hg, HgPh2, Φ2Hg of HgΦ2. Zoals in vrijwel alle organokwikverbindingen is de geometrie rond het kwikatoom lineair.[2]
Synthese[bewerken | brontekst bewerken]
De standaard, commerciële, bereiding van difenylkwik verloopt via de reactie van kwik(II)chloride met methyltrifenyltin in de molverhouding 2:1 in ethanol.[2] Daarnaast zijn er in het verleden diverse andere syntheseroutes naar deze stof beschreven.
In 1924 werd de synthese beschreven uitgaande van fenylkwikacetaat met benzeen in aanwezigheid van basisch natriumstanniet (Na2SnO2).[3]
In 1929 werd de synthese beschreven op basis van fenylmagnesiumbromide en kwik(II)halides.[4]
Difenylkwik kan ook bereid worden uit de reactie van broombenzeen met natriumamalgaam.[5]
Bronnen, noten en/of referenties
|



