Nitron

In de organische chemie is een nitron een functionele groep. Het kan beschouwd worden als een amineoxide van een imine en heeft als brutoformule R1R2C=NR3+O− (waarbij R3 geen waterstofatoom mag zijn).
Nitronen worden veel gebruikt bij organische syntheses en worden regelmatig vermeld in wetenschappelijke literatuur. Heel wat natuurlijk voorkomende stoffen zijn gerelateerd aan nitronen, waaronder alkaloïden, aza- en aminosuikers.
Reacties[bewerken | brontekst bewerken]
Nitronen vormen 1,3-dipolen in 1,3-dipolaire cycloaddities. Ze reageren met alkenen tot een isoxazolidine volgens onderstaand reactiemechanisme:

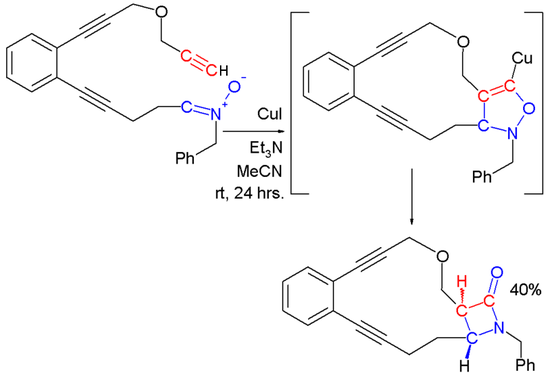
Nitronen reageren ook met terminale alkyngroepen en een koperzout tot een bètalactam. Dit wordt de Kinugasa-reactie genoemd, waarvan hieronder een voorbeeld staat. Het koperzout is hier koper(I)jodide. Het nitron reageert met het in situ gevormde koper(I)acetylide tot een vijfring, die in de tweede stap omgelegd wordt tot een vierring.