Molnupiravir
| Molnupiravir | ||||
|---|---|---|---|---|
| Chemische structuur | ||||
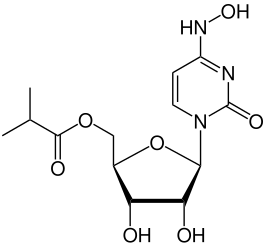
| ||||
| Databanken | ||||
| CAS-nummer | 2349386-89-4 | |||
| PubChem | 145996610 | |||
| Chemische gegevens | ||||
| Molecuulformule | ||||
| IUPAC-naam | ((2R,3S,4R,5R)-3,4-dihydroxy-5-(4-(hydroxyimino)-2-oxo-3,4-dihydropyrimidin-1(2H)-yl)tetrahydrofuran-2-yl)methyl isobutyrate | |||
| Molmassa | 329,31 g/mol | |||
| SMILES | CC(C)C(=O)OC[C@@H]1[C@H]([C@H]([C@@H](O1)N2C=CC(=NC2=O)NO)O)O | |||
| ||||
Molnupiravir is een experimenteel antiviraal geneesmiddel dat oraal ingenomen kan worden en werd ontwikkeld voor de behandeling van griep. Het is een prodrug van het synthetische nucleosidederivaat N4-hydroxycytidine en oefent zijn antivirale werking uit door de introductie van kopieerfouten tijdens virale RNA-replicatie.[1][2]
Het middel is ontwikkeld aan de Emory-universiteit door het innovatiebedrijf van de universiteit, Drug Innovation Ventures at Emory (DRIVE). Het werd vervolgens overgenomen door Ridgeback Biotherapeutics, dat later begon samen te werken met Merck & Co. (MSD) om het medicijn verder te ontwikkelen als virusremmer tegen COVID-19.[3]
De merknaam van hun medicijn is Lagevrio®.[4]
Gebruik[bewerken | brontekst bewerken]
De virusremmer in pilvorm is bedoeld voor volwassenen risicopatiënten met milde tot gemiddelde COVID-19-symptomen. Het middel is alleen werkzaam in een vroeg stadium van de infectie, maximaal vijf dagen na het begin van de symptomen.[5]
Controverse[bewerken | brontekst bewerken]
In april 2020 diende Rick Bright, die werd ontslagen als hoofd van de Biomedical Advanced Research and Development Authority (BARDA) vóór de goedkeuring van het medicijn, een klokkenluidersklacht in waarin hij beweerde dat Ridgeback BARDA onder druk had gezet om financiering te verstrekken voor de productie van EIDD-2801, ondanks de zorgen van Bright dat soortgelijke geneesmiddelen in zijn klasse mutagene eigenschappen hebben.[6] Een eerder bedrijf, Pharmasset, dat het actieve ingrediënt van het medicijn had onderzocht, was daarmee gestopt vanwege soortgelijke zorgen.[7] Deze beweringen werden ontkend door George Painter, CEO van DRIVE, die opmerkte dat er toxiciteitsonderzoeken naar molnupiravir waren uitgevoerd en gegevens waren verstrekt aan regelgevers in de VS en het VK, die toestemming gaven voor veiligheidsonderzoeken bij mensen in het voorjaar van 2020. Op dat moment verklaarden DRIVE en Ridgeback Biotherapeutics dat ze toekomstige veiligheidsstudies bij dieren gepland hadden.[8]
COVID-19[bewerken | brontekst bewerken]
Eind juli 2020 kondigde Merck, dat met Ridgeback Biotherapeutics samenwerkte aan de ontwikkeling van het medicijn, zijn voornemen aan om molnupiravir te onderwerpen aan vervolgstadiumproeven vanaf september 2020.[9] Op 19 oktober 2020 begon Merck met een eenjarige fase 2/3-studie die zich richtte op ziekenhuispatiënten. In juni 2021 heeft het Amerikaanse ministerie van Volksgezondheid (HHS) toegezegd om voor US$ 1,2 miljard aan molnupiravir (ongeveer 1,7 miljoen kuren) van Merck te kopen als het een autorisatie voor noodgebruik (EUA) of goedkeuring van de FDA zou krijgen.[10][11][12]
Op 1 oktober 2021 verklaarde Merck dat een onafhankelijke adviesraad die de klinische proef met COVID-19 had gemonitord, vroeg de studie vroegtijdig te stoppen omdat overtuigend bewijs geleverd was van de voordelen van het medicijn.[13] Het risico op ziekenhuisopname of overlijden werd verminderd met 48%. Merck kondigde plannen aan om een EUA aan te vragen bij de FDA en om marketingaanvragen in te dienen bij andere wereldwijde regelgevende instanties voor geneesmiddelen. Het bedrijf kondigde plannen aan om het medicijn in licentie te geven aan generieke fabrikanten, om de beschikbaarheid ervan te versnellen.[14][15][16]
Op 27 oktober 2021 werd bekend dat MSD het patent van molnupiravir gaat delen om het medicijn beschikbaar te maken voor 105 arme landen.[17]
De Britse MHRA, het agentschap dat beslist over toelating van geneesmiddelen, bepaalde begin november 2021 dat het medicijn mag worden verkocht in Groot-Brittannië voor thuisgebruik[5], hoewel er nog geen wetenschappelijk publicatie van het onderzoek heeft plaatsgevonden en zodoende geen informatie bekend is over bijwerkingen.[18]
OP 20 november gaf het EMA zijn goedkeuring. Het geneesmiddelenbureau adviseert na voorlopig onderzoek positief over het gebruik door volwassenen die geen zuurstoftoediening nodig hebben en die een verhoogd risico hebben om ernstige covid te krijgen.[19]
Op 30 november 2021 werd bekendgemaakt dat molnupiravir hoogstwaarschijnlijk zal worden goedgekeurd voor gebruik in de VS. Een commissie van de Amerikaanse voedsel- en medicijnautoriteit FDA verstrekte een positief advies over het middel. Doorgaans neemt de FDA adviezen van de commissie over. Eerder werd in Groot-Brittannië het medicijn al goedgekeurd.[20]
Uit het fase 3 onderzoek bleek dat het effect van het middel kleiner was dan aanvankelijk aangekondigd. De absolute kans op ziekenhuisopname in de steekproef daalde met krap zeven procent, de kans op overlijden met circa drie procent. Het dubbelblinde onderzoek werd uitgevoerd met meer dan 1400 patienten die bij het begin van de test nog niet zo ziek waren dat ze al in het ziekenhuis opgenomen moesten worden.[21]

