Gebruiker:CFCF/Kladblok/Hepatitis C
{{samenvoegennaar|Hepatitis C}} Hepatitis C is een infectieziekte die voornamelijk de lever aantast. De ziekte wordt veroorzaakt door het hepatitis-C-virus (HCV). [1] Mensen met hepatitis C vertonen in veel gevallen geen symptomen, maar chronische infectie kan leiden tot beschadiging van de lever en, na vele jaren, tot levercirrose. In sommige gevallen, hebben mensen met cirrose tevens leverfalen, leverkanker, of ernstig gezwollen aderen op de maag en slokdarm, hetgeen kan leiden tot bloedingen waaraan men overlijdt.[1]
De voornaamste oorzaken van hepatitis C zijn: direct bloedcontact bij intraveneus drugsgebruik, het gebruik van niet-steriel medisch materiaal en bloedtransfusies. Naar schatting lijden wereldwijd 130–170 miljoen mensen aan hepatitis C. Onderzoek naar HCV begon in de jaren 70 van de vorige eeuw en in 1989 werd het bestaan van de ziekte aangetoond.[2] Voor zover bekend, veroorzaakt het virus geen ziekte bij dieren.
De standaardmedicatie bij de behandeling van HCV bestaat uit peginterferon en ribavirine. 50 à 80% van de behandelde mensen wordt genezen. Mensen die cirrose of leverkanker krijgen, hebben mogelijk een levertransplantatie nodig, maar na een transplantatie komt het virus in de meeste gevallen weer terug.[3] Er bestaat geen vaccin tegen hepatitis C. { {TOC limit|3}}
Klachten en symptomen[bewerken | brontekst bewerken]
Slechts in 15% van de gevallen veroorzaakt hepatitis C acute symptomen.[4] Meestal echter zijn de symptomen licht en vaag, zoals een afname van de eetlust, vermoeidheid, misselijkheid, spier- of gewrichtspijn en gewichtsverlies.[5] Slechts in enkele gevallen gaat de acute infectie gepaard met geelzucht.[6] Bij 10 tot 50% van de patiënten verdwijnt de infectie zonder behandeling, met name bij jonge vrouwen.[6]
Chronische infectie[bewerken | brontekst bewerken]
Bij 80% van de mensen die met het virus in aanraking komen, ontstaat een chronische infectie.[7] Tijdens de eerste decennia van de infectie vertonen de meeste mensen geen of zeer lichte symptomen, [8] al kan chronische hepatitis C gepaard kan gaan met vermoeidheid.[9] Hepatitis C is de belangrijkste oorzaak van cirrose en leverkanker onder mensen die vele jaren met het virus zijn besmet.[3] 10 tot 30% van de mensen die minstens dertig jaar met het virus zijn besmet krijgt levercirrose.[3][5] Cirrose komt vaker voor bij mensen die tevens zijn besmet met hepatitis B of HIV, alcoholisten en mannen.[5] Mensen met cirrose hebben een twintig keer verhoogd risico om leverkanker te krijgen: een incidentie van 1 à 3% per jaar.[3][5] Voor alcoholisten is dit risico honderd keer verhoogd.[10] Hepatitis C is de oorzaak van 27% van de cirrosegevallen en 25% van de gevallen van leverkanker.[11]
Levercirrose kan leiden tot hoge bloeddruk in de aderen die zijn verbonden met de lever, vochtophoping in de buik, het gemakkelijk krijgen van blauwe plekken of bloedingen, vergrote aderen, met name in de maag en de slokdarm, geelzucht (een gele verkleuring van de huid) en hersenschade.[12]
Effecten buiten de lever[bewerken | brontekst bewerken]
Hepatitis C wordt in zeldzame gevallen ook in verband gebracht met het Sjögren-syndroom (een auto-immuunziekte), een verlaagd aantal bloedplaatjes, chronische huidziekten, diabetes en non-Hodgkin lymfklierkanker.[13][14]
Oorzaak[bewerken | brontekst bewerken]
Het hepatitis-C-virus is een klein, omhuld, 'positive sense' enkelstrengs-RNA-virus.[3] Het is een lid van de virussoort hepacivirus behorend tot de familie van Flaviviridae.[9] Er bestaan zeven belangrijke genotypen van het HCV.[15] In de Verenigde Staten wordt 70% van de gevallen veroorzaakt door genotype 1 en 20% door genotype 2; elk van de andere genotypen veroorzaakt 1% van de gevallen. [5] Genotype 1 is ook in Zuid-Amerika en Europa het meest voorkomende genotype.[3]
Overdracht[bewerken | brontekst bewerken]
De voornaamste wijze van overdracht in ontwikkelde landen is via intraveneus drugsgebruik (IVD) (injecteren van drugs in een ader). In ontwikkelingslanden zijn bloedtransfusies en onveilige medische ingrepen de belangrijkste wijzen van overdracht.[16] In 20% van de gevallen blijft de oorzaak onbekend,[17] maar veel van deze gevallen zijn waarschijnlijk het gevolg van IVD.[6]
Intraveneus drugsgebruik[bewerken | brontekst bewerken]
IVD is in grote delen van de wereld een belangrijke risicofactor voor hepatitis C.[18] Uit een onderzoek in 77 landen blijkt dat in 25 daarvan, waaronder de Verenigde Staten en China[18], 60 tot 80% van de gebruikers van intraveneuze drugs hepatitis C heeft. [7] In twaalf landen is dit meer dan 80%.[7] Maar liefst tien miljoen gebruikers van intraveneuze drugs zijn besmet met hepatitis C; China (1,6 miljoen), de Verenigde Staten (1,5 miljoen) en Rusland (1,3 miljoen) hebben de hoogste aantallen besmette drugsgebruikers.[7] Het percentage hepatitis C onder gedetineerden in de Verenigde Staten is tien tot twintig keer zo hoog als onder de algehele bevolking, hetgeen in deze onderzoeken wordt geweten aan risicovol gedrag als IVD en tatoeëren met niet-steriel materiaal.[19][20]
Risico's gerelateerd aan de gezondheidszorg[bewerken | brontekst bewerken]
Bloedtransfusies, bloedproducten, en orgaantransplantaties zonder HCV-screening brengen een aanzienlijk risico op infectie met zich mee.[5] De Verenigde Staten hebben in 1992 een algemene screening ingevoerd. Sindsdien is het aantal besmettingen gedaald van een op tweehonderd per bloedeenheid[21] tot een op tienduizend à tien miljoen per bloedeenheid.[6][17] Dit lage risico blijft bestaan omdat het ongeveer elf tot zeventig dagen duurt voordat hepatitis C in het bloed van een potentiële bloeddonor kan worden aangetoond als hij of zij besmet is geraakt.[17] In sommige landen wordt vanwege de kosten nog steeds niet op hepatitis C gescreend.[11]
Iemand die een prikletsel oploopt van een naald gebruikt door iemand met HCV, heeft ongeveer een kans van 1,8% om de ziekte te krijgen.[5] Het risico is groter wanneer de gebruikte naald hol is en de prik diep.[11] Er bestaat risico wanneer bloed met slijmvlies in aanraking komt, maar dit risico is klein en er is geen risico wanneer bloed in aanraking komt met een intacte huid.[11]
Hepatitis C kan ook overgedragen worden via de uitrusting van ziekenhuizen, zoals: hergebruikte naalden en spuiten, medicatieflacons voor meervoudig gebruik, infuuszakken en niet-steriel chirurgisch materiaal.[11] Slechte hygiënische omstandigheden in medische en tandheelkundige klinieken zijn de voornaamste oorzaak van de verspreiding van HCV in Egypte, het land met de hoogste besmettingsgraad ter wereld.[22]
Geslachtsgemeenschap[bewerken | brontekst bewerken]
Het is niet bekend of hepatitis C overgedragen kan worden via seks.[23] Er is verband tussen riskant seksueel gedrag en hepatitis C, maar het is niet duidelijk of de overdracht van de ziekte het gevolg is van onvermeld drugsgebruik of van de seks op zich.[5] Er zijn aanwijzingen die erop duiden dat er geen risico is voor heteroseksuele paren die geen seks met anderen hebben.[23] Seksuele activiteiten die gepaard gaan met aanzienlijk letsel van de binnenwand van de anus, zoals anale penetratie, of die plaatsvinden wanneer er tevens sprake is van een seksueel overdraagbare infectie, inclusief HIV of genitale zweren, brengen wel een risico met zich mee.[23] De Amerikaanse overheid adviseert mensen met meerdere partners alleen condooms te gebruiken om besmetting met hepatitis C te voorkomen.[24]
Piercings[bewerken | brontekst bewerken]
Tatoeëring hangt samen met een twee tot drie keer verhoogd risico op hepatitis C.[25] Dit kan het gevolg zijn van het gebruik van niet-steriel materiaal of door besmetting van de gebruikte inkt.[25] Het gaat hierbij met name om tatoeages of piercings die vóór het midden van de jaren tachtig zijn gezet of die niet-professioneel zijn aangebracht, omdat de steriele technieken in dergelijke omstandigheden slecht geweest kunnen zijn. De risico's lijken ook groter te zijn naarmate de tatoeages groter zijn.[25] Bijna de helft van de gedetineerden deelt ongesteriliseerde tatoeage-apparatuur met anderen.[25] Tatoeages die zijn aangebracht in gecertificeerde instellingen worden slechts in zeldzame gevallen direct in verband gebracht met een HCV-besmetting.[26]
Contact met bloed[bewerken | brontekst bewerken]
Lichaamsverzorgingsartikelen zoals scheermesjes, tandenborstels en een manicure- of pedicure-uitrusting, kunnen in contact komen met bloed. Het delen van deze artikelen met anderen, brengt een risico op HCV-besmetting met zich mee.[27][28] Men moet voorzichtig zijn met snijwonden, zweren of andere vormen van bloedingen.[28] HCV wordt niet verspreid door vluchtig contact zoals knuffelen, kussen of het delen van bestek of kookgerei.[28]
Overdracht van moeder op kind[bewerken | brontekst bewerken]
Overdracht van een met hepatitis C besmette moeder op haar kind komt voor bij minder dan 10% van de zwangerschappen.[29] Er bestaan geen maatregelen die iets aan dit risico kunnen veranderen.[29] Besmetting kan plaatsvinden tijdens de zwangerschap en tijdens de bevalling.[17] Een langdurige bevalling hangt samen met een groter risico op besmetting.[11] Er zijn geen aanwijzingen dat HCV verspreid wordt via borstvoeding; een besmette moeder moet het geven van borstvoeding echter vermijden wanneer haar tepels gebarsten zijn en bloeden,[30] of wanneer haar virale waarden hoog zijn.[17]
Diagnose[bewerken | brontekst bewerken]
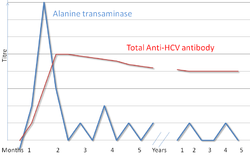
Hepatitis C kan met verschillende onderzoeksmethoden worden opgespoord, zoals het testen op antistoffen tegen HCV, de ELISA-test, de Western blot-test en het testen op de hoeveelheid HCV-RNA.[5] Met behulp van de PCR-test (polymerasekettingreactie) kan men binnen een à twee weken na besmetting al HCV-RNA aantonen, terwijl het aanzienlijk langer kan duren voordat antilichamen gevormd worden en aantoonbaar zijn.[12]
Chronische hepatitis C is een besmetting met het hepatitis-C-virus die langer dan zes maanden aanhoudt en waarbij de aanwezigheid van HCV-RNA aangetoond is.[8] Omdat chronische infecties normaal gesproken decennia lang geen symptomen veroorzaken,[8] ontdekken medici de infectie meestal bij het afnemen van leverfunctietests of tijdens een routine-onderzoek van mensen die tot de risicogroep behoren. Op basis van tests is niet te zien of het een acute of een chronische infectie betreft.[11]
Bloedonderzoek[bewerken | brontekst bewerken]
Medisch onderzoek naar hepatitis C begint gewoonlijk met bloedonderzoek om antilichamen tegen HCV op te sporen met behulp van een zogeheten enzym-immuno-assay.[5] Als deze test positief is, wordt een tweede test uitgevoerd om de immuno-assay te controleren en de ernst vast te stellen.[5] De immuno-assay wordt gecontroleerd met behulp van een 'recombinant immunoblot assay', de ernst wordt bepaald met behulp van een 'HCV-RNA-polymerasekettingreactietest'.[5] Indien er geen RNA aanwezig is en de immunoblot is positief, dan had de patiënt een eerdere infectie, maar is spontaan of d.m.v. een behandeling genezen; indien de immunoblot negatief is, was de immuno-assay verkeerd.[5] Pas zes tot acht weken na de infectie is de immuno-assay positief.[9]
In de eerste fase van de infectie zijn de hoeveelheden leverenzymen in het bloed wisselend;[8] gemiddeld zeven weken na de infectie beginnen die hoeveelheden te stijgen.[9] Er is weinig verband tussen de hoeveelheid leverenzymen en de ernst van de ziekte.[9]
Biopsie[bewerken | brontekst bewerken]
Met een leverbiopsie (het afnemen van een stukje weefsel uit de lever) kan de mate van leverschade worden vastgesteld, maar aan deze procedure zijn risico's verbonden.[3] De typische veranderingen die met een biopsie gevonden worden zijn lymfocyten in het leverweefsel, lymfoïde follikels (blaasjes) in de driehoekjes van Kiernan (bepaalde driehoekige veldjes in de lever) en veranderingen in de galwegen.[3] Er bestaan een aantal bloedonderzoeken waarmee men kan proberen om de omvang van de leverschade zodat een biopsie hopelijk kan worden voorkomen.[3]
Screening[bewerken | brontekst bewerken]
Slechts 5 tot 50% van de geïnfecteerde mensen in de Verenigde Staten en Canada zijn zich van hun toestand bewust.[25] Een onderzoek wordt aanbevolen voor mensen met een hoog risico, waaronder mensen met tatoeages.[25] Screening wordt ook aanbevolen bij mensen met verhoogde leverenzymwaarden, omdat dit vaak het enige teken is van chronische hepatitis.[31] Routinematige screening wordt in de Verenigde Staten niet aanbevolen.[5]
Preventie[bewerken | brontekst bewerken]
In 2011 bestonden er nog geen vaccins tegen hepatitis C. Er zijn wel vaccins in ontwikkeling en met sommige daarvan zijn bemoedigende resultaten bereikt.[32] Een combinatie van preventieve maatregelen, zoals het verschaffen van nieuwe naalden en spuiten en de behandeling van drugsmisbruik, verminderen het risico op hepatitis C bij gebruikers van intraveneuze drugs met ongeveer 75%.[33] Landelijk gezien is het screenen van bloeddonoren belangrijk, alsook het naleven van universele voorzorgsmaatregelen binnen instellingen voor gezondheidszorg.[9] In landen waar onvoldoende steriele injectiespuiten beschikbaar zijn, dienen zorgverleners medicatie zoveel mogelijk via de mond toe te dienen in plaats van via een injectie.[11]
Behandeling[bewerken | brontekst bewerken]
HCV leidt bij 50–80% van de geïnfecteerde mensen tot chronische infectie. Ongeveer 40-80% van deze mensen geneest na behandeling.[34][35] In zeldzame gevallen geneest de infectie zonder behandeling.[6] Mensen met chronische hepatitis C moeten alcohol en geneesmiddelen die giftig voor de lever zijn vermijden,[5] en gevaccineerd worden tegen hepatitis A en hepatitis B.[5] Mensen met levercirrose dienen met behulp van echografie te worden gecontroleerd op leverkanker.[5]
Geneesmiddelen[bewerken | brontekst bewerken]
Mensen met leverafwijkingen door HCV-infectie moeten worden behandeld. [5] De huidige behandeling is een combinatie van gepegyleerd interferon en het antivirale middel ribavirine gedurende 24 of 48 weken, afhankelijk van het type HCV.[5] Bij 50 tot 60% van de behandelde patiënten worden goede resultaten geboekt.[5] Het combineren van ofwel boceprevir of telaprevir met ribavirine en peginterferon alfa verbetert de antivirale werking tegen hepatitis C genotype 1.[36][37][38] Bijwerkingen van de behandeling komen vaak voor; de helft van de behandelde patiënten krijgt griepachtige symptomen, en een derde ervaart emotionele problemen.[5] Een behandeling tijdens de eerste zes maanden heeft meer effect dan wanneer hepatitis C chronisch is geworden.[12] Wanneer iemand een nieuwe infectie oploopt en deze niet binnen acht tot twaalf weken geneest, dan wordt een 24 weken durende behandeling met gepegyleerd interferon aanbevolen.[12] Bij mensen met thalassemie (een bloedziekte) blijkt ribavirine nuttig te zijn, maar neemt de behoefte aan bloedtransfusies wel toe.[39]
Voorstanders beweren dat verschillende alternatieve therapieën werkzaam zijn tegen hepatitis C, waaronder maria- (melk-)distel, ginseng, en colloïdaal zilver.[40] Van geen enkele alternatieve therapie is echter aangetoond dat de resultaten bij hepatitis C erdoor verbeteren, en er bestaat geen enkel bewijs dat alternatieve therapieën überhaupt enig effect op het virus hebben.[40][41][42]
Prognose[bewerken | brontekst bewerken]
De reactie op de behandeling wisselt naargelang het genotype. Bij ongeveer 40 tot 50% van de patiënten met HCV genotype 1 houdt het effect na een behandeling van 48 weken langere tijd aan.[3] Bij 70 tot 80% van de patiënten met de HCV genotypen 2 en 3 houdt het effect na een behandeling van 24 weken langere tijd aan.[3] Bij ongeveer 65% van de patiënten met HCV genotype 4 houdt het effect na een behandeling van 48 weken langere tijd aan. Momenteel zijn er nog zeer weinig gegevens over de behandeling van HCV genotype 6, en de gegevens die er zijn betreffen een behandeling van 48 weken met dezelfde dosering als bij genotype 1.[43]
Epidemiologie[bewerken | brontekst bewerken]
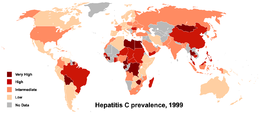

130 tot 170 miljoen mensen, of ~3% van de wereldbevolking leeft met chronische hepatitis C.[44] Elk jaar worden 3 tot 4 miljoen personen geïnfecteerd en meer dan 350.000 mensen sterven jaarlijks aan ziekten die verband houden met hepatitis C.[44] In de 20e eeuw zijn deze cijfers aanzienlijk gestegen door een combinatie van injecterende drugsgebruikers en intraveneuze medicatie of niet-gesteriliseerde medische apparatuur.[11]
In de Verenigde Staten heeft ongeveer 2% van de inwoners hepatitis C,[5] met jaarlijks 35.000 tot 185.000 nieuwe gevallen. Sedert de jaren '90 zijn deze cijfers in het Westen gedaald dankzij de verbeterde bloedscreening vóór bloedtransfusies.[12] In de Verenigde Staten sterven jaarlijks 8000 tot 10.000 mensen aan HCV. Naar verwachting zal dit sterftecijfer gaat stijgen doordat de mensen die door transfusie besmet raakten voordat het testen op HCV werd ingevoerd, ziek worden en overlijden.[45]
In sommige Afrikaanse en Aziatische landen liggen de infectiepercentages hoger.[46] Landen met een zeer hoog besmettingspercentage zijn Egypte (22%), Pakistan (4,8%) en China (3,2%).[44] Het hoge percentage in Egypte houdt verband met een inmiddels beëindigde grootschalige campagne voor de behandeling van Schistosomiasis, waarvoor slecht gesteriliseerde, glazen injectiespuiten werden gebruikt.[11]
Geschiedenis[bewerken | brontekst bewerken]
In het midden van de jaren '70 van de vorige eeuw toonden Harvey J. Alter, hoofd van de Dienst Infectieziekten van de afdeling Transfusiegeneeskunde van de National Institutes of Health, en zijn onderzoeksteam aan dat de meeste gevallen van hepatitis na een bloedtransfusie niet te wijten waren aan hepatitis-A- of hepatitis-B-virussen. Ondanks deze ontdekking duurde het nog een jaar of tien voordat internationale onderzoeken resultaat hadden en het virus werd geïdentificeerd dat wel verantwoordelijk was: in 1987 werd met een nieuwe techniek, moleculaire klonering, vastgesteld welk organisme de boosdoener was en werd er een diagnostische test ontwikkeld. De eer hiervoor komt toe aan Michael Houghton, Qui-Lim Choo en George Kuo van de Chiron Corporation, in samenwerking met Dr. D.W. Bradley van de Centers for Disease Control and Prevention.[47] In 1988 bevestigde Alter het bestaan van het virus door de aanwezigheid ervan vast te stellen in een groep monsters waarin hepatitis A en hepatitis B niet voorkwamen. In april 1989 werd de ontdekking van HCV gepubliceerd in twee artikelen in het tijdschrift Science.[48][49] De ontdekking leidde tot aanzienlijke verbeteringen in de diagnostiek en een betere antivirale behandeling.[47] In 2000 werden Dr. Alter en Dr. Houghton beloond met de Laskerprijs voor "pionierswerk dat leidde tot de ontdekking van het virus dat hepatitis C veroorzaakt en de ontwikkeling van screeningmethoden die het risico van bloedtransfusie-gerelateerde hepatitis in de VS verlaagde van 30% in 1970 tot vrijwel nul in 2000."[50]
Chiron legde een aantal octrooien op het virus en de diagnostiek van het virus vast.[51] Een concurrerende octrooiaanvraag van het CDC werd in 1990 ingetrokken nadat Chiron 1,9 miljoen dollar aan het CDC en 337.500 dollar aan Bradley had betaald. In 1994 klaagde Bradley Chiron aan met als doel het octrooi ongeldig te verklaren, zichzelf als mede-uitvinder te laten opnemen en schadevergoeding en royalty's te verkrijgen. Hij gaf het in 1998 op toen hij de zaak verloor voor het Hof van Beroep.[52]
Samenleving en cultuur[bewerken | brontekst bewerken]
De World Hepatitis Alliance coördineert de Wereld hepatitisdag die elk jaar op 28 juli wordt gehouden.[53] De economische kosten van hepatitis C zijn aanzienlijk, zowel voor het individu als voor de maatschappij. In 2003 werden de gemiddelde kosten van de ziekte per mensenleven in de Verenigde Staten op 33.407 dollar,[54] in 2011 bedroegen de kosten van een levertransplantatie ongeveer 200.000 dollar.[55] In 2003 kostte een kuur met antivirale middelen in Canada 30.000 dollar,[56] terwijl de kosten in de Verenigde Staten in 1998 tussen 9200 en 17.600 dollar bedroegen.[54] In veel gebieden van de wereld kunnen patiënten zich geen behandeling met antivirale middelen veroorloven omdat ze ofwel niet verzekerd zijn of omdat hun verzekering geen antivirale middelen vergoedt.[57]
Wetenschappelijk onderzoek[bewerken | brontekst bewerken]
Sinds 2011 wordt er gewerkt aan ongeveer honderd geneesmiddelen voor hepatitis C.[55] Deze geneesmiddelen zijn onder meer vaccins voor het behandelen van hepatitis, immunomodulatoren en cyclofilineremmers.[58] Deze mogelijke nieuwe behandelingen zijn het gevolg van een beter begrip van het hepatitis-C-virus.[59]
Referenties[bewerken | brontekst bewerken]
{ {Reflist|colwidth=30em}}
- ↑ a b Sherris Medical Microbiology, 4th. McGraw Hill (2004), 551–2. ISBN 0838585299.
- ↑ Houghton M (November 2009). The long and winding road leading to the identification of the hepatitis C virus. Journal of Hepatology 51 (5): 939–48. PMID 19781804. DOI: 10.1016/j.jhep.2009.08.004.
- ↑ a b c d e f g h i j k Rosen, HR (23 juni 2011). Clinical practice. Chronic hepatitis C infection.. The New England journal of medicine 364 (25): 2429–38. PMID 21696309.
- ↑ Maheshwari, A, Ray, S, Thuluvath, PJ (26 juli 2008). Acute hepatitis C.. Lancet 372 (9635): 321–32. PMID 18657711. DOI: 10.1016/S0140-6736(08)61116-2.
- ↑ a b c d e f g h i j k l m n o p q r s t u v Wilkins, T, Malcolm, JK, Raina, D, Schade, RR (1 juni 2010). Hepatitis C: diagnosis and treatment.. American family physician 81 (11): 1351–7. PMID 20521755.
- ↑ a b c d e Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future.. Springer Verlag (2011), p. 4. ISBN 9781461411918.
- ↑ a b c d Nelson, PK, Mathers, BM, Cowie, B, Hagan, H, Des Jarlais, D, Horyniak, D, Degenhardt, L (13 augustus 2011). Global epidemiology of hepatitis B and hepatitis C in people who inject drugs: results of systematic reviews.. Lancet 378 (9791): 571–83. PMID 21802134. DOI: 10.1016/S0140-6736(11)61097-0.
- ↑ a b c d Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future.. Springer Verlag (2011), 103–104. ISBN 9781461411918.
- ↑ a b c d e f Dolin, [edited by] Gerald L. Mandell, John E. Bennett, Raphael (2010), Mandell, Douglas, and Bennett's principles and practice of infectious diseases, 7th ed.. Churchill Livingstone/Elsevier, Philadelphia, PA, Chapter 154. ISBN 978-0443068393.
- ↑ Mueller, S, Millonig, G, Seitz, HK (28 juli 2009). Alcoholic liver disease and hepatitis C: a frequently underestimated combination.. World journal of gastroenterology : WJG 15 (28): 3462–71. PMID 19630099.
- ↑ a b c d e f g h i j Alter, MJ (7 mei 2007). Epidemiology of hepatitis C virus infection.. World journal of gastroenterology : WJG 13 (17): 2436–41. PMID 17552026.
- ↑ a b c d e Ozaras, R, Tahan, V (2009 Apr). Acute hepatitis C: prevention and treatment.. Expert review of anti-infective therapy 7 (3): 351–61. PMID 19344247.
- ↑ Zignego AL, Ferri C, Pileri SA, Caini P, Bianchi FB (January 2007). Extrahepatic manifestations of Hepatitis C Virus infection: a general overview and guidelines for a clinical approach. Digestive and Liver Disease 39 (1): 2–17. PMID 16884964. DOI: 10.1016/j.dld.2006.06.008.
- ↑ Louie, KS, Micallef, JM, Pimenta, JM, Forssen, UM (2011 Jan). Prevalence of thrombocytopenia among patients with chronic hepatitis C: a systematic review.. Journal of viral hepatitis 18 (1): 1–7. PMID 20796208.
- ↑ Nakano T, Lau GM, Lau GM, Sugiyama M, Mizokami M (December 2011). An updated analysis of hepatitis C virus genotypes and subtypes based on the complete coding region. Liver Int.. PMID 22142261. DOI: 10.1111/j.1478-3231.2011.02684.x.
- ↑ Maheshwari, A, Thuluvath, PJ (2010 Feb). Management of acute hepatitis C.. Clinics in liver disease 14 (1): 169–76; x. PMID 20123448.
- ↑ a b c d e Pondé, RA, Mikhaĭlova, A (2011 Feb). Hidden hazards of HCV transmission.. Medical microbiology and immunology 200 (1): 7–11. PMID 20461405.
- ↑ a b Xia, X, Luo, J, Bai, J, Yu, R (2008 Oct). Epidemiology of HCV infection among injection drug users in China: systematic review and meta-analysis.. Public health 122 (10): 990–1003. PMID 18486955. DOI: 10.1016/j.puhe.2008.01.014.
- ↑ Imperial, JC (2010 Jun). Chronic hepatitis C in the state prison system: insights into the problems and possible solutions.. Expert review of gastroenterology & hepatology 4 (3): 355–64. PMID 20528122.
- ↑ Vescio, MF, Longo, B, Babudieri, S, Starnini, G, Carbonara, S, Rezza, G, Monarca, R (2008 Apr). Correlates of hepatitis C virus seropositivity in prison inmates: a meta-analysis.. Journal of epidemiology and community health 62 (4): 305–13. PMID 18339822.
- ↑ Marx, John (2010), Rosen's emergency medicine: concepts and clinical practice 7th edition. Mosby/Elsevier, Philadelphia, PA, p. 1154. ISBN 9780323054720.
- ↑ Highest Rates of Hepatitis C Virus Transmission Found in Egypt. Al Bawaba (9 augustus 2010). Geraadpleegd op 27 augustus 2010.
- ↑ a b c Tohme RA, Holmberg SD (June 2010). Is sexual contact a major mode of hepatitis C virus transmission?. Hepatology 52 (4): 1497–505. PMID 20635398. DOI: 10.1002/hep.23808.
- ↑ Hepatitis C Group Education Class. United States Department of Veteran Affairs.
- ↑ a b c d e f Jafari, S, Copes, R, Baharlou, S, Etminan, M, Buxton, J (2010 Nov). Tattooing and the risk of transmission of hepatitis C: a systematic review and meta-analysis.. International journal of infectious diseases : IJID : official publication of the International Society for Infectious Diseases 14 (11): e928-40. PMID 20678951.
- ↑ Hepatitis C. Center for Disease Control and Prevention. Geraadpleegd op 2 January 2012.
- ↑ Lock G, Dirscherl M, Obermeier F, et al. (September 2006). Hepatitis C —contamination of toothbrushes: myth or reality?. J. Viral Hepat. 13 (9): 571–3. PMID 16907842. DOI: 10.1111/j.1365-2893.2006.00735.x.
- ↑ a b c Hepatitis C. FAQ – CDC Viral Hepatitis. Geraadpleegd op 2 januari 2012.
- ↑ a b Lam, NC, Gotsch, PB, Langan, RC (15 november 2010). Caring for pregnant women and newborns with hepatitis B or C.. American family physician 82 (10): 1225–9. PMID 21121533.
- ↑ Mast EE (2004). Mother-to-infant hepatitis C virus transmission and breastfeeding. Advances in Experimental Medicine and Biology 554: 211–6. PMID 15384578.
- ↑ Senadhi, V (2011 Jul). A paradigm shift in the outpatient approach to liver function tests.. Southern medical journal 104 (7): 521–5. PMID 21886053.
- ↑ Halliday, J, Klenerman, P, Barnes, E (2011 May). Vaccination for hepatitis C virus: closing in on an evasive target.. Expert review of vaccines 10 (5): 659–72. PMID 21604986. DOI: 10.1586/erv.11.55.
- ↑ Hagan, H, Pouget, ER, Des Jarlais, DC (1 juli 2011). A systematic review and meta-analysis of interventions to prevent hepatitis C virus infection in people who inject drugs.. The Journal of infectious diseases 204 (1): 74–83. PMID 21628661.
- ↑ Torresi, J, Johnson, D, Wedemeyer, H (2011 Jun). Progress in the development of preventive and therapeutic vaccines for hepatitis C virus.. Journal of hepatology 54 (6): 1273–85. PMID 21236312. DOI: 10.1016/j.jhep.2010.09.040.
- ↑ Ilyas, JA, Vierling, JM (2011 Aug). An overview of emerging therapies for the treatment of chronic hepatitis C.. Clinics in liver disease 15 (3): 515–36. PMID 21867934.
- ↑ Foote BS, Spooner LM, Belliveau PP (September 2011). Boceprevir: a protease inhibitor for the treatment of chronic hepatitis C. Ann Pharmacother 45 (9): 1085–93. PMID 21828346. DOI: 10.1345/aph.1P744.
- ↑ Smith LS, Nelson M, Naik S, Woten J (May 2011). Telaprevir: an NS3/4A protease inhibitor for the treatment of chronic hepatitis C. Ann Pharmacother 45 (5): 639–48. PMID 21558488. DOI: 10.1345/aph.1P430.
- ↑ Ghany MG, Nelson DR, Strader DB, Thomas DL, Seeff LB (October 2011). An update on treatment of genotype 1 chronic hepatitis C virus infection: 2011 practice guideline by the American Association for the Study of Liver Diseases. Hepatology 54 (4): 1433–44. PMID 21898493. PMC 3229841. DOI: 10.1002/hep.24641.
- ↑ Alavian SM, Tabatabaei SV (April 2010). Treatment of chronic hepatitis C in polytransfused thalassaemic patients: a meta-analysis. J. Viral Hepat. 17 (4): 236–44. PMID 19638104. DOI: 10.1111/j.1365-2893.2009.01170.x.
- ↑ a b Hepatitis C and CAM: What the Science Says. NCCAM March 2011. (Retrieved 07 March 2011)
- ↑ Liu, J, Manheimer, E, Tsutani, K, Gluud, C (2003 Mar). Medicinal herbs for hepatitis C virus infection: a Cochrane hepatobiliary systematic review of randomized trials.. The American journal of gastroenterology 98 (3): 538–44. PMID 12650784.
- ↑ Rambaldi, A, Jacobs, BP, Gluud, C (17 oktober 2007). Milk thistle for alcoholic and/or hepatitis B or C virus liver diseases.. Cochrane database of systematic reviews (Online) (4): CD003620. PMID 17943794.
- ↑ Fung J, Lai CL, Hung I, et al. (September 2008). Chronic hepatitis C virus genotype 6 infection: response to pegylated interferon and ribavirin. The Journal of Infectious Diseases 198 (6): 808–12. PMID 18657036. DOI: 10.1086/591252.
- ↑ a b c WHO Hepatitis C factsheet (2011). Geraadpleegd op 13 juli 2011.
- ↑ Colacino, ed. by J. M., Heinz, B. A. (2004), Hepatitis prevention and treatment. Birkhäuser, Basel, pp. 32. ISBN 9783764359560.
- ↑ al.], edited by Gary W. Brunette ... [et, CDC health information for international travel : the Yellow Book 2012. Oxford University, New York, pp. 231. ISBN 9780199769018.
- ↑ a b Boyer, JL (2001), Liver cirrhosis and its development: proceedings of the Falk Symposium 115. Springer, 344. ISBN 9780792387602.
- ↑ Choo QL, Kuo G, Weiner AJ, Overby LR, Bradley DW, Houghton M (April 1989). Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome. Science 244 (4902): 359–62. PMID 2523562. DOI: 10.1126/science.2523562.
- ↑ Kuo G, Choo QL, Alter HJ, et al. (April 1989). An assay for circulating antibodies to a major etiologic virus of human non-A, non-B hepatitis. Science 244 (4902): 362–4. PMID 2496467. DOI: 10.1126/science.2496467.
- ↑ Winners Albert Lasker Award for Clinical Medical Research, The Lasker Foundation. Retrieved 20 February 2008.
- ↑ Houghton, M., Q.-L. Choo, and G. Kuo. NANBV Diagnostics and Vaccines. European Patent No. EP-0-3 18-216-A1. European Patent Office (filed 18 November 1988, published 31 May 1989).
- ↑ Wilken, Judge, United States Court of Appeals for the Federal Circuit. United States Court of Appeals for the Federal Circuit. Geraadpleegd op 11 January 2012.
- ↑ Eurosurveillance editorial, team (28 juli 2011). World Hepatitis Day 2011.. Euro surveillance : bulletin europeen sur les maladies transmissibles = European communicable disease bulletin 16 (30). PMID 21813077.
- ↑ a b Wong, JB (2006). Hepatitis C: cost of illness and considerations for the economic evaluation of antiviral therapies.. PharmacoEconomics 24 (7): 661–72. PMID 16802842.
- ↑ a b El Khoury, A. C., Klimack, W. K., Wallace, C., Razavi, H. (1 december 2011). Economic burden of hepatitis C-associated diseases in the United States. Journal of Viral Hepatitis. DOI: 10.1111/j.1365-2893.2011.01563.x.
- ↑ Hepatitis C Prevention, Support and Research ProgramHealth Canada. Public Health Agency of Canada (Nov 2003). Geraadpleegd op 10 January 2012.
- ↑ Zuckerman, edited by Howard Thomas, Stanley Lemon, Arie (2008), Viral Hepatitis., 3rd ed.. John Wiley & Sons, Oxford, pp. 532. ISBN 9781405143882.
- ↑ Ahn, J, Flamm, SL (2011 Aug). Hepatitis C therapy: other players in the game. Clinics in liver disease 15 (3): 641–56. PMID 21867942. DOI: 10.1016/j.cld.2011.05.008.
- ↑ Vermehren, J, Sarrazin, C (2011 Feb). New HCV therapies on the horizon.. Clinical microbiology and infection : the official publication of the European Society of Clinical Microbiology and Infectious Diseases 17 (2): 122–34. PMID 21087349.
