Methode naar Nierle-Tegge
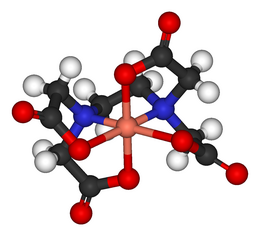
De methode naar Nierle-Tegge[1] is een bepaling van aldosen, reducerende suikers. De bepaling berust op het reduceren (door een suiker) van Cu2+ naar Cu+, dat als Cu2O neerslaat. De Cu2+ ionen komen voor in een complex met EDTA. Cu2O vormt geen complex met EDTA, zodat er na reactie tussen Cu2+ en de aldose een hoeveelheid EDTA vrijkomt die equivalent is met de hoeveelheid Cu2+ die gereageerd heeft met de reducerende suikers. Deze hoeveelheid vrij EDTA kan titrimetrisch worden bepaald met een Cu2+ oplossing. De methode lijkt sterk op de Methode naar Luff-Schoorl.
De methode bestaat uit 2 stappen:
- Reductie van Cu2+ tot Cu2O met Nierle-Tegge reagens, met vrijzetten van een equivalente hoeveelheid EDTA
- Het vrijgezette EDTA wordt getitreerd met een Cu2+ oplossing
Reductie van Cu2+[bewerken | brontekst bewerken]
De methode maakt gebruik van het Nierle-Tegge reagens. Dit reagens bestaat uit drie componenten:
- een 0.1 mol/L CuSO4 oplossing, ongeveer 25g CuSO4.5H2O per liter. Het koperion hierin is de eigenlijke oxidator.
- een 1 mol/L Na2CO3, ongeveer 286 gram per liter. De reactie verloopt alleen in basisch milieu, deze hoeveelheid natriumcarbonaat zorgt voor een pH van ongeveer 9,3-9,4.
- een 0,1 mol/L Na2H2EDTA-dihydraat oplossing, ongeveer 37,4 gram per liter. In het basische milieu van de reactie zou koper(II)hydroxide neerslaan als de koperionen niet in een complex, in dit geval EDTA, gebonden zijn.
Deze oplossing reageert met de reducerende suikers in het te analyseren monster volgens de reacties (het EDTAion wordt in reactievergelijkingen meestal als Y4− weergegeven):
Het Cu2O vormt een rood neerslag.
Praktisch wordt het te analyseren monster verdund tot 2-3g suiker per 100 mL oplossing. De verdunde oplossing wordt aangezuurd met ongeveer 2,5 mL 4 mol/L HCl. Van deze verdunning wordt dan 10 mL genomen en bij 10 mL Nierle-Tegge reagens gevoegd. Deze oplossing wordt gedurende 10 minuten tussen 65° en 85 °C verhit.
Titrimetrisch bepalen van de hoeveelheid EDTA[bewerken | brontekst bewerken]
Nadat de reductie is uitgevoerd, wordt de oplossing gekoeld tot kamertemperatuur, en aangelengd in een maatkolf van 250 mL met water. Van deze oplossing wordt 50 mL genomen, en getitreerd met een ongeveer 0.02M CuSO4 oplossing. Een geschikte indicator is murexide.
Berekening reducerende suikers[bewerken | brontekst bewerken]
Aangezien Cu2+ en EDTA2− reageren in een 1:1 verhouding en Cu2+ en C6H12O6 in een 2:1 verhouding, moet men het aantal mol Cu2+ die men heeft gebruikt om het vrije EDTA te binden, delen door twee om het aantal mol reducerende suikers te bepalen in het monster.
Zie ook[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|



