Regel van Markovnikov
In de organische chemie is de regel van Markovnikov (of regel van Markownikoff) de verwoording van een aantal waarnemingen bij reacties van alkenen met polaire reagentia zoals waterstofchloride en waterstofbromide. De regel werd rond 1870 geformuleerd door de Russische scheikundige Vladimir Markovnikov.[1][2] Samen met de regel van Markovnikov vormt de regel van Zajtsev een fenomenologische beschrijving van de reactie van alkenen met waterstofhalogeniden of de vorming van alkenen onder afstaan van een waterstofhalogenide.
De regel van Markovnikov luidt:
Bij de additie van een verbinding H-X aan een alkeen zal het waterstofatoom gebonden worden aan het koolstofatoom dat al de meeste waterstofatomen heeft, de groep X zal gebonden worden aan het koolstofatoom met de minste waterstofatomen.[3]
De regel van Markovnikov wordt geïllustreerd door de reactie van propeen met waterstofbromide:
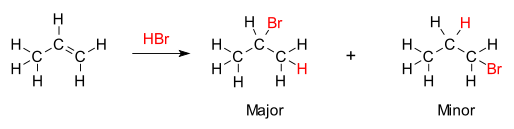
2-broompropaan is hier het voornaamste reactieproduct, in overeenstemming met de regel van Markovnikov.
Markovnikov formuleerde zijn regel op basis van de reactie van waterstofhalogeniden met alkenen (de hydrohalogenering). De regel bleek ook op te gaan voor de grote groep verbindingen met (gedeeltelijk) positief geladen waterstofatomen zoals water en alcoholen, waarbij dan alcoholen (met de OH-groep aan het koolstofatoom met de minste waterstofatomen) respectievelijk ethers gevormd werden.
De verklaring voor de regel kon Markovnikov nog niet geven omdat de ideeën rond de structuur van moleculen en reacties in 1870 nog niet ver genoeg ontwikkeld waren. Tegenwoordig kunnen we de waarneming verklaren via de vorming van het meest stabiele carbokation als overgangstoestand in de additie. Tijdens de additie wordt waterstof als positief ion aan een van de atomen van een dubbele binding overgedragen. De elektronen van de dubbele binding verzorgen de binding zodat een positieve lading op het andere koolstofatoom van de dubbele binding ontstaat. Hierdoor ontstaat een carbokation. Hoe meer koolstofatomen, of elektrondonerende groepen, aan het positieve koolstofatoom gebonden zijn, hoe stabieler het carbokation is. Het hoofdproduct van de reactie zal gevormd worden via het meest stabiele carbokation. Hierdoor zal het hoofdproduct van de additie van HX (waarbij X een willekeurig atoom / atoomgroep is die elektronegatiever is dan waterstof) aan een alkeen waterstof aan het minder gesubstitueerde en X aan de meer gesubstitueerde koolstofatoom hebben. Bewust is sprake van hoofdproduct: het minder stabiele carbokation wordt ook gevormd, en het reactieproduct ervan, H en X precies andersom aan het alkeen gebonden dus ook.
Historische context
[bewerken | brontekst bewerken]Een van de reacties waarop Markovnikov zijn regel baseerde was de in 1865 beschreven additie van waterstofjodide aan broometheen. Bij een andere gelegenheid werd het tussenproduct niet geïsoleerd maar de reactie ervan met vochtig Ag2O leverde aceetaldehyde, waarmee wel de koppeling van het halogeenatoom aan het koolstofatoom dat al een halogeen had aangetoond werd.

De regel werd voor het eerst in 1869 gepubliceerd, maar het duurde 60 jaar voor de chemische gemeenschap de regel ook als zodanig accepteerde. Mogelijk is dit het gevolg van het feit dat de regel als een voetnoot van liefst 4 pagina's in een artikel van 26 pagina's was opgenomen. Bovendien was veel van het experimentele werk dat als onderbouwing genoemd werd niet Markovnikovs eigen werk[2].
Anti-Markovnikov
[bewerken | brontekst bewerken]In een aantal gevallen gaat de regel van Markovnikov niet op. Er wordt dan gesproken van anti-Markovnikov-additie. Er kunnen verschillende reden zijn waarom afwijkingen optreden.
Waterstof is niet positief
[bewerken | brontekst bewerken]De additie van boranen aan dubbele bindingen (hydroboratie) verloopt naar de letter van de regel omgekeerd: boor aan het koolstofatoom met de meeste waterstofatomen en waterstof aan het koolstofatoom dat de minste waterstofatomen had. Het mechanisme, de vorming van een intermediair carbokation is echter gelijk, het verschil wordt gevormd door het feit dat waterstof elektronegatiever is dan boor. Na koppeling van het positieve - boor - deel van het molecule aan het alkeen koppelt het hydride met het gevormde carbokation.
Radicalen
[bewerken | brontekst bewerken]Reacties die niet via een carbokation verlopen maar via een radicaal gedragen zich tegenovergesteld aan de Markovnikov-regel. Het halogeen koppelt eerst aan het alkeen, en die eerste koppeling van het reagens is weer op het koolstofatoom dat de meeste waterstofatomen draagt: ook voor radicalen geldt dat hoe meer substituenten hoe stabieler het radicaal.
Katalysatoren
[bewerken | brontekst bewerken]Onder invloed van katalysatoren kan de additie ook omgekeerd verlopen: hydratatie van fenylacetyleen met goud als katalysator levert het Markovnikov-product: acetofenon. Met een speciale ruthenium-houdende katalysator (in situ gemaakt uit ruthenoceen met cyclopentadienyl, naftaleen en pyridine-liganden) levert het andere isomeer: 2-fenylacetaldehyde[4]:

Omleggingen
[bewerken | brontekst bewerken]Anti-Markovnikov gedrag komt ook soms tot uiting in omleggingsreacties: na de eerste reactie treedt zeer snel een wijziging op in het molecule, zo snel dat het eerste product eigenlijk niet geïsoleerd kan worden. In een door titanium(IV)chloride gekatalyseerde, formeel als nucleofiele substitutie beschreven reactie, van optisch zuiver 1 in het schema hieronder, worden twee racemische producten gevormd: 2a and 2b[5] :

Het ontstaan van de verschillende producten kan verklaard worden door aan te nemen dat de hydroxy-groep uit 1 aanleiding geeft tot het tertiaire carbokation A, dat vervolgens omlegt naar het schijnbaar minder stabiele ion B. Chloor kan vervolgens vanaf twee verschillende kanten dit positieve ion benaderen, waarbij de waargenomen reactieproducten ontstaan.
- ↑ W. Markownikoff (1870). Ueber die Abhängigkeit der verschiedenen Vertretbarkeit des Radicalwasserstoffs in den isomeren Buttersäuren. Annalen der Pharmacie 153 (1): 228–259. DOI: 10.1002/jlac.18701530204.
- ↑ a b Was Markovnikov’s Rule an Inspired Guess? Peter Hughes 1152 Journal of Chemical Education • Vol. 83 No. 8 August 2006
- ↑ Additions to Alkenes: Regiochemistry
- ↑ Highly Active in Situ Catalysts for Anti-Markovnikov Hydration of Terminal AlkynesAurélie Labonne, Thomas Kribber, and Lukas Hintermann Org. Lett.; 2006; 8(25) pp 5853 - 5856; (Letter) DOI:10.1021/ol062455k
- ↑ TiCl4 Induced Anti-Markovnikov Rearrangement Mugio Nishizawa, Yumiko Asai, and Hiroshi Imagawa Org. Lett.; 2006; 8(25) pp 5793 - 5796; (Letter) DOI:10.1021/ol062337x.
