Organonikkelchemie

In de organonikkelchemie worden stoffen bestudeerd waarin een directe binding optreedt tussen koolstof en nikkel. Nikkel is een metaal, en daarmee is de organonikkelchemie een subdiscipline van de organometaalchemie.[1]
Organonikkelverbindingen worden toegepast als katalysator, als synthon en in de chemical vapor deposition. De verbindingen treden ook op als - kort bestaande - intermediairen in een aantal reacties. De eerste organonikkelverbinding die beschreven is, nikkeltetracarbonyl, Ni(CO)4, dateert uit 1890. Kort daarna volgde de technische toepassing ervan in de zuivering van nikkel via het Mondprocess. Organonikkelverbindingen spelen een belangrijke technisch/industriële rol in bijvoorbeeld carbonyleringen, hydrocyaneringen en in het Shell higher olefin proces.
Verbindingen[bewerken | brontekst bewerken]
In de organonikkelchemie treedt nikkel op met de oxidatiegetallen 0, +1 en +2. De gelijkenis met de organopalladiumchemie is slechts oppervlakkig, hoewel beide metalen in hun reacties betrokken zijn bij afwisselende reductieve eliminaties en oxidatieve addities.
Nikkel-alkeencomplexen[bewerken | brontekst bewerken]
Er is een groot aantal complexen bekend van nikkel met alkenen. Nikkel heeft in deze complexen een formeel oxidatiegetal van 0, Ni0. De binding in deze complexen wordt beschreven met behulp van het Dewar-Chatt-Duncanson-model. Een illustratief voorbeeld van deze groep stoffen is Bis(cyclooctadieen)nikkel(0), Ni(COD)2, waarin twee cyclo-octadieenmoleculen als ligand optreden. Deze verbinding heeft 18 valentieelektronen, 10 van nikkel zelf en 4 keer 2 uit de vier dubbele bindingen. Deze vaste stof heeft een smeltpunt van 60 °C,[2] en wordt toegepast als katalysator.
Nikkel-allylcomplexen[bewerken | brontekst bewerken]

Allylhalogeniden reageren met Ni(CO)4 tot π-allyl complexen, (allyl)2Ni2Cl2. Op hun beurt zijn deze complexen een bron voor allyl-nucleofielen, een typisch voorbeeld van Umpolung. In (allyl)2Ni2Cl2 en (allyl)Ni(C5H5) heeft nikkel oxidatiegetal +2, met respectievelijk 16 en 18 elektronen.
Nikkeloceen[bewerken | brontekst bewerken]
Nikkeloceen NiCp2, met nikkel als tweewaardig kation en 20 valentieelektronen rond nikkel, is het voornaamste metalloceen van nikkel. Nikkeloceen kan tot NiCp2+ geoxideerd worden. Het overeenkomstige palladoceen en platinoceen zijn niet bekend (januari 2012).
Nikkel-carbeencomplexen[bewerken | brontekst bewerken]
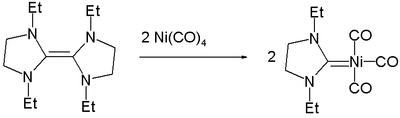
Nikkel vormt carbeencomplexen waarin formeel een dubbele bindi ng tussne koolstof en nikkel optreedt: C = Ni.
Nikkel met 12 valentieelektronen[bewerken | brontekst bewerken]
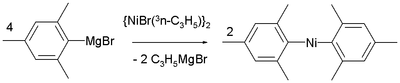
Nikkelverbindingen van het type NiR2 komen ook voor met slechts 12 valentieelektronen. In oplossingen zullen deze stoffen, via solvatatie, hun aantal valentieelektronen altijd uitbouwen. Een echte verbinding met 12 valentieelektronen is di(mesityl)nikkel dat ontstaat uit (η3allyl)2Ni2Br2 en het corresponderende Grignard-reagens.
Reacties[bewerken | brontekst bewerken]
In onderstaande voorbeelden van reacties van organonikkelverbindingen worden de reacties allemaal uitgevoerd in aanwezigheid van anorganische nikkelzouten. De structuur ven de verbindingen waarin nikkel aan koolstof gebonden is blijft meestal in het midden. Omdat de aanwezigheid van nikkel wel cruciaal is voor het verlopen van de reacties, is het zeer waarschijnlijk dat er organonikkelverbindingen optreden tijdens het verloop van de reacties.
Oligomerisatie van alkenen en alkynen[bewerken | brontekst bewerken]
Organonikkelverbindingen katalyseren de oligomerisatie van alkenen en alkynen. Deze eigenschap kwam aan het licht tijdens onderzoek naar de polymerisatie van ethyn in de jaren 50 van de 20e eeuw. Het bleek dat sporen nikkel, afkomstig van de autoclaaf waarin de reactie werd uitgevoerd, de propagatiereactie blokkeerden in het voordeel van de terminatiereactie. Een eindstandig alkeen ontstond: de polymerisatie van etheen stopte heel simpel bij 1-buteen. Dit zogenoemde nikkeleffect initieerde het onderzoek naar vergelijkbare katalysatoren. Deze zoektocht resulteerde uiteindelijk in de ontwikkeling van de Ziegler-Natta-katalysatoren waarmee zeer hoogmoleculaire, regelmatige polymeren gemaakt kunnen worden.
Een praktische toepassing van de alkynoligomerisatie is de door Reppe ontwikkelde synthese van cyclooctatetraeen:
Formeel is dit een [2+2+2+2]cycloadditie. De oligomerisatie van etheen met 1,3-butadieen heeft een tijdlang industriële betekenis gehad in de synthese van trans-1,4-hexadieen.
Formele [2+2+2] cycloaddities treden ook op. Zelfs een bijna hypothetisch molecuul als benzyn laat zich op deze manier vastleggen.[3] Benzyn wordt In situ gemaakt uit een benzeenverbinding met een triflaat en een trimethylsilylgroep in 1,2-positie ten opzichte van elkaar. De reactie wordt uitgevoerd in aanwezigheid van bijvoorbeeld 1,7-octadiyn en een mengsel van nikkel(II)bromide / zink katalysator (eigenlijk: NiBr2 bis(difenylfosfino) ethaan / Zn). Het overeenkomstige naftaleen is het reactieproduct.
In de katalytische cyclus speelt metallisch zink de rol van reductor, het zet Ni+2 om naar Ni0 dat weer met 2 alkynbindingen kan coördineren. Er volgt een cyclometalatiestap waarbij een nikkelacyclopentadieen als intermediair ontstaat. Er volgt een inschuifreactie naar een nikkelacycloheptatrieen. Uiteindelijk komt het tetrahydroantraceen via een reductieve eliminatie vrij.
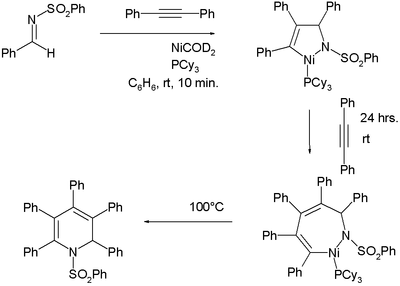
De vorming van de intermediaire organonikkelverbindingen is uit de totaalreactie niet altijd duidelijk. Onder speciale omstandigheden konden twee van dergelijk verbindingen kwantitatief geïsoleerd worden.[4]
In een van de studies[5] wordt aangegeven dat de reactie eigenlijk alleen goed werkt met symmetrisch gesubstitueerde acetylenen. De reactie is nauwelijks regioselectief zodat een eindstandig alkyn al aanleiding geeft tot 7 isomere tetrameren, die alleen van elkaar verschillen in de relatieve posities van de substituenten en dubbele bindingen. Een manier om dit probleem (deels) op te lossen is gebruik te maken van speciale diynen:
De gekozen reactieomstandigheden hebben ook tot gevolg dat de (bij)reactie naar het trimeer, een gesubstitueerd benzeen, geminimaliseerd wordt..
Koppelingsreacties[bewerken | brontekst bewerken]
Mert behulp van nikkelverbindingen kunnen koppelingsreacties tussen allyl- en aryl-halogeniden gerealiseerd worden. Ook bij de Kumada- en de Negishi-koppeling worden katalytische hoeveelheden van nikkelverbindingen gebruikt.
Nikkel-gekatalyseerde carbonylering[bewerken | brontekst bewerken]
Nikkel katalyseert de additie van koolstofmonoxide aan alkenen en alkynen. De industriële productie van acrylzuur is een tijd gebaseerd geweest op de reactie van acetyleen, koolstofmonoxide en water bij 40-55 atm en and 160−200°C onder invloed van nikkel(II)bromide en een koperhalide.
[bewerken | brontekst bewerken]
Navigatie Koolstof-elementbinding
Bronnen, noten en/of referenties
|