Gebogen moleculaire geometrie
Uiterlijk
| Gebogen moleculaire geometrie | ||||
|---|---|---|---|---|
| Ruimtelijke structuur | ||||
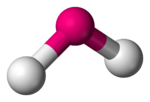
| ||||
Ruimtelijke schikking van de atomen
| ||||
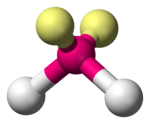
| ||||
■ twee vrije elektronenparen | ||||

| ||||
■ één vrij elektronenpaar | ||||
| Eigenschappen | ||||
| Puntgroep | C2v | |||
| Bindende elektronenparen | 2 | |||
| Vrije elektronenparen | 1 of 2 | |||
| Bindingshoeken | 120° of 109,5° | |||
| Coördinatiegetal | 2 | |||
| AXE-symbool | geknikt: AX2E1 gebogen: AX2E2 | |||
| ||||
In de scheikunde verwijst een gebogen moleculaire geometrie ernaar, dat een molecuul een geometrie heeft waarbij drie atomen via twee bindingen met elkaar zijn verbonden en waarbij deze twee bindingen een hoek kleiner dan 180° maken. Water heeft deze moleculaire geometrie, waarbij de twee O-H-bindingen een hoek van 104,45° maken. Andere voorbeelden zijn stikstofdioxide, waterstofselenide en zwaveldichloride.
Het centrale atoom van deze verbindingen heeft meestal een binding met twee vrije elektronenparen. In het geval dat het centrale element een binding met maar één vrij elektronenpaar heeft, wordt soms van een geknikte structuur gesproken, omdat de bindingshoek groter is. Die is dan 120°. Zwaveldioxide is hiervan een voorbeeld.
