Tubocurarine
| D-Tubocurarine | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuurformule van Tubocurarine
| ||||
| Algemeen | ||||
| Molecuulformule | C37H42Cl2N2O6 | |||
| IUPAC-naam | 7',12'-dihydroxy-6,6'-dimethoxy-2,2',2'-trimethyltubocuraranium | |||
| Andere namen | d-Turbocurarine | |||
| Molmassa | 609.73 g/mol | |||
| CAS-nummer | 6989-98-6 | |||
| PubChem | 6000 | |||
| Wikidata | Q421268 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| EG-Index-nummer | 615-023-7 | |||
| ||||
Tubocurarine (afgekort DTC) is een toxische alkaloïde, dat van nature voorkomt in de bast van de Zuid-Amerikaanse klimplant Chondrodendron tomentosum. In het verleden werd tubocurarine gebruikt als een bestanddeel voor pijlgif. In het midden van de 20e eeuw ontdekte men dat tubocurarine de skeletspieren kan ontspannen, waardoor het destijds veel werd gebruikt bij medische ingrepen, met name als anestheticum. Het wordt tegenwoordig zelden gebruikt als bijmiddel voor anesthesie omdat er veiligere alternatieven beschikbaar zijn, zoals rocuronium.
Geschiedenis
[bewerken | brontekst bewerken]Tubocurarine is een mono-quaternair alkaloïde, dat van oorsprong voorkomt in de bast van lianen in grote delen van Zuid-Amerika. In Europa is deze plant bekend sinds de Spaanse verovering van Zuid-Amerika. Zuid-Amerikaanse indianen gebruikten extracten van de lianen als pijlgif. De verzamelnaam voor de verschillende pijlgifstoffen is curare. Jachtbuit die met curares zijn aangetast kan gewoon gegeten worden omdat deze gifstoffen moeilijk de slijmvliesmembranen in het spijsverterinskanaal passeren. Fysioloog Claude Bernard toonde in 1856 aan dat de opnamesnelheid vanuit het maag-darmkanaal kleiner is dan de uitscheiding ervan door de nieren. Daarnaast wees hij de koppeling tussen zenuw en spier als plaats van interactie aan.[1] In 1977 werd aangetoond dat de werking van tubocurarine zich beperkte tot de skeletspieren.[2]
Biochemie
[bewerken | brontekst bewerken]Werking
[bewerken | brontekst bewerken]Tubocurarine heeft een sterke fysiologische werking op het menselijk lichaam, doordat het inwerkt op het perifeer zenuwstelsel. Het kan in voldoende concentraties de skeletspieren volledig doen verslappen. Tubocurarine wordt geclassificeerd als een niet-depolariserend spierrelaxans. In normale omstandigheden activeert de neurotransmitter acetylcholine de skeletspieren. Acetylcholine wordt door choline-acetyltransferase in de neuronen geproduceerd en via het axon naar de synaptische spleet getransporteerd. Tubocurarine werkt als een antagonist voor de nicotine-acetylcholinereceptor (nAChr). Dit houdt in dat het de bindingsplaats van acetylcholine aan zijn receptor blokkeert. De spier ontvangt geen prikkels meer, waardoor de spier zich niet meer kan samentrekken en volledig ontspant.
Biosynthese
[bewerken | brontekst bewerken]Tubocurarine een derivaat van de benzylisochinolinen. De structuur van het molecuul werd pas in 1970 volledig ontrafeld.[3] Bij de biosynthese van tubocurarine worden twee enantiomeren van N-methylcoclaurine in een radicaalreactie aan elkaar gekoppeld. Deze twee enantiomeren ontstaan uit de reactie tussen dopamine en 4-hydroxyfenylacetaldehyde. Zowel dopamine als 4-hydroxyfenylacetaldehyde zijn afkomstig uit de tyrosinestofwisseling. Methylering van de amine- en hydroxylgroepen wordt mogelijk gemaakt door S-adenosylmethionine (SAM). In de laatste stap wordt een extra methylgroep gebonden aan een van de stikstofatomen. Zie de onderstaande reactie.
| Radicaalmechanisme van tubocurarinesynthese |
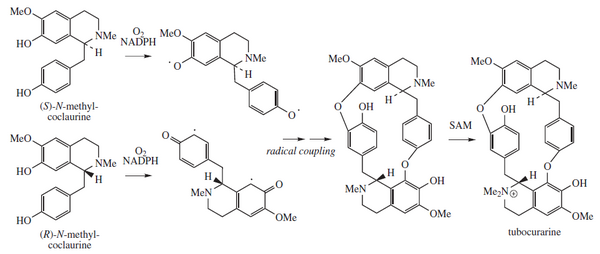
|
Onder fysiologische omstandigheden is het tweede stikstofatoom geprotoneerd, zodat de stof als tweewaardig ion voorkomt. De standaard tegenionen zijn chloride.
Toxologie
[bewerken | brontekst bewerken]Iemand die tubocurarine toegediend krijgt zal niet in staat zijn de spieren, waaronder het middenrif, te bewegen. Een voldoende grote dosis zal daarom resulteren in de dood door verstikking, tenzij het slachtoffer kunstmatige wordt beademd. De LD50 voor muizen en konijnen is respectievelijk 0,13 mg/kg en 0,146 mg/kg intraveneus. Tubocurarine maakt histamine vrij en veroorzaakt hypotensie.[4]
Zie ook
[bewerken | brontekst bewerken]Bron
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Tubocurarine chloride op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
Referenties
- ↑ C. Bernard. (1856). Analyse physiologie des propriétés des actions de curare et de la nicotine sure systèmes musculaire et nerveux au moyen du curare Compt. Rend.. 43 pag.: 305–319
- ↑ A.M. Bechter. (1977). The civilizing of curare: a history of its development and introduction into anesthesiology Anesth.Analg.. 56 (2): pag.: 305–319 DOI:10.1213/00000539-197703000-00032 , geraadpleegd op 16 oktober 2018 Internetpagina: The civilizing of curare geraadpleegd op 16 oktober 2018 (alleen samenvatting, voor volledig artikel is betaald abonnement nodig) PubMed: 322548
- ↑ Everett AJ, Lowe LA, Wilkinson S (1970). J. Chem. Soc. Chem. Commun.: 1020.
- ↑ Gesler, HM. Hoppe JO. (1956). 3,6-bis(3-diethylaminopropoxy)pyridazine bismethiodide, a long-acting neuromuscular blocking agent. The Journal of Pharmacology and Experimental Therapeutics 118.
