Williamson-ethersynthese
De Williamson-ethersynthese is een eenvoudige en veelzijdige methode om ethers te synthetiseren, en is geschikt voor de vorming van zowel symmetrische als asymmetrische ethers. De reactie is genoemd naar Alexander Williamson, die ze reeds in 1850 beschreef.[1]
De Williamson-ethersynthese is een reactie van een alkylhalogenide met een alkoxide (de geconjugeerde base van een alcohol). De reactie verloopt door middel van een SN2-reactie:

De groepen R1 en R2 stellen hierbij alkyl- of arylgroepen voor. Deze kunnen beiden gelijk zijn (dan wordt een symmetrisch ether gevormd) of zij kunnen verschillen (dan wordt een asymmetrisch ether gevormd). Het element X is het halogenide (de leaving group), doorgaans chloor, broom of jood. Aangezien de binding tussen fluor en koolstof te sterk is, worden alkylfluoriden niet ingezet in deze reactie. Als alternatief voor halogeniden kunnen ook triflaten worden ingezet.
Wanneer er secundaire of benzylische alkylhalogeniden gebruikt worden, kan de reactie ook via een SN1-reactie verlopen. Bij een SN1-reactie vindt er eerst nog heterolytische splitsing plaats, waardoor een carbokation gevormd wordt, waarna het nucleofiele alkoxide hierop aanvalt. Bij dit soort reacties wordt een polair oplosmiddel gebruikt, omdat dit de solvatatie van vrije ionen bevordert. Hierdoor komt het reactie-evenwicht sterker naar rechts te liggen.
Wanneer tertiaire alkylhalogeniden gebruikt worden, kan competitie met E2-eliminatie optreden, zoals de reactie tussen natriummethoxide en 2-jood-2-methylpropaan:
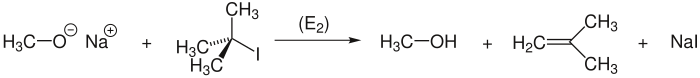
Voorbeelden[bewerken | brontekst bewerken]
De reactie van natriumethoxide met joodethaan levert di-ethylether (een symmetrisch ether) en natriumjodide:
In bijzondere gevallen wordt gebruikgemaakt van zilver(I)oxide als koppelingsreagens:[2]

Uitvoering[bewerken | brontekst bewerken]
Alkoxiden zijn reactieve verbindingen (het zijn sterke basen, maar tevens goede nucleofielen) en ze worden doorgaans vlak voor de ethersynthese bereid of in situ aangemaakt door een sterke base, zoals natriumhydride, toe te voegen aan een oplossing van het alcohol. Vanwege deze reactiviteit is het soms nodig om beschermende groepen te gebruiken om bepaalde basegevoelige functionele groepen, zoals hydroxyl- of aminegroepen, te vrijwaren.
De reactie verloopt het best met alkoxiden van primaire alcoholen; die van secundaire of tertiaire alcoholen reageren minder goed, zeker als het om grotere moleculen gaat die slecht oplosbaar zijn. In dergelijke gevallen kan men een fase-transfer-katalysator gebruiken, zoals een quaternair ammoniumzout of een kroonether.
De reactie verloopt in een oplosmiddel: dat kan het alcohol zelf zijn of een polair oplosmiddel zoals dimethylsulfoxide, dimethylformamide of tetrahydrofuraan. Daar ethers vaak vluchtige stoffen zijn, kunnen ze meestal tijdens de reactie uit het reactiemengsel weggedestilleerd worden. De reactie gebeurt best in watervrije omstandigheden omdat er anders nevenreacties kunnen optreden die de opbrengst aan ether verminderen. De belangrijkste nevenreactie is dat het alkoxide onmiddellijk weer geprotoneerd en dus inactief wordt.
De reactie gaat ook met een dialkylsulfaat in plaats van het alkylhalogenide. Dit is vooral bruikbaar voor de bereiding van fenolethers. Een voorbeeld van deze reactie is de synthese van anisol uit natriumfenoxide en dimethylsulfaat:
Bronnen, noten en/of referenties
|


