Trögers base
| Trögers base | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuurformule van Trögers base
| ||||

| ||||
Configuratie van de twee enantiomeren: de (5S,11S)-(–)-vorm (boven) en de (5R,11R)-(+)-vorm (onder)
| ||||
| Algemeen | ||||
| Molecuulformule | C17H18N2 | |||
| IUPAC-naam | (±)-2,8-dimethyl-6H,12H-5,11-methanodibenzo[b,f][1,5]diazocine | |||
| Molmassa | 250,34 g/mol | |||
| SMILES | CC1=CC2=C(C=C1)N3CC4=C(C=CC(=C4)C)N(C2)C3
| |||
| InChI | 1S/C17H18N2/c1-12-3-5-16-14(7-12)9-18-11-19(16)10-15-8-13(2)4-6-17(15)18/h3-8H,9-11H2,1-2H3
| |||
| CAS-nummer | 529-81-7 | |||
| PubChem | 196981 | |||
| Wikidata | Q410493 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H315 - H319 - H335 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P261 - P305+P351+P338 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Smeltpunt | 133-136 °C | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Trögers base, genoemd naar haar ontdekker Julius Tröger (Duits scheikundige, 1862-1942), is een heterocyclische verbinding met als brutoformule C17H18N2.
Synthese[bewerken | brontekst bewerken]
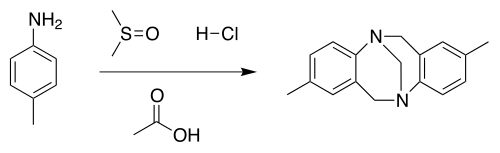
Julius Tröger bereidde de verbinding voor het eerst in 1887, vertrekkende van p-toluïdine en formaldehyde in zuur milieu.[1]
De correcte structuurformule van de verbinding werd echter pas in 1935 gevonden.[2]
In plaats van formaldehyde kan ook een andere methyleenbron gebruikt worden, zoals hexamethyleentetramine. Al deze methoden leveren een racemisch mengsel op van de twee enantiomeren.
Structuur en eigenschappen[bewerken | brontekst bewerken]
Trögers base is een symmetrische verbinding met vier zesringen, waarvan er twee aromatisch zijn. Ze bevat twee piramidale stikstofatomen. De methyleenbrug ertussen verhindert een piramidale inversie van de stikstofatomen, zodat de molecule een stabiele configuratie heeft, namelijk een starre V-vorm. De twee aromatische ringen staan daardoor bijna loodrecht op elkaar. Het hoekpunt van de V vormt een hydrofobe caviteit.
Doordat geen piramidale inversie mogelijk is, vormen de stikstofatomen elk een chiraal centrum. Er bestaan twee stabiele enantiomeren van deze base, de (R,R)- en de (S,S)-vorm. De enantiomeren kunnen gescheiden worden langs chromatografische weg. Dit gebeurde voor het eerst in 1944 door Prelog en Wieland.[3]
Derivaten en analoga[bewerken | brontekst bewerken]
Derivaten van Trögers base kunnen bekomen worden door functionele groepen in te voeren op de methyleenbruggen of door elektrofiele aromatische substitutie op de aromatische ringen. De synthese van niet-symmetrische analoga is mogelijk in een stapsgewijze procedure, uitgaande van twee verschillend gesubstitueerde anilinederivaten. Er zijn vele van deze analoga bekend, waaronder ook macrocyclische verbindingen. Ze kunnen onder meer in de synthese van metaalliganden, bij asymmetrische katalyse, of als gastheermoleculen in de supramoleculaire chemie gebruikt worden.[4]
Bronnen, noten en/of referenties
|