Cis-trans-isomerie
Cis-trans-isomerie, ook wel bekend als Z/E-isomerie of geometrische isomerie, is een vorm van stereo-isomerie. Het concept wordt zowel in de organische als anorganische chemie toegepast. De woordelementen cis en trans komen uit het Latijn, waarin cis betekent 'aan dezelfde kant' en trans 'aan de andere kant' of 'eroverheen'. Cis-trans-isomerie komt zowel voor in organische verbindingen als in anorganische coördinatieverbindingen.
Organische chemie[bewerken | brontekst bewerken]
Dubbele binding[bewerken | brontekst bewerken]
Functionele groepen die aan weerszijden van een dubbele binding of aan weerszijden van een ringstructuur liggen, kunnen of aan dezelfde kant (de cis-vorm), of aan tegengestelde kanten van elkaar (de trans-vorm) liggen. Dit komt doordat een dubbele koolstof-koolstofbinding, in tegenstelling tot een enkele, niet vrij kan roteren.
In de tegenwoordige scheikundige nomenclatuur wordt echter gebruikgemaakt van de Z/E-aanduiding. Hiertoe worden de atoomnummers van de eerstgebonden atomen aan de dubbele binding met elkaar vergeleken. Indien de twee atomen met het hoogste atoomnummer aan dezelfde zijde van de dubbele binding zitten, wordt gesproken van de Z-configuratie (van het Duitse zusammen). In het andere geval is sprake van de E-configuratie (van het Duitse entgegen). In ringsystemen wordt enkel gebruikgemaakt van de cis- en trans-notatie.
1,2-dichlooretheen kan bijvoorbeeld voorkomen als cis- of als trans-1,2-dichlooretheen (ook aangeduid als respectievelijk Z- en E-1,2-dichlooretheen):

|

|
| cis-1,2-dichlooretheen of Z-1,2-dichlooretheen |
trans-1,2-dichlooretheen of E-1,2-dichlooretheen |
In de natuur komen veel onverzadigde en meervoudig onverzadigde vetzuren voor, die in het algemeen de cis-configuratie hebben. Transvetzuren komen vooral in chemisch geharde vetten voor.
Cyclische verbindingen[bewerken | brontekst bewerken]
|
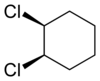
| cis-1,2-dichlorocyclohexaan |
|
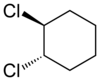
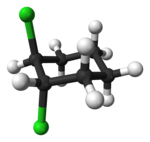
| trans-1,2-dichlorocyclohexaan |
In tweevoudig gesubstitueerde cyclische verbindingen treedt ook cis/trans-isomerie op, zoals in de voorbeeldverbinding 1,2-dichloorcyclohexaan. De twee substituenten kunnen zich beiden aan dezelfde kant bevinden, de structuur wordt dan als cis beschreven. Bevinden de twee of juist ieder aan een kant, dan wordt van een trans-verbinding gesproken.
In structuurformules is dit duidelijk te zien, omdat de ringen dan plat in het vlak van de tekening worden weergegeven. De chloor-atomen kunnen voor het vlak van de tekening liggen, de binding wordt aangegeven door de breder wordende getrokken streep. Liggen de chlooratomen achter het vlak van de tekening, dan wordt de binding aangegeven door een steeds breder wordende arcering.
In de ruimtelijke molecuulmodellen is een en ander lastiger te zien door de draaiing tussen de delen van het molecuul.
Het cis-1,2-dichloorcyclopentaan zal stabieler zijn dan het overeenkomstige trans isomeer.
Anorganische chemie[bewerken | brontekst bewerken]
- Cis-trans-isomerie in kobaltcomplexen
-
cis-CoCl2(NH3)4+
-
trans-CoCl2(NH3)4+
De aanduiding cis en trans wordt vooral toegepast bij complexen van metaalionen om aan te geven hoe de liganden ten opzichte van elkaar geplaatst zijn.
In complexen met een zesvoudige omringing zijn de liganden doorgaans gerangschikt volgens een octaëdrische moleculaire geometrie. Voor tetra-amminedichlorokobalt(III), een coördinatieverbinding met de formule CoCl2(NH3)4+, kunnen de twee chloorliganden trans, op twee tegenover elkaar liggende zijden een plaats vinden, of cis, op twee naast elkaar liggende vlakken, ten opzichte van elkaar staan.


