Grignard-reactie
De Grignard-reactie is een organische reactie waarbij een organomagnesiumhalogenide (het Grignard-reagens) met een carbonylverbinding reageert tot een alcohol. Het is een belangrijke syntheseroute in de organische chemie, omdat er op relatief eenvoudige manier een koolstof-koolstofbinding wordt gevormd.

De Grignard-reagentia en hun reactiviteit ten opzichte van elektrofielen werden ontdekt en ontwikkeld door Victor Grignard. Hij werd in 1912 voor zijn werk onderscheiden met de Nobelprijs voor de Scheikunde.
Verder kan de Grignard-reactie worden ingezet om bindingen te vormen tussen koolstof en fosfor, tin, silicium of boor. De reactie is ook niet beperkt tot carbonylverbindingen als elektrofielen: ook andere verbindingen, zoals disulfiden, epoxiden en imines komen in aanmerking.
Het Grignard-reagens

De binding tussen koolstof en een halogeen kan in veel gevallen worden geconverteerd in een koolstof-metaalbinding. In het geval van de Grignard-reactie betreft dit een koolstof-magnesiumbinding. In alle gevallen resulteert dit in de vorming van een organometaalverbinding. Omdat het metaal minder elektronegatief is dan de koolstof, is de binding zodanig gepolariseerd dat het koolstofatoom, dat rechtstreeks aan het metaal gebonden is, zich als nucleofiel gedraagt.
De Grignard-reagentia worden bereid door een organisch halogenide te laten reageren met magnesium in een droge ether als oplosmiddel, zoals di-ethylether, THF of MTBE. Een kleine hoeveelheid di-jood, dibroom of 1,2-dibroomethaan moet worden toegevoegd om de magnesium te activeren. Ether is een veelgebruikt oplosmiddel bij dergelijke reacties omdat het als Lewisbase optreedt en zo het organomagnesiumhalogenide door adductvorming stabiliseert. De ether moet volledig droog zijn, omdat de minste sporen water leiden tot protonering van de organometaalverbinding.
Reactiemechanisme
Additie van het nucleofiele Grignard-reagens is een voorbeeld van een nucleofiele carbonyladditie en verloopt via een zesringintermediair.[1] Na protonering van het ontstane alkoxide wordt het alcohol gevormd:

Omdat aan de ene kant deze organometaalreagentia zulke krachtige nucleofielen zijn en aan de andere kant de koolstof-koolstofbinding een zeer hoge vormingswarmte bezit, is de reactie irreversibel.
Reacties
Reactie met carbonylverbindingen
De meest voor de hand liggende en toegepaste Grignard-reactie is deze met carbonylverbindingen als elektrofiel. Er komen zeer uiteenlopende reacties voor:

De meest toegepaste reacties zijn de alkyleringen van ketonen en aldehyden, met vorming van alcoholen. Daarnaast zijn er ook andere reacties mogelijk:
- De reactie met koolstofdioxide levert (na protonering) een carbonzuur op
- De reactie met een zuurchloride, ester, thio-ester zuuranhydride of amide levert via een nucleofiele acylsubstitutie een keton of aldehyde op
Reacties met andere elektrofielen
Naast carbonylverbindingen treden Grignard-reagentia ook als alkylerend reagens bij andere elektrofielen op:

Bindingsvorming tussen koolstof en een heteroatoom
Niet alleen Grignard-reacties met vorming van een koolstof-koolstofbinding kunnen uitgevoerd worden, maar ook naar andere elementen toe:
- Reactie van een Grignard-reagens met tributyltinchloride levert vorming van een koolstof-tinbinding
- Reactie met een ester van boorzuur levert een organoboorverbinding
- Reactie met chloordifenylfosfaan levert een organofosforverbinding
- Reactie met trimethylchloorsilaan levert een organosiliciumverbinding
Koppelingsreacties
Een Grignard-reagens kan ingezet worden bij bepaalde koppelingsreacties. Een voorbeeld is de vorming van 4-nonylbenzoëzuur uit reactie van 4-chloormethylbenzoaat en nonylmagnesiumbromide, in aanwezigheid van tris(acetylacetonaat)ijzer(III). Zonder aanwezigheid van het acetylacetoncomplex van ijzer zou eerst additie aan de carbonylgroep van de ester optreden.[2]

Industriële toepassing
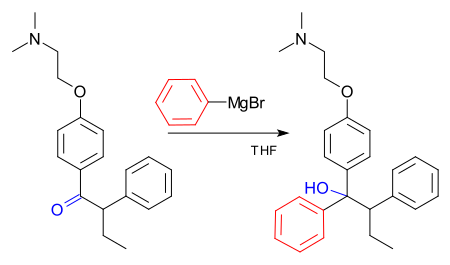
Een voorbeeld van de industriële toepassing van de Grignard-reactie is de productie van tamoxifen, een geneesmiddel met een anti-oestrogene werking.
Zie ook
- ↑ (en) K. Maruyama & T. Katagiri (1989) - Mechanism of the Grignard reaction, J. Phys. Org. Chem., 2 (3), p. 205-213
- ↑ (en) A. Fürstner, A. Leitner & G. Seidel (2005) - 4-Nonylbenzoic Acid, Org. Synth., 81, pp. 33–42
