Peroxysalpeterigzuur
| Peroxysalpeterigzuur | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuurformule van peroxysalpeterigzuur
| ||||
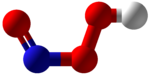
| ||||
cis-vorm van peroxysalpeterigzuur
| ||||

| ||||
trans-vorm van peroxysalpeterigzuur
| ||||
| Algemeen | ||||
| Molecuulformule | HNO3 | |||
| IUPAC-naam | (Hydridodioxido)oxidonitrogen[1][2] | |||
| Andere namen | Peroxysalpetrigzuur, Peroxynitrous acid | |||
| Molmassa | 63,0128 g/mol | |||
| SMILES | OON=O
| |||
| CAS-nummer | 14691-52-2 | |||
| PubChem | 123349 | |||
| Wikidata | Q7169514 | |||
| Evenwichtsconstante(n) | pKz = ~6.8 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Peroxysalpeterigzuur (HNO3 O=N-O-OH) is een reactieve stikstofcomponent. Het is de geprotoneerde vorm, het geconjugeerde zuur, van peroxynitriet (ONOO−). Het zuur heeft een pKz van ongeveer ~6,8. In vivo wordt het gevormd via de diffusie gecontroleerde reactie van stikstofmonoxide () en superoxide (). De verbinding bestaat als in een cis/trans mengsel dat isomeriseert met een snelheidsconstante k = 1.2 s−1, een proces waarbij tot 5% aan hydroxyl- en stikstofdioxide-radicalen gevormd kan worden.
Aromatische verbindingen worden door peroxysalpeterigzuur in lage opbrengst geoxideerd en genitreerd. In het mechanisme van deze reactie kan een complex van ONOOH en de aromaat optreden, in combinatie met een overgang van cis- naar de trans-configuratie van ONOOH.[3] Peroxysalpeterzuur speelt ook een belangrijke rol in de atmosfeerchemie.
Peroxysalpeterigzuur is een isomeer van het veel bekendere salpeterzuur.
Bronnen, noten en/of referenties
|


