Hydroxonium
| Hydroxonium | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
| ||||
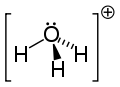
Structuurformule van hydroxonium
| ||||

| ||||
Molecuulmodel van hydroxonium
| ||||
| Algemeen | ||||
| Molecuulformule | H3O+ | |||
| IUPAC-naam | oxonium | |||
| Andere namen | hydronium | |||
| Molmassa | 19,02322 g/mol | |||
| SMILES | [OH3+]
| |||
| InChI | 1S/H2O/h1H2/p+1
| |||
| CAS-nummer | 13968-08-6 | |||
| PubChem | 123332 | |||
| Wikidata | Q849881 | |||
| Evenwichtsconstante(n) | pKa = 0 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Het hydroxonium-ion, ook bekend als oxonium- of hydronium-ion, is een ion met de formule H3O+. Het is een positief geladen ion (kation) dat gevormd wordt wanneer water (H2O) een waterstofion (H+) opneemt. Het hydroxonium-ion heeft een pKa-waarde (zuurconstante) van 0. Het is het sterkste zuur dat opgelost in water stabiel is. Een nog sterker zuur, zoals zoutzuur (HCl), zal een proton afgeven aan water, dat zo in een hydroxonium-ion omgezet worden. De pH van een waterige oplossing wordt uitsluitend bepaald door de H3O+-concentratie (of correcter: de activiteit van de hydroxonium-ionen) in de oplossing.
Ionisatie van water[bewerken | brontekst bewerken]
Water ondervindt ook in pure toestand een kleine mate van ionisatie. Dit gebeurt wanneer een watermolecuul een proton afstaat aan een ander watermolecuul. Dit wordt de eigendissociatie of autoprotolyse van water genoemd, en kan worden gezien als een evenwichtsreactie:
Het hydroxonium-ion is daarmee volgens de theorie van Johannes Nicolaus Brønsted het geconjugeerde zuur van water:
De mate van ionisatie is echter heel klein: de K-waarde voor de eigendissociatie van water is 10-14. Dit getal wordt wel de waterconstante (Kw) genoemd.
Deeltjesmodel voor zure oplossingen[bewerken | brontekst bewerken]
Waterstofionen of protons (H+) komen in water altijd gehydrateerd (verbonden met watermoleculen) voor. Dit wordt in chemische reacties vaak, maar beslist niet altijd, genoteerd als H3O+. Beide notaties worden naast, en soms door elkaar gebruikt. Vooral in de organische synthese wordt van de notatie H+ gebruikgemaakt. Hydroxonium verwijst naar een gehydrateerd waterstofion. Wanneer de nadruk gelegd moet worden op de zuur-base-eigenschappen, is H3O+ een praktische beschrijving.
De werkelijkheid is echter complexer. Een proton is in water niet aan slechts één watermolecule gebonden. Formules als H5O2+, H7O3+ en H9O4+ vormen een reeks waarin de werkelijke toestand van protonen in water steeds beter beschreven wordt.[1] Zure waterige oplossingen bestaan uit een verzameling van clusters van geprotoneerde watermoleculen.
Voor veel reacties waarin een waterstofion noodzakelijk is om de reactie uit te voeren, zonder dat de nadruk gelegd wordt op de zuur-base-aspecten van de reactie, wordt de reactievergelijking vaak een stuk eenvoudiger als de hydratatie-mantel, net als bij gewone ionen, weggelaten wordt. Vergelijk
met
Bronnen, noten en/of referenties
|




