Natriumtetrachloorauraat(III)
| Natriumtetrachloorauraat(III)[1] | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
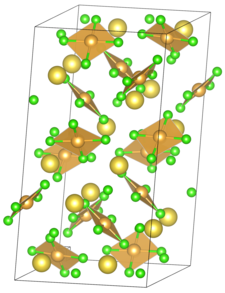
| ||||
__ Na+ __ Au3+ __ Cl−
| ||||
| Algemeen | ||||
| Molecuulformule | (watervrij) (dihydraat) | |||
| IUPAC-naam | Natriumterhloroauraat(III) Natriumterhloroauraat(III)dihydraat | |||
| Andere namen | Natrium-goudchloride Geel goudchloride | |||
| Molmassa | (watervrij) 361,8 g/mol (dihydraat)[2] 397,8 g/mol | |||
| SMILES | [Na+].Cl[Au-](Cl)(Cl)Cl
| |||
| CAS-nummer | 15189-51-2 (watervrij) 13874-02-7 (dihydraat) | |||
| EG-nummer | 628-726-9 | |||
| PubChem | 27127 | |||
| Wikidata | Q27122658 | |||
| Beschrijving | Oranje poeder (watervrij) Geel, kristallijn poeder[2] | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H302 - H314 - H317 - H318 - H412 | |||
| P-zinnen | P260 - P261 - P264 - P270 - P272 - P273 - P280 - P301+P312 - P301+P330+P331 - P302+P352 - P303+P361+P353 - P304+P340 - P305+P351+P338} - P310 - P321 - P330 - P333+P313 - P363 - P405 - P501 | |||
| EG-Index-nummer | 239-241-3 | |||
| LD50 (muizen) | 72 mg/kg | |||
| Fysische eigenschappen | ||||
| Dichtheid | [3] 3,81 g/cm³ | |||
| Smeltpunt | [2] 99-101 °C | |||
| Goed oplosbaar in | Water, ethanol[2] | |||
| Matig oplosbaar in | diethylether[4] | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Natriumtetrachloorauraat(III) is een anorganische verbinding, een zout van natrium en het complexe -anion
Synthese[bewerken | brontekst bewerken]
De eerste synthese-route bestond uit het toevoegen van een oplossing van tetrachloorauraat(III)zuur aan natriumhydroxide of natriumcarbonaat. Het ontstane mengsel wordt verwarmd tot 100 °C en dan onder roeren ingedampt. Voordat al het water verdampt is wordt de oplossing gekoeld waarbij het product uitkristalliseert. Na drogen heeft men de oranje kristallijne stof in handen.[4][5]
Tegenwoordig wordt een efficientere methode gebruikt waarbij goud wordt toegevoegd aan een mengsel van een natrium-oxy-halogeenzout en waterstofchloride.[5]
Toepassingen[bewerken | brontekst bewerken]
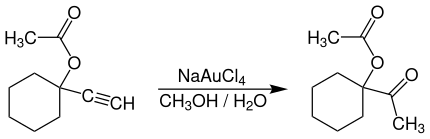
Na(AuCl4) is een niet-toxisch alternatief voor kwik als katalysator voor reacties met alkynen, bijvoorbeeld voor de aanmaak van geneesmiddelen. Voorbeeldreacties zijn de additie van waterstofchloride aan acetyleen, de oxidatie van sulfides[4] of de hydratie van terminale alkynen om methyl-ketonen te vormen:[6]
Na(AuCl4) is uitgangsstof voor andere goudverbindingen en complexen, zoals .[7]
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Sodium tetrachloroaurate op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- Verwijzingen in de tekst
- ↑ Tenzij anders aangegeven is de informatie op deze pagina afkomstig van gegevens in PubChem van Natriumtetrachloorauraat(III)
- ↑ a b c d HSP NaAuCl4.2H2O.
- ↑ Jones, P. G., Hohbein, R., Schwarzmann, E. (15 juli 1988). Anhydrous sodium tetrachloroaurate(III). Acta Crystallographica Section C Crystal Structure Communications 44 (7): 1164–1166 (International Union of Crystallography (IUCr)). ISSN: 0108-2701. DOI: 10.1107/s0108270188002756.
- ↑ a b c Stephen A. Westcott. (2001). Encyclopedia of Reagents for Organic Synthesis. , hoofdstuk Sodium Tetrachloroaurate(III) – American Cancer Society ISBN 9780470842898 DOI:10.1002/047084289x.rs108
- ↑ a b 20180208476, LU ; Wang ; Fan ; Wang: Method of Making Inorganic Gold Compoundinternet
- ↑ Y. Fukuda, K. Utimoto. (1991). Effective transformation of unactivated alkynes into ketones or acetals with a gold(III) catalyst J. Org. Chem.. 56 (11): 3729 DOI:10.1021/jo00011a058 , geraadpleegd op 28-1-2022
- ↑ Douglas E. Berning, Kattesh V. Katti, Charles L. Barnes, Wynn A. Volkert, Alan R. Ketring. (1997). Chemistry in Environmentally Benign Media. 7.(1) Chelating Hydroxymethyl-Functionalized Bisphosphines as Building Blocks to Water-Soluble and in-Vitro-Stable Gold(I) Complexes. Synthesis, Characterization, and X-ray Crystal Structures of [Au{(HOH(2)C)(2)PC(6)H(4)P(CH(2)OH)(2)}(2)]Cl and [Au(2){(HOH(2)C)(2)PCH(2)CH(2)P(CH(2)OH)(2)}(2)]Cl(2) Inorganic chemistry. 36 (11): 2765–2769 DOI:10.1021/ic961396b. PubMed: Chemistry in Environmentally Benign Media. , geraadpleegd op 28-1-2022








![{\displaystyle {\ce {[Au\{(HOH2C)2PC6H4P(CH2OH)2\}2]Cl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3bee1c36ab87651106dbd943229d2ae35d720e26)