Structuurisomeer
Structuurisomeren zijn isomere stoffen. Structuurisomeren komen met elkaar overeen doordat zij hetzelfde aantal en dezelfde soort atomen bevatten, maar verschillen van elkaar door de wijze waarop die atomen onderling zijn verbonden. Structuurisomeren hebben vaak grote gelijkenis qua chemische eigenschappen en zijn daardoor vaak moeilijk van elkaar te (onder)scheiden.
Voorbeelden:
- n-butaan en iso-butaan (beide C4H10)
- ethanol en dimethylether (beide C2H6O)
- α-, β- en γ-picoline (alle C6H7N)
Skeletisomerie[bewerken | brontekst bewerken]
Bij skeletisomerie of ketenisomerie worden de koolstofatomen uit een koolstofketen anders gebonden, zonder het aantal te wijzigen. Een voorbeeld is pentaan, waarvan 3 skeletisomeren bestaan: n-pentaan, 2-methylbutaan en 2,2-dimethylpropaan.
| Skeletisomeren van pentaan | ||
|---|---|---|

|

| |
| n-pentaan | 2-methylbutaan | 2,2-dimethylpropaan |
Positie-isomerie[bewerken | brontekst bewerken]
Positie-isomeren ontstaan door substituenten of functionele groepen op een andere plaats in een koolstofketen te plaatsen. Een voorbeeld vormt pentanol, die 3 positie-isomeren kent. De hydroxylgroep wordt immers telkens op een ander koolstofatoom geplaatst.
| Positie-isomeren van pentanol | ||
|---|---|---|

|

| |
| pentan-1-ol | pentan-2-ol | pentan-3-ol |
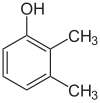
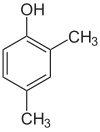
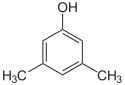
Een grotere verscheidenheid aan positie-isomeren is te vinden bij gesubstitueerde benzeenringen of andere aromatische verbindingen. Hieronder wordt xylenol aangehaald, waarvan 6 positie-isomeren bestaan.
| Positie-isomeren van xylenol | ||
|---|---|---|
|
|

|
| xylen-2,3-ol | xylen-2,4-ol | xylen-2,5-ol |

|

|
|
| xylen-2,6-ol | xylen-3,4-ol | xylen-3,5-ol |
Metamerie[bewerken | brontekst bewerken]
Metamerie ontstaat door een ongelijke verdeling van koolstofatomen aan beide zijden van een functionele groep, die is opgenomen in de koolstofketen zelf. Dit kan ontstaan bij bijvoorbeeld ethers, amines, esters, sulfonen en amiden.
| Metamerie | ||
|---|---|---|
| methyl-n-propylether | di-ethylether | |
Andere voorbeelden zijn chinoline en isochinoline of benzofuraan en isobenzofuraan.
