Butaan
| Butaan | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
Structuurformule van butaan
| ||||
| ||||
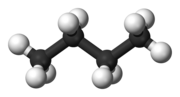
Molecuulmodel van butaan
| ||||
| Algemeen | ||||
| Molecuulformule | C4H10 | |||
| IUPAC-naam | butaan | |||
| Andere namen | butagas, n-butaan | |||
| Molmassa | 58,12 g/mol | |||
| SMILES | CCCC
| |||
| CAS-nummer | 106-97-8 | |||
| EG-nummer | 203-448-7 | |||
| PubChem | 7843 | |||
| Wikidata | Q134192 | |||
| Beschrijving | Brandbaar gas | |||
| Vergelijkbaar met | propaan | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H220 - H280 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P210 - P410+P403 | |||
| Opslag | Verwijderd houden van warmte en ontstekingsbronnen, fles niet langdurig blootstellen aan zonlicht. | |||
| EG-Index-nummer | 601-004-00-0 | |||
| MAC-waarde | 2400 mg/m³ | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | gasvormig | |||
| Kleur | kleurloos | |||
| Dichtheid | 0,59 (bij 15°C - vloeibaar)[1] en 0,00248 (bij 15°C - gas) g/cm³ | |||
| Smeltpunt | −138,35 °C | |||
| Kookpunt | −0,5 °C | |||
| Vlampunt | −60 °C | |||
| Zelfontbrandings- temperatuur | 287 °C | |||
| Oplosbaarheid in water | 0,061 g/L | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Butaan (C4H10) is een koolwaterstof uit de groep alkanen.
Bij kamertemperatuur is butaan een brandbaar gas dat als brandstof gebruikt wordt. Ook in de chemische industrie heeft het tal van toepassingen. Het wordt gewonnen uit de raffinage van aardolie en aardgas.
Isomeren[bewerken | brontekst bewerken]
Er bestaan twee verschillende isomere moleculen van butaan. De koolstofketens van de twee soorten butaanmoleculen verschillen daarbij in de mate van vertakking:
- onvertakt, vier koolstofatomen op een rij: n-butaan, orthobutaan of gewoon butaan.
- vertakt: isobutaan of methylpropaan.
Etymologie[bewerken | brontekst bewerken]
Het prefix but- is afgeleid uit het Latijnse butyrum, dat boter betekent. Boterzuur is de gebruikelijke naam voor butaanzuur. Zouten en esters van boterzuur heten butyraten.
Zwaarder dan lucht[bewerken | brontekst bewerken]
De relatieve dichtheid van butaan ten opzichte van lucht bedraagt circa 2,09. Butaan is dus iets meer als twee keer zo zwaar als lucht. Doordat butaan zwaarder is dan lucht kan het zich, bij onvoldoende ventilatie, laag bij de grond ophopen met mogelijk gevaarlijke situaties als gevolg. Uit veiligheidsoogpunt moet daarom worden voorzien in onderventilatie bij opslag en gebruik van butaan.
Toepassingen[bewerken | brontekst bewerken]

Butaan in gasflessen wordt in België - naast propaan - gebruikt op plaatsen waar geen aardgas beschikbaar is (voornamelijk om eten te bereiden). In Nederland worden gasflessen voornamelijk gevuld met propaan. Ook wordt butaan gebruikt als gas in aanstekers, hiervoor wordt het ook als navulling in bussen verkocht.
Het kookpunt van −0,5 °C is soms een probleem: butaan is bij omgevingstemperaturen beneden deze waarde vloeibaar en dus niet direct bruikbaar. Bij lage temperaturen is propaan daarom beter geschikt voor verwarming en om te koken.
Mengsels van butaan en propaan worden onder de naam lpg gebruikt als brandstof voor voertuigen. Bij kamperen wordt dit gas gebruikt om op te koken en dergelijke. Ook de gaspatronen voor hobbybranders zijn er mee gevuld. Bedrijfsmatig worden gasflessen met butaan en propaan gebruikt door onder meer dakdekkers en loodgieters. Mengsels in gezuiverde vorm worden gebruikt als drijfgas in spuitbussen.
Gezondheid[bewerken | brontekst bewerken]
Butaangas zoals dat voorkomt gemengd met propaangas in onder andere aanstekers, kan als dat wordt geïnhaleerd ernstige hartritmestoornissen veroorzaken. Iemand kan daaraan zelfs overlijden. Dit wordt aangeduid met het ”sudden sniffing death syndrome”.[2] Gebruik van drijfgassen om ze te snuiven kan bovendien tot leverschade leiden. Door het inhaleren van aanstekergas overleed in maart 2017 een 13-jarige Nederlandse jongen en een maand eerder een 19-jarige Belgische vrouw.[3] In 2010 raakte een 15-jarige jongen in coma.[4]
Externe links[bewerken | brontekst bewerken]
 butaan - International Chemical Safety Card
butaan - International Chemical Safety Card- (en) Gegevens van butaan in de GESTIS-stoffendatabank van het IFA
Bronnen, noten en/of referenties
|


