Lewistheorie
| Chemische binding |
|---|
| Dipool-dipoolinteracties
|
| Moleculen (intramoleculair)
Moleculen (intermoleculair) Zouten Metalen Covalente netwerken Theorieën Eigenschappen |
| Portaal |
De lewistheorie is een van de oudste theorieën over chemische binding. Al in 1902 had Gilbert Newton Lewis, samen met veel Europese chemici, opgemerkt dat de stabiliteit van edelgassen zou kunnen samenhangen met het bezit van 8 elektronen in de buitenste sfeer van Thomsons (krentenbol)atoommodel.[1] In 1916 publiceerde hij een lang artikel. In dit artikel nam hij enige postulaten op waarin onder andere is beschreven dat een neutraal atoom bestaat uit een atoomromp en een aantal elektronen in een buitenste schil. De atoomromp blijft ongewijzigd bij chemische veranderingen; het aantal elektronen in die buitenste schil is gelijk aan de positieve lading van de atoomromp en ligt tussen 0 en 8. De elektronen in de buitenste schil zijn later valentie-elektronen genoemd. Een atoom of ion heeft de edelgasconfiguratie als het 8 valentie-elektronen heeft. In datzelfde artikel definieerde Lewis de essentie van de covalente binding, de binding die verantwoordelijk is voor de vorming van moleculen door atomen:
- een covalente binding is een tweetal elektronen dat gemeenschappelijk bezit is van twee atomen.[2][3]
In de meeste gevallen draagt elk atoom één elektron bij aan dat tweetal gemeenschappelijke elektronen. In sommige gevallen echter levert één atoom beide elektronen. Dat tweetal elektronen heet nu “elektronenpaar”. In beide situaties bevindt het gemeenschappelijk elektronenpaar zich tussen beide atomen. Omdat dat elektronenpaar beide atoomkernen aantrekt worden volgens Lewis ook beide atomen naar elkaar toe getrokken. Lewis opperde verder het idee dat het aantal gemeenschappelijke elektronen tussen atomen samenhangt met het bereiken van de edelgasconfiguratie.
Dankzij deze theorie kan de meest waarschijnlijke elektronenstructuur van vele chemische stoffen op vrij eenvoudige manier gevonden worden. In combinatie met de VSEPR-theorie is het vaak ook mogelijk de driedimensionale vorm van het molecuul of samengesteld ion te voorspellen en in vele gevallen ook om een uitspraak te doen over het soort reacties dat het molecuul of ion kan ondergaan.
Criteria[bewerken | brontekst bewerken]
De theorie gaat ervan uit dat de stabielste elektronenstructuur voldoet aan de volgende criteria:
- paring: alle elektronen zijn gepaard.
- octetregel: alle atomen streven een edelgasconfiguratie na, dat wil zeggen een duet (2) voor H of een octet (8) voor andere atomen, eventueel door valentie-elektronenparen te delen met een buuratoom.
- lokalisatie: valentie-elektronenparen zijn ofwel eenzame elektronenparen ofwel gedeelde paren die een binding vormen tussen de atomen waartussen zij gedeeld zijn. (Valentie-elektronen zijn dus gelokaliseerd op één of tussen twee atomen.)
- ladingsminimalisatie: de stabielste structuur heeft een minimum aan formele ladingen op alle atomen. Indien het minimum niet nul is, horen tegengestelde formele ladingen elkaars buren te zijn en de negatieve ladingen op de meest elektronegatieve atomen te resideren.
De theorie doet geen poging om te zeggen waarom' het voldoen aan deze criteria juist tot de meest stabiele structuur zou moeten leiden. De ervaring leert echter dat met name de ruimtelijke structuur van veel moleculen en samengestelde ionen de Lewistheorie ondersteunt, (zie ook de eerder vermelde VSEPR-theorie). Echter, in veel gevallen is de theorie niet voldoende.
Een lewisstructuur is een elektronenstructuur volgens de lewistheorie. De term wordt ook gebruikt voor een diagram op basis van deze theorie.
Structuur[bewerken | brontekst bewerken]
De criteria maken het mogelijk met een eenvoudige berekening te voorspellen wat de valentie-elektronenstructuur van een molecuul of ion kan zijn.
- Bepaal de VE, de vereiste valentie-elektronen, dat wil zeggen het aantal atomen maal 8. (Behalve voor H, vermenigvuldig dat aantal met 2.)
- Sommeer de BE, de beschikbare valentie-elektronen van alle atomen in het molecuul; tel daar 1 bij voor iedere negatieve lading (in een anion) en haal daar 1 af voor iedere positieve lading in een kation;
- Deel BE door 2. Dit geeft het totaal aantal valentie-elektronenparen TP.
- Bereken het verschil tussen VE en BE. Dit geeft het aantal valentie-elektronen dat gedeeld moet worden in bindingen om alle atomen hun edelgasconfiguratie te geven. De helft van (VE-BE) geeft het aantal gedeelde paren GP ofwel bindingen.
- TP minus GP geeft het aantal eenzame valentie-elektronenparen EP.
- Gebruik een valentie-elektronenpaar om een binding te vormen tussen elk paar gebonden atomen;
- Verdeel de overgebleven valentie-elektronenparen over de atomen, dusdanig dat alle atomen de edelgasconfiguratie krijgen en de formele ladingen minimaal zijn.
Elektronen tellen[bewerken | brontekst bewerken]
Er zijn drie verschillende manieren van boekhouding wat betreft de valentie-elektronen die bij een bepaald atoom gerekend worden. Eenzame paren worden altijd geheel aan het atoom toegekend waaraan zij gehecht zijn. De manier waarop gedeelde paren behandeld worden verschilt echter.
Octet-telling[bewerken | brontekst bewerken]
Bij het bepalen van de octetregel worden alle valentie-elektronen rond een atoom daartoe gerekend, ook als zij gedeeld zijn met een buuratoom. Gedeelde paren worden dus dubbel geteld, eens bij het ene atoom en nog een keer bij het andere atoom.
Formele lading[bewerken | brontekst bewerken]
Voor het bepalen van de formele lading verloopt de boekhouding anders: alle gedeelde paren worden in tweeën gehakt en aan beide atomen wordt één elektron toegekend. Daarna wordt er vergeleken met het aantal valentie-elektronen dat een neutraal atoom bijdraagt. Het verschil is de formele lading. Idealiter zijn alle formele ladingen nul, maar bij sommige moleculen is er geen Lewisstuctuur te bedenken waar dat het geval is.
De formele lading bepaalt -vanwege de aanname van ladingsminimalisatie- mede welke elektronenstructuur geacht moet worden de meest stabiele te zijn.
Oxidatiegetal[bewerken | brontekst bewerken]
Voor het bepalen van de formele oxidatietoestand van een atoom kijkt men naar de elektronegativiteit van de twee atomen die een elektronenpaar delen en rekent de elektronen geheel tot het atoom dat het meest elektronegatief is. Bijvoorbeeld in CH4 worden alle 8 gedeelde elektronen bij koolstof gerekend omdat dit element net iets elektronegatiever is dan waterstof. Vervolgens wordt er dan vergeleken met de valentie-elektronen van het neutrale atoom (4 voor C). Het oxidatiegetal voor C is dus -4 in dit geval (en +1 voor de vier waterstofatomen). In CO2 behoren de gedeelde paren geheel bij de zuurstofatomen en heeft C een formeel oxidatiegetal van +4.
Indien een elektronenpaar gedeeld wordt door twee dezelfde atomen, bijvoorbeeld C-C of N-N worden zij wel in tweeën gehakt, omdat de elektronegativiteit dan gelijk is.
Het oxidatiegetal is niet van belang bij het bepalen van de meest waarschijnlijke elektronische structuur, maar het bepaalt wel aan wat voor redoxreacties het molecuul of ion kan deelnemen en hoeveel elektronen bij een eventueel redoxproces betrokken zijn.
Voorbeelden[bewerken | brontekst bewerken]

Water[bewerken | brontekst bewerken]
In water () bestaat elk molecuul uit twee waterstofatomen met elk één valentie-elektron, en een zuurstofatoom met zes valentie-elektronen; samen dus en het totaal aantal paren .
Het aantal elektronen vereist om edelgasconfiguratie te bereiken is .
Het verschil met het beschikbare aantal is . Er zijn dus gedeelde paren, ofwel bindingen en eenzame paren. Voor de binding tussen het zuurstofatoom en de beide waterstofatomen zijn twee elektronenparen nodig. Elk waterstofatoom heeft dan twee elektronen in zijn buitenste schil, dus een edelgasconfiguratie. Samen met de vier overgebleven elektronen bezetten de acht elektronen de buitenste schil bij het zuurstofatoom, dus ook een edelgasconfiguratie. De zo ontstane structuur staat rechts. Er is maar één mogelijkheid in dit geval. Elektronenparen worden in dit soort afbeeldingen als twee bolletjes (:) of als een streepje (-) weergegeven.
Formele lading[bewerken | brontekst bewerken]
Voor het bepalen van de formele lading worden de bindingen doorgeknipt en de valentie-elektronen rond de atomen geteld. Voor zuurstof is dat in dit geval 6 (2×2 voor de eenzame paren en 2×1 voor de doorgeknipte bindingen). Omdat zuurstof 6 valentie-elektronen inbrengt is de formele lading in dit geval nul. Op identieke wijze kan voor een waterstofatoom de formele lading nul worden afgeleid.
Oxidatiegetallen[bewerken | brontekst bewerken]
Omdat zuurstof elektronegatiever is dan waterstof worden alle 8 valentie-elektronen aan het zuurstofatoom toegekend, dat daarmee twee valentie-elektronen meer heeft dan een neutraal atoom. Het oxidatiegetal voor O is daarom -2. De waterstofatomen hebben in deze telling een elektron minder dan zij inbrengen en hun oxidatiegetal is dus +1.
Lachgas[bewerken | brontekst bewerken]

In lachgas is de situatie wat anders. De berekening gaat als volgt:
De 4+4 elektronenparen kunnen echter in dit geval op verschillende manieren verdeeld worden, zoals de afbeelding toont (zie Mesomerie). In het ene geval (N≡N-O) is er een drievoudige en een enkele binding (samen GP=4), in de andere (N=N=O) zijn er twee dubbele bindingen (ook GP=4).
Formele ladingen[bewerken | brontekst bewerken]
In beide gevallen zijn formele ladingen niet te vermijden, zoals aangegeven in de afbeelding. In dit geval is de structuur met een negatieve formele lading op zuurstof de stabielere structuur omdat zuurstof elektronegatiever is dan stikstof.
Er is een derde structuur mogelijk met een drievoudige binding naar zuurstof (N-N≡O). Deze zou echter een positieve formele lading zowel op zuurstof als op de stikstof ernaast bezitten en dit is zo ongunstig dat deze mogelijkheid niet in de afbeelding is opgenomen.
Oxidatiegetallen[bewerken | brontekst bewerken]
In de stabielste structuur N≡N-O heeft O een oxidatiegetal van −2 omdat de elektronen van het met het buuratoom gedeelde bindingspaar geheel aan het elektronegatievere zuurstofatoom toegekend worden. Omdat de twee stikstofatomen een gelijke elektronegativiteit hebben wordt de drievoudige binding gesplitst, zodat het centrale atoom nog drie elektronen bezit. Het heeft derhalve een formeel oxidatiegetal van +2. Het eindstandige stikstof atoom worden vijf elektronen toegekend, drie van de drievoudige binding en twee van zijn eenzaam elektronenpaar. Het heeft daarmee een oxidatiegetal van nul.
Op deze manier van bepaling van oxidatiegetallen verkrijgt men dus een waarde voor ieder atoom afzonderlijk: de twee stikstofatomen hebben een ander oxidatiegetal. Het is dus mogelijk dat een oxidatiegetal nul is, terwijl er geen sprake is van een niet-ontleedbare stof.
Uitzonderingen[bewerken | brontekst bewerken]
De Lewisaannames gaan op voor veel moleculen en moleculaire ionen, maar er zijn ook erg veel uitzonderingen:
- Moleculen waarin men meerdere correcte Lewisstructuren kan opstellen, die door spiegeling of rotatie in elkaar om te vormen zijn.
Ieder afzonderlijk komen deze niet overeen met de werkelijke eigenschappen van de stof. In deze gevallen spreek men dan van resonantie. De verschillende Lewisstructuren worden grensstructuur genoemd. Vaak geven deze grensstructuren aanwijzingen over de reactiviteit van de betrokken verbinding; in feite is dit verschijnsel een artefact van de aanname dat elektronen altijd maar door één of door twee atomen gedeeld kunnen worden. Sinds de komst van de golfmechanica is men gaan beseffen dat deze Lewisaanname niet juist is omdat elektronen ook golfeigenschappen bezitten en als zodanig best door veel meer atomen gedeeld kunnen worden
- Moleculen met een oneven aantal elektronen, zoals NO;
Alles paren is dan onmogelijk, toch is dit een stabiele -zij het reactieve- verbinding
- Moleculen zoals O2 waarvoor de Lewisstructuur alle valentie-elektronen gepaard voorspelt, maar die in werkelijkheid ongepaarde valentie-elektronen bezitten in hun stabielste toestand;
In dit geval voorspelt Lewis echt de verkeerde structuur: zuurstof met gepaarde valentie-elektronen heet singletzuurstof en is een uiterst agressieve vorm van zuurstof. De reden dat de paringsaanname hier niet opgaat is de regel van Hund, die zegt dat het paren van elektronen eigenlijk energie kost (niet: oplevert).
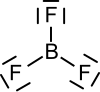
Een goed voorbeeld van een molecuul dat niet aan de Lewisaannames voldoet is BF3. Een structuur die aan de eerste drie criteria voldoet kan wel worden getekend maar alleen met één dubbele binding tussen het B-atoom en een F-atoom. Omdat hierbij dat F-atoom de formele lading +1 heeft en het B atoom de formele lading -1 is deze structuur in strijd met het 4e criterium.
- Moleculen waarin een atoom meer dan acht valentie-elektronen rond zich heeft.
Anderzijds zijn er moleculen als SF6 met een octaëdrische structuur waarin het centrale atoom niet vier maar zes bindingen met de omringende fluoratomen bezit. Rond zwavel moet men daarom zich niet een octet van 8 valentie-elektronen denken, maar wel 12 valentie-elektronen. Vooral voor wat zwaardere elementen (P,S,Se,As etc) is dit een veelgezien fenomeen. Er zijn wel pogingen gedaan de Lewistheorie 'uit te breiden' en men spreekt dan vaak van "hypervalente" moleculen en verbindingen, maar latere theorieën op basis van de golfmechanica hebben laten zien dat er weinig theoretische rechtvaardiging is voor dit soort uitbreidingsgedachten.
Voor de meeste elementen is de Lewistheorie namelijk gewoon ongeschikt en moet vervangen worden door kwantummechanische theorieën. Echter omdat het voor verbindingen van lichtere elementen, vooral koolstof meestal redelijk opgaat en gemakkelijk op een stukje papier valt uit te werken (in plaats van met een supercomputer) is de Lewistheorie nog altijd van onschatbare waarde voor de chemie en met name de organische chemie.
Externe link[bewerken | brontekst bewerken]
| Bronnen, noten en/of referenties
Bronnen
Referenties
|