Natriumamide
| Natriumamide | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
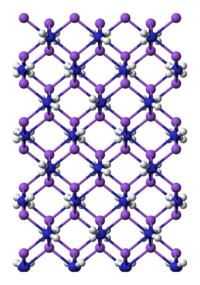
| ||||
Kristalstructuur van natriumamide
| ||||
| Algemeen | ||||
| Molecuulformule | NaNH2 | |||
| IUPAC-naam | natriumamide | |||
| Andere namen | natriumtrinitride | |||
| Molmassa | 39,01234928 g/mol | |||
| CAS-nummer | 7782-92-5 | |||
| Wikidata | Q188260 | |||
| Beschrijving | Grijs poeder | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H300 - H410 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P264 - P273 - P301+P310 - P501 | |||
| EG-Index-nummer | 011-004-00-7 | |||
| VN-nummer | 1687 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | grijs | |||
| Dichtheid | 1,39 g/cm³ | |||
| Smeltpunt | 210 °C | |||
| Kookpunt | 400 °C | |||
| Vlampunt | 4,44 °C | |||
| Zelfontbrandings- temperatuur | 450 °C | |||
| Evenwichtsconstante(n) | pKa = 38 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Natriumamide (NaNH2) is het natriumzout van ammoniak. De stof komt voor als een grijs poeder, maar is in zuivere toestand kleurloos. De grijze kleur is afkomstig van kleine metallische deeltjes uit het productieproces. Natriumamide reageert hevig met water.
Synthese[bewerken | brontekst bewerken]
Natriumamide wordt gesynthetiseerd uit een reactie van ammoniakgas en natrium,[1] alhoewel ze meestal bereid wordt uit vloeibare ammoniak, met ijzer(III)nitraat als katalysator. De reactie, die plaatsvindt bij een temperatuur van −33 °C (kokende ammoniak), verloopt als volgt:[2]
Toepassingen[bewerken | brontekst bewerken]
Natriumamide wordt in een aantal industriële productieprocessen aangewend, onder andere bij de productie van indigo, hydrazine en natriumcyanide. In de organische chemie wordt de stof gebruikt als sterke base, meestal in een oplossing van vloeibare ammoniak. Een van de voordelen van deze stof is dat het zelden nucleofiel reageert. Het is echter slecht oplosbaar, wegens de hevige reactie met water, en het gebruik van de stof wordt meestal vervangen door verwante verbinding, zoals natriumhydride, natriumbis(trimethylsilyl)amide en lithiumdi-isopropylamide.
Externe links[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|



