Waterstofjodaat
| Waterstofjodaat | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
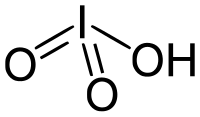
| ||||
Structuurformule van waterstofjodaat
| ||||

| ||||
Molecuulmodel van waterstofjodaat
| ||||
| Algemeen | ||||
| Molecuulformule | HIO3 | |||
| IUPAC-naam | waterstofjodaat | |||
| Molmassa | 175,91061 g/mol | |||
| SMILES | OI(=O)=O
| |||
| InChI | 1S/HIO3/c2-1(3)4/h(H,2,3,4)
| |||
| CAS-nummer | 7782-68-5 | |||
| EG-nummer | 231-962-1 | |||
| PubChem | 24345 | |||
| Wikidata | Q408822 | |||
| Beschrijving | Witte vaste stof | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H272 - H314 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P220 - P280 - P305+P351+P338 - P310 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit | |||
| Dichtheid | 4,62 g/cm³ | |||
| Smeltpunt | 110 °C | |||
| Oplosbaarheid in water | 2690 g/L | |||
| Goed oplosbaar in | water | |||
| Onoplosbaar in | ethanol, chloroform en di-ethylether | |||
| Evenwichtsconstante(n) | pKa = 0,75 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Waterstofjodaat of joodzuur is een sterk monoprotisch zuur van jood, met als brutoformule HIO3. Het behoort tot de groep der halogeenzuurstofzuren en is een sterke oxidator. De stof komt voor als een witte kristallijne vaste stof, in tegenstelling tot andere halogeenbevattende oxozuren (chloorzuur en broomzuur) die alleen in waterige oplossingen voorkomen. Waterstofjodaat is extreem goed oplosbaar in water. Zouten van waterstofjodaat worden jodaten genoemd.
Synthese[bewerken | brontekst bewerken]
Waterstofjodaat kan bereid worden uit een oxidatie van di-jood met een sterke oxidator (salpeterzuur, chloorgas, chloorzuur of waterstofperoxide) in een waterige oplossing.
Toepassingen[bewerken | brontekst bewerken]
Waterstofjodaat kent toepassingen als oxidator en zwak zuur in de analytische scheikunde. Het kan worden gebruikt om bepaalde zwak of sterk basische oplossingen te standaardiseren, met methylrood of methyloranje als pH-indicator.



