2-broombutaan
| 2-broombutaan | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
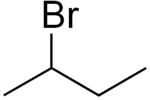
| ||||
Structuurformule van 2-broombutaan
| ||||
| Algemeen | ||||
| Molecuulformule | C4H9Br | |||
| IUPAC-naam | 2-broombutaan[1] | |||
| Andere namen | s-butylbromide, sec-butylbromide | |||
| Molmassa | 137,02 g/mol | |||
| CAS-nummer | 78-76-2 | |||
| EG-nummer | 201-140-7 | |||
| PubChem | 6554 | |||
| Wikidata | Q209314 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H225 - H412 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P210 - P262 - P273 - P403+P235 | |||
| VN-nummer | 2339 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,255 g/cm³ | |||
| Smeltpunt | −112,65 °C | |||
| Kookpunt | 91 °C | |||
| Vlampunt | 21 °C | |||
| Zelfontbrandings- temperatuur | 265[2] °C | |||
| Dampdruk | (bij 20°C) 7,33 × 103 Pa | |||
| log(Pow) | 2,672 | |||
| Brekingsindex | 1,437 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
2-broombutaan, ook bekend als sec-butylbromide, is een organische verbinding met als brutoformule C4H9Br. De vloeistof heeft een door veel mensen als prettig ervaren geur. 2-broombutaan is een chirale verbinding.
Met een sterke base ondergaat de stof een E2-eliminatie, waarbij vooral 2-buteen ontstaat.
Synthese
[bewerken | brontekst bewerken]2-broombutaan kan uit verschillende uitgangsstoffen, zoals isomere butenen (1-buteen, 2-buteen) of 2-butanol met behulp van waterstofbromide verkregen worden.[3]
Toepassingen
[bewerken | brontekst bewerken]2-broombutaan wordt in de farmaceutische- en de geurstoffenindustrie toegepast om de sec-butylgroep in te voeren.[2]
In de studie van reactiemechanismen is de reactie van 2-broombutaan met een jodide een schoolvoorbeeld van de SN2-reactie.
Toxicologie en veiligheid
[bewerken | brontekst bewerken]2-broombutaan is irriterend voor huid en ogen en schadelijk bij inslikken. Het is een giftige en brandbare vloeistof.
- ↑ . (26 maart 2005). 2-bromobutane - Compound Summary26 maart 2015 National Center for Biotechnology Information Internetpagina: 2-bromobutane - Compound Summary geraadpleegd op 26 maart 2015
- ↑ a b . Gestis-Stoffdatenbank16 maart 2015 Internetpagina: Gestis-Stoffdatenbank geraadpleegd op 16 maart 2015. Gearchiveerd op 5 januari 2019.
- ↑ Francis A. Carey; Organic Chemistry, ISBN 0-07-290501-8, S. 215, S. 275.

