Vinylacetyleen
| Vinylacetyleen | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuurformule van vinylacetyleen
| ||||
| Algemeen | ||||
| Molecuulformule | C4H4 | |||
| IUPAC-naam | but-1-en-3-yn | |||
| Andere namen | butenyn | |||
| Molmassa | 52,07456 g/mol | |||
| SMILES | C=CC#C
| |||
| InChI | 1S/C4H4/c1-3-4-2/h1,4H,2H2
| |||
| CAS-nummer | 689-97-4 | |||
| EG-nummer | 211-713-3 | |||
| PubChem | 12720 | |||
| Wikidata | Q422748 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | gasvormig | |||
| Kleur | kleurloos | |||
| Dichtheid | (bij 0°C) 0,71 g/cm³ | |||
| Smeltpunt | −92 °C | |||
| Kookpunt | 0–6 °C | |||
| Vlampunt | < −5 °C | |||
| Slecht oplosbaar in | water | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Vinylacetyleen of butenyn is een organische verbinding met als brutoformule C4H4. De stof komt voor als een kleurloos licht ontvlambaar gas, dat slecht oplosbaar is in water. Vinylacetyleen is het kleinst mogelijke eenyn, een groep meervoudig onverzadigde koolwaterstoffen met een dubbele en een drievoudige binding.
Synthese
[bewerken | brontekst bewerken]Vinylacetyleen werd voor het eerst bereid door middel van een Hofmann-eliminatie van het quaternair ammoniumzout 1,4-bis(trimethylammonium)but-2-eendijodide:[1]
Tegenwoordig wordt het bereid door dehydrohalogenering van 1,3-dichloor-2-buteen. Het kan ook ontstaan door dimerisatie van ethyn.
Toepassingen
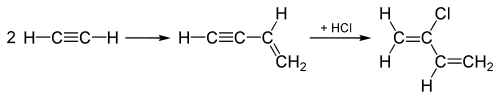
[bewerken | brontekst bewerken]Vinylacetyleen werd vroeger gebruikt in de polymeerindustrie, onder meer bij de productie van chloropreen. Chloropreen werd bereid door dimerisatie van 2 ethyn-moleculen en vervolgens additie van zoutzuur (HCl) met behulp van koper(I)chloride (CuCl):[2]
Externe links
[bewerken | brontekst bewerken]- (en) MSDS van vinylacetyleen
- (en) Gegevens van vinylacetyleen in de GESTIS-stoffendatabank van het IFA
- ↑ (de) R. Willstätter & T. Wirth (1913) - Über Vinyl-acetylen[dode link], Chemische Berichte, 46, p. 535
- ↑ (en) W.H. Carothers et al. (1933) - Acetylene Polymers and their Derivatives. II. A New Synthetic Rubber: Chloroprene and its Polymers, Journal of the American Chemical Society, 55 (2), pp. 789–795

![{\displaystyle \mathrm {C_{10}H_{24}N_{2}I_{2}\ \longrightarrow \ 2\ [NH(CH_{3})_{3}]I\ +\ C_{4}H_{4}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/7e14f4776a68f81693e763fe74c6bc50d3c21c80)