Broomcresolgroen
| Broomcresolgroen | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuurformule van broomcresolgroen
| ||||
| Algemeen | ||||
| Molecuulformule | C21H14Br4O5S | |||
| IUPAC-naam | 2,6-dibroom-4-[7-(3,5-dibroom-4-hydroxy-2-methylfenyl)-9,9-dioxo-8-oxa-9λ6-thiabicyclo[4.3.0]nona-1,3,5-trien-7-yl]-3-methylfenol | |||
| Andere namen | 3,3',5,5'-tetrabroom-m-cresolsulfonftaleïne, BCG | |||
| Molmassa | 698,02 (vrij zuur) g/mol | |||
| SMILES | Brc1cc(c(c(Br)c1O)C)C3(OS(=O)(=O)c2ccccc23)c4cc(Br)c(O)c(Br)c4C
| |||
| CAS-nummer | 76-60-8 | |||
| PubChem | 6451 | |||
| Wikidata | Q418613 | |||
| Evenwichtsconstante(n) | pKz = 4,8 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
| Broomcresolgroen (pH-indicator) | ||
| onder pH 3,8 | boven pH 5,4 | |
| 3,8 | 5,4 | |
Broomcresolgroen is een kleurstof uit de groep van de trifenylmethanen, de triarylmethaankleurstoffen. Een van de belangrijkste toepassingen van de stof vormt zijn gebruik als pH-indicator en als detectiereagens in de elektroforese van DNA. De stof wordt zowel als vrij zuur (licht bruine vaste stof) als in de vorm van het natriumzout (donkergroene vaste stof) toegepast. Broomcresolgroen heeft een negatief effect op het transporteiwit van prostaglandine E2
Na oplossen in water is de sulfonzuurgroep geïoniseerd en ontstaat het geelgekleurde mono-anion. Afstaan van een tweede proton bij hogere pH geeft het blauwgekleurde tweewaardige anion. In beide ionen speelt resonantie een belangrijke rol. In het eenwaardige ion gaat dit gepaard met ladingsscheiding, in het tweewaardige ion wordt de lading verdeeld tussen de twee zuurstofatomen:
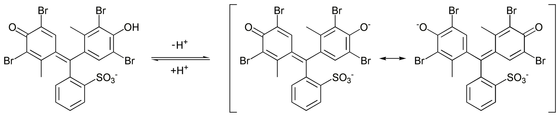
De pKz van broomcresolgroen is 4.8.[1]

De zure en de basische vorm van deze kleurstof / indicator hebben een isosbestisch punt rond 515 nm.
Een oplossing van 0,04% van broomcresolgroen in ethanol wordt toegepast als kleurreagens in de dunnelaagchromatografie voor het aantonen van verbindingen met een pKz kleiner dan 5.0 (zoals carbonzuren, sulfonzuren, enz.). In tegenstelling tot andere reagentia voor de detectie van verbindingen hoeft het chromatogram niet verwarmd te worden om de kleuring te laten ontstaan. De plek van verbindingen wordt aangegeven door gele vlekken op een blauwe achtergrond. Een broomfenolblauw-oplossing kan voor hetzelfde doel gebruikt worden.
Broomcresolgroen wordt gesynthetiseerd door het bromeren van Cresolpurper (m-cresolsulfonfthaleïne).
Bronnen, noten en/of referenties
|

