Energieniveau


Een energieniveau is de discrete energie die als een energetische eigentoestand bij een kwantummechanische toestand van een systeem (bijvoorbeeld een atoom of een atoomkern) hoort. Energieniveaus zijn toegestane eigenwaarden van de Hamiltonoperator en zijn daarom tijdsonafhankelijk. Het systeem kan zich continu slechts in één toestand bevinden, maar kan niet een van de daartussenin liggende energiewaarden hebben. Een aan zichzelf overgelaten systeem tracht er altijd zijn laagste energieniveau, zijn grondtoestand, te bereiken. Alle andere niveaus worden aangeslagen toestanden genoemd.
Om het aanschouwelijk te maken, kan men zich voorstellen dat de rangschikking en de bewegingen van de elektronen in de elektronenschil – of de nucleonen in de atoomkern – alleen bij bepaalde gevallen stabiel zijn. Elk van deze toestanden heeft een andere, vaste, energie-inhoud. Boven een bepaalde grensenergie is er echter ook een continuüm, een gebied waar willekeurige energiewaarden mogelijk zijn. Bij een atoom komt deze grensenergie overeen met de bindingsenergie van het betreffende elektron; het niet langer gebonden elektron (bijvoorbeeld bij ionisatie) kan daardoor een willekeurige kinetische energie hebben. In de atoomkern is de situatie gecompliceerder; hier bestaan er ook discrete energieniveaus boven de bindingsenergie van het nucleon. Deze niveaus leiden bijvoorbeeld tot resonanties in de werkzame doorsnede van kernreacties.
Overgangen tussen energieniveaus[bewerken | brontekst bewerken]
Het systeem kan alleen energie opnemen wanneer het naar een hoger energieniveau of naar het continuüm overgaat. Dat kan bijvoorbeeld door absorptie van een foton of door een niet-elastische botsing met een deeltje, zoals in de proef van Franck en Hertz. Bij overgangen tussen discrete niveaus moet daarbij altijd de passende energie worden toegevoerd. Dit proces heet excitatie of ook wel aanslaan. Dit leidt tot een discrete absorptielijn in het spectrum.
De omgekeerde overgang van een hoger naar een lager niveau, onder afgifte van een foton, vindt gewoonlijk plaats zonder uitwendige beïnvloeding als spontane emissie en wordt gekarakteriseerd door een bepaalde halveringstijd. Hij veroorzaakt discrete emissie-spectraallijnen (bij atomen - vaak - zichtbaar licht, bij kernen gammastraling). In bepaalde gevallen kan ook niet-spontane emissie optreden. Men spreekt dan van gestimuleerde emissie, het verschijnsel waarop de laser is gebaseerd.
Energieniveaus in het atoom[bewerken | brontekst bewerken]
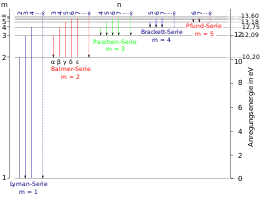
Energieniveaus in atomen worden beschreven door het hoofdkwantumgetal . De energie van de toestand met kwantumgetal in een atoom met atoomnummer is bij benadering:
waarin de Rydberg-energie eV, wat echter alleen voor waterstofachtige systemen (atomen met één elektron, zoals H, He+, enz.) geldt.
Daar komen dan nog de fijnstructuur- en de hyperfijnstructuur-correcties en de Lamb-verschuiving bij.




