Cresol
| Cresol | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||

| |||||
De verschillende structuurformules van cresol
| |||||
| Algemeen | |||||
| Molecuulformule | C7H8O | ||||
| IUPAC-naam | methylfenol | ||||
| Andere namen | hydroxytolueen | ||||
| Molmassa | 108,14 g/mol | ||||
| SMILES | OC(CCC(O)=O)=O
| ||||
| CAS-nummer | 1319-77-3 | ||||
| EG-nummer | 215-293-2 | ||||
| Wikidata | Q413524 | ||||
| Beschrijving | Viskeuze vloeistof | ||||
| Vergelijkbaar met | Fenol | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H301 - H311 - H314 - H331 - H341 | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P261 - P280 - P301+P310 - P305+P351+P338 - P310 | ||||
| LD50 (ratten) | 1454 mg/kg | ||||
| Fysische eigenschappen | |||||
| Kleur | wit | ||||
| Dichtheid | 1,04 g/cm³ | ||||
| Vlampunt | 82 °C | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Met cresol worden 3 verschillende isomeren bedoeld, waarbij een methylgroep en een hydroxylgroep op een benzeenring gesubstitueerd staan. De methylgroep kan op 3 verschillende plaatsen ten opzichte van de hydroxylgroep op de ring zijn gesubstitueerd. Elk isomeer wordt aangeduid door middel van de klassieke ortho-, meta- en para-nomenclatuur of gewoon door nummering van het koolstofatoom in de arylgroep.
Verder bestaat er een zeer grote groep stoffen die in valt te delen als de groep van de cresolen. Al deze organische stoffen hebben gemeen dat ze ten minste één methylgroep en een hydroxylgroep op dezelfde aromatische ring als substituent hebben. Een bekend voorbeeld is de stof broomcresolgroen, een triarylmethaankleurstof.
Cresol van technische kwaliteit zoals dat in de handel verkrijgbaar kan zijn, bestaat bij benadering uit een isomerenmengsel van de volgende componenten:
- Metacresol: 40-45 %
- Paracresol: 29-34 %
- Orthocresol: 10 %
- Fenol: 6 %
Ook zijn de drie isomeren in hun zuivere vorm verkrijgbaar, meestal als laboratoriumreagens.
Cresolen als reagens in het organisch laboratorium[bewerken | brontekst bewerken]
Cresolen kunnen een heel scala aan reacties ondergaan, de ring is over het algemeen geactiveerd. De plaats van substitutie aan de arylgroep hangt wel af van het soort cresolisomeer, al naargelang eventuele sterische hinder of hinder door mesomere effecten. Ook kan de fenolische groep veresterd worden met behulp van een zuuranhydride. Partiële oxidatie van de methylgroep is mogelijk, hierbij ontstaan de corresponderende benzylalcoholen, aldehyden of carbonzuren.
Voorkomen in de natuur[bewerken | brontekst bewerken]
Cresolen en derivaten van cresolen komen in de natuur veelvuldig voor. Zo zijn ze gevonden als metaboliet in verschillende micro-organismen als wel in urine. Bovendien komen cresolen voor in steenkool en onder andere teren, hier werden zij vroeger dan ook uit gewonnen.
Eigenschappen van isomeren[bewerken | brontekst bewerken]
| Isomeren van Cresol[1][2][3][4] | ||||||
|---|---|---|---|---|---|---|
| Structuurformule | 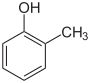 |
 |
||||
| Ball-and-stick model | 
|

|
| |||
| General | ||||||
| Triviale naam | o-cresol | m-cresol | p-cresol | |||
| IUPACnaam | 2-methylfenol | 3-methylfenol | 4-methylfenol | |||
| Systematische naam | 2-methylbenzenol | 3-methylbenzenol | 4-methylbenzenol | |||
| Andere namen | ortho-Cresol 2-Hydroxytolueen |
meta-Cresol 3-Hydroxytolueen |
para-Cresol 4-Hydroxytolueen | |||
| Formule | ||||||
| SMILES | Oc1c(C)cccc1 | Oc1cc(C)ccc1 | Oc1ccc(C)cc1 | |||
| Molaire massa | 108.14 g/mol | |||||
| Beschrijving (kamertemperatuur en druk) | Kleuloze kristallen | Dikvloeibare olie | vettig ogende vaste stof | |||
| CAS number | [95-48-7] | [108-39-4] | [106-44-5] | |||
| mengsel van cresolen (tricresol): [1319-77-3] | ||||||
| Eigenschappen | ||||||
| Dichtheid en fase | 1.05 g/cm3, vaste stof | 1.03 g/cm3, vloeistof | 1.02 g/cm3, vloeistof | |||
| Oplosbaarheid in water (pH = 7.0, 20−25 °C) |
25 g/L | 24 g/L | 19 g/L | |||
| Goed oplosbaar in sterk alkalisch water | ||||||
| Smeltpunt | 29.8 °C (303.0 K) | 11.8 °C (285.0 K) | 35.5 °C (309.7 K) | |||
| Kookpunt | 191.0 °C (464.2 K) | 202.0 °C (475.2 K) | 201.9 °C (475.1 K) | |||
| Zuursterkte (pKz) | 10.287 | 10.09 | 10.26 | |||
| Structuur | ||||||
| Dipoolmoment | 1.35 D | 1.61 D | 1.58 D | |||
| Veiligheid | ||||||
| SDS | ||||||
| Algemene risico's | Brandbaar, toxisch bij inslikken en inademen | |||||
| Vlampunt | 81 °C c.c. | 86 °C | 86 °C c.c. | |||
| GHS-pictogrammen |
| |||||
Externe links[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|





