Di-ethylaminozwaveltrifluoride
| Di-ethylaminozwaveltrifluoride | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||
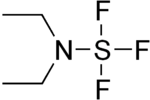
| |||||
Structuurformule van di-ethylaminozwaveltrifluoride
| |||||
| Algemeen | |||||
| Molecuulformule | C4H10F3NS | ||||
| IUPAC-naam | N,N-di-ethylamino-zwaveltrifluoride | ||||
| Andere namen | DAST | ||||
| Molmassa | 161,18911 g/mol | ||||
| SMILES | CCN(CC)S(F)(F)F
| ||||
| InChI | 1S/C4H10F3NS/c1-3-8(4-2)9(5,6)7/h3-4H2,1-2H3
| ||||
| CAS-nummer | 38078-09-0 | ||||
| EG-nummer | 253-771-2 | ||||
| PubChem | 123472 | ||||
| Wikidata | Q412982 | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H226 - H302 - H312 - H314 - H332 | ||||
| EUH-zinnen | EUH014 | ||||
| P-zinnen | P280 - P305+P351+P338 - P310 | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | vloeibaar | ||||
| Kleur | kleurloos | ||||
| Dichtheid | 1,22 g/cm³ | ||||
| Goed oplosbaar in | dichloormethaan | ||||
| Matig oplosbaar in | acetonitril | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Di-ethylaminozwaveltrifluoride (afgekort tot DAST) is een organische verbinding met als brutoformule C4H10F3NS. In zuivere toestand is het een kleurloze olieachtige vloeistof, die reageert met water. Di-ethylaminozwaveltrifluoride wordt voornamelijk gebruikt in de organische synthese als fluoreringsreagens.
Synthese[bewerken | brontekst bewerken]
Di-ethylaminozwaveltrifluoride kan bereid worden door de reactie van di-ethylaminotrimethylsilaan met zwaveltetrafluoride bij −60 °C:[1]
De drijvende kracht voor deze reactie berust op de vorming van een zeer sterke binding tussen silicium en fluor. De reactie moet uitgevoerd worden in inerte kunststoffen recipiënten, aangezien tijdens de bereiding normaal glaswerk kan aangetast worden door fluor. Meestal wordt de stof echter aangekocht, omdat aan de bereidingsprocedure ook enkele veiligheidsrisico's verbonden zijn: zwaveltetrafluoride is onder standaardomstandigheden immers een giftig gas.
Eigenschappen en reacties[bewerken | brontekst bewerken]
Aangezien di-ethylaminozwaveltrifluoride een vloeistof is en dus relatief makkelijk hanteerbaar, wordt dit reagens vaak gebruikt voor fluoreringen in plaats van het gasvormige zwaveltetrafluoride. Di-ethylaminozwaveltrifluoride zet alcoholen en thio-ethers om tot de corresponderende organofluoriden. Aldehyden en ketonen worden omgezet in geminale difluoriden. Met carbonzuren worden de overeenkomstige acylfluoriden gevormd.
Daarnaast kan de stof dienen als katalysator bij Friedel-Crafts-allyleringen.
Toxicologie en veiligheid[bewerken | brontekst bewerken]
Di-ethylaminozwaveltrifluoride is een vluchtige organische verbinding, die aanleiding geeft tot corrosieve en ontvlambare dampen. Het werkt corrosief op de huid, de ogen en luchtwegen. Bij contact met water, bij verhitting boven 90 °C en bij destillatie kan het explosief ontleden.[2] Di-ethylaminozwaveltrifluoride wordt daarom bij lage temperatuur opgeslagen.
- ↑ (en) W.J. Middleton & E.M. Bingham (1977) – Diethylaminosulfur Trifluoride, Organic Syntheses, 57, p. 50
- ↑ (en) P.G. Urben (2007) – Bretherick's handbook of reactive chemical hazards, volume 1, Elsevier, p. 641 – ISBN 978-0-12-373945-2




