Fluoresceïne
| Fluoresceïne | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuurformule van fluoresceïne
| ||||

| ||||
Fluoresceïnepoeder
| ||||

| ||||
Fluoresceïne onder UV-licht
| ||||

| ||||
| Uranine is een krachtige groene kleurstof | ||||
| Algemeen | ||||
| Molecuulformule | C20H12O5 | |||
| IUPAC-naam | 6-hydroxy-9-(2-carboxyfenyl)- (3H)-xanthen-3-on | |||
| Andere namen | 2-(6-hydroxy-3-oxo-(3H)-xanthen-9-yl)benzoëzuur, C.I. 45350 | |||
| Molmassa | 332,31 g/mol | |||
| SMILES | c1ccc2c(c1)C(=O)OC23c4ccc(cc4Oc5c3ccc(c5)O)O
| |||
| InChI | 1S/C20H12O5/c21-11-5-7-15-17(9-11)24-18-10-12(22)6-8-16(18)20(15)14-4-2-1-3-13(14)19(23)25-20/h1-10,21-22H
| |||
| CAS-nummer | 2321-07-5 | |||
| EG-nummer | 219-031-8 | |||
| PubChem | 16850 | |||
| Wikidata | Q410922 | |||
| Beschrijving | Rode kristallen | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H319 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P305+P351+P338 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | rood | |||
| Smeltpunt | (ontleedt) 314-216 °C | |||
| Onoplosbaar in | water | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Fluoresceïne is een synthetische organische fluorescerende kleurstof. Het behoort tot de groep der xanthenen. De zuivere stof komt voor als een donkerrood poeder, dat vrijwel onoplosbaar is in water. Het is een zwak organisch zuur, dat met een base gemakkelijk een goed oplosbaar zout vormt. Het dinatriumzout van fluoresceïne wordt uranine genoemd.
Synthese[bewerken | brontekst bewerken]
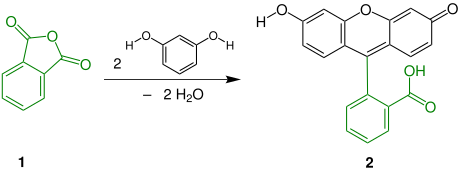
Fluoresceïne (2) wordt bereid door de condensatiereactie van gesmolten ftaalzuuranhydride (1) met twee equivalenten resorcinol. Als katalysator die de afsplitsing van water bevordert kan geconcentreerd zwavelzuur of watervrij zinkchloride gebruikt worden

De reactie, met zwavelzuur als katalysator, werd voor het eerst in 1871 beschreven door Adolf von Baeyer.[1]
Eigenschappen[bewerken | brontekst bewerken]
Fluoresceïne is een fluorofoor. Het absorbeert blauw licht met absorptiemaxima bij 493,5 en 460 nm en emitteert geel-groen licht met een golflengte van 515 nm. De fluorescentie is evenwel sterk afhankelijk van de pH: het maximum ligt bij pH 9.
Het wateroplosbare uranine (met hetzelfde color index-nummer, 45350, als fluoresceïne) is in water een sterke gele, onder UV- en daglicht groen fluorescerende kleurstof. Uranine absorbeert licht van 475-490 nm en emitteert licht met een golflengte van 510-520 nm. De fluorescentie piekt bij een pH van 7,4.[2]
Toepassingen[bewerken | brontekst bewerken]
Fluoresceïne wordt als kleurstof gebruikt in de celbiologie. In de analytische scheikunde kan het worden gebruikt als pH-indicator. Boven een pH van ongeveer 4 verandert een oplossing ervan van kleurloos naar groen fluorescerend.
Paul Ehrlich gebruikte uranine in 1881 om de stroming van oogkamervocht te onderzoeken.[3] Dit zou de eerste toepassing geweest zijn van fluorescerende kleurstoffen in in vivo medisch onderzoek en illustreert eveneens dat deze verbinding niet schadelijk is. Uranine wordt gebruikt in de fluoresceïneangiografie om de bloedvaten aan de achterkant van het oog te onderzoeken. De stof wordt in de hydrologie en geohydrologie gebruikt als tracer om de stroming van rivieren, lozingen in water of het verloop van ondergrondse waterstromingen te bestuderen. Dit werd reeds in 1877 voor het eerst toegepast op de bovenloop van de Donau, waar het water onder de grond verdwijnt en enkele kilometers verder in een nieuwe "bron" aan de oppervlakte komt.[4] Uranine is ook verantwoordelijk voor de groene fluorescentie van antivries voor voertuigen. Ze kan worden gebruikt bij schipbreuken of noodlandingen op water: een kleine hoeveelheid ervan kan een groot wateroppervlak opvallend groen kleuren en zo de aandacht trekken op de plaats van het ongeval.[5]
Fluoresceïne mag aangewend worden voor het denatureren van ethanol (alcohol).
Door jodering van fluoresceïne wordt de rode kleurstof erythrosine (tetrajoodfluoresceïne) bekomen. Met de bromering van fluoresceïne verkrijgt men eosine Y (tetrabromofluoresceïne).
Externe links[bewerken | brontekst bewerken]
- (en) MSDS van fluoresceïne
- (en) Gegevens van fluoresceïne in de GESTIS-stoffendatabank van het IFA
Bronnen, noten en/of referenties
|

