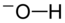Polyatomisch ion
Een polyatomisch ion (poly is Grieks voor veel) ook bekend als moleculair ion, is een geladen chemische verbinding: een ion dat wordt gevormd door de covalente binding tussen minstens twee atomen, afkomstig van meestal verschillende atoomsoorten.
Bekende voorbeelden van polyatomische ionen zijn het hydroxideanion (OH−) en het ammoniumkation (NH4+).
Een polyatomisch ion kan vaak beschouwd worden als het geconjugeerde zuur of de geconjugeerde base van een neutrale molecule. Het sulfaation (SO42−) is hiervan een voorbeeld: het is namelijk afgeleid van zwavelzuur (H2SO4), dat zelf kan beschouwd worden als het hydraat van zwaveltrioxide.
Nomenclatuur[bewerken | brontekst bewerken]
Er bestaan in de scheikundige nomenclatuur twee regels die kunnen toegepast worden om polyatomische ionen te benoemen. Wanneer het prefix bi- wordt gebruikt, dan dient aan de brutoformule van het ion een waterstof (formeel een proton) toegevoegd te worden. De lading van het ion stijgt met 1 eenheid. Als alternatief voor bi- wordt meestal waterstof- als prefix toegevoegd. Een voorbeeld is het carbonaat-anion (CO32−): wanneer hieraan een waterstof wordt toegevoegd, ontstaat het bicarbonaatanion (meestal waterstofcarbonaat genoemd) met als brutoformule HCO3−.
De tweede regel betreft het aantal zuurstofatomen in het ion (meestal van toepassing bij oxoanionen). Een voorbeeld vormen de (oxo)anionen van chloor:
| Oxidatietoestand | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Benaming | chloride | hypochloriet | chloriet | chloraat | perchloraat |
| Brutoformule | Cl− | ClO− | ClO2− | ClO3− | ClO4− |
| Molecuulmodel | 
|

|

|

|

|
De achtervoegsels -ide, -iet en -aat slaan op de verschillende oxidatietoestanden die chloor kan aannemen.
Overzicht van de meestvoorkomende polyatomische ionen[bewerken | brontekst bewerken]
Onderstaande tabel heeft een overzicht van veel voorkomende polyatomische ionen met hun brutoformule, structuurformule en moleculaire massa.
Anionen[bewerken | brontekst bewerken]
| Anion | Moleculaire massa (g/mol) | Brutoformule | Structuurformule |
|---|---|---|---|
| Acetaat | 59,04402 | CH3COO− |  |
| Benzoaat | 121,1134 | C6H5COO− |  |
| Waterstofcarbonaat (bicarbonaat) | 61,01684 | HCO3− |  |
| Carbonaat | 60,0089 | CO32− | 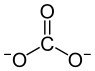 |
| Azide | 42,02065 | N3− | |
| Cyanide | 26,0174 | CN− | |
| Hydroxide | 17,00734 | OH− | |
| Nitraat | 62,0049 | NO3− |  |
| Fosfaat | 94,971362 | PO43− | 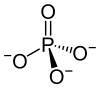 |
| Sulfaat | 96,0626 | SO42− |  |
| Chloraat | 83,4512 | ClO3− |  |
| Bromaat | 127,9022 | BrO3− |  |
| Cyclopentadienyl | 52,07511 | C5H5− |  |
Kationen[bewerken | brontekst bewerken]
| Kation | Moleculaire massa (g/mol) | Brutoformule | Structuurformule |
|---|---|---|---|
| Ammonium | 18,03846 | NH4+ |  |
| Hydroxonium | 19,02322 | H3O+ | 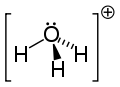 |
| Kwik(I) | 401,18 | Hg22+ | |
| Tropylium | 91,13048 | C7H7+ |  |