Koper(I)cyanide
| Koper(I)cyanide | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Kristalstructuur van koper(I)cyanide
| ||||
| Algemeen | ||||
| Molecuulformule | CuCN | |||
| IUPAC-naam | koper(I)cyanide | |||
| Andere namen | kopercyanide, cupricine | |||
| Molmassa | 89,5634 g/mol | |||
| SMILES | [C-]#N.[Cu+]
| |||
| InChI | 1S/CN.Cu/c1-2;/q-1;+1
| |||
| CAS-nummer | 544-92-3 | |||
| EG-nummer | 208-883-6 | |||
| PubChem | 11009 | |||
| Wikidata | Q419695 | |||
| Beschrijving | Wit tot groen poeder | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H300 - H310 - H330 - H410 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P260 - P264 - P273 - P280 - P284 - P301+P310 | |||
| EG-Index-nummer | 006-007-00-5 | |||
| VN-nummer | 1587 | |||
| LD50 (ratten) | (oraal) 1265 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit-groen | |||
| Dichtheid | 2,92 g/cm³ | |||
| Smeltpunt | 474 °C | |||
| Goed oplosbaar in | ammoniumhydroxide, kaliumcyanide | |||
| Slecht oplosbaar in | water | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Koper(I)cyanide is een toxische anorganische verbinding van koper en het cyanide-ion, met als brutoformule CuCN. De stof komt voor als een wit tot groen poeder, dat slecht oplosbaar is in water. Het oplosbaarheidsproduct (Ks) van koper(I)cyanide bedraagt 1,602 × 10−9. Het reageert zeer hevig met magnesium, nitraten en oxidatoren. In contact met zuren ontstaat het zeer toxische waterstofcyanide (HCN).
Synthese[bewerken | brontekst bewerken]
Koper(I)cyanide kan bereid worden door een reductie van koper(II)sulfaat met natriumcyanide. Hierbij ontstaan, naast koper(I)cyanide, ook nog oxalonitril en natriumsulfaat:
Toepassingen[bewerken | brontekst bewerken]
Wegens de hoge toxiciteit wordt het nog maar weinig commercieel gebruikt. Vroeger werd koper(I)cyanide ingezet als fungicide, insecticide en als algemeen biocide. Het kende ook toepassingen als katalysator bij polymerisaties, elektrodepositie van koper en ijzer en in scheepsverf.
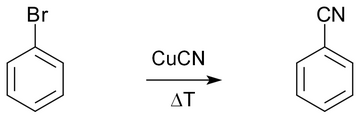
In de organische chemie kent het toepassing bij de Rosenmund-von Braun-reactie, waarbij een aryl-halogenide wordt omgezet naar een aryl-nitril: