Magnesium
Magnesium is een scheikundig element met symbool Mg en atoomnummer 12. Het is een zilverwit aardalkalimetaal.
Geschiedenis[bewerken | brontekst bewerken]
Magnesium is genoemd naar het district Magnesia in Thessalië in Griekenland. Magnesium was in de vorm van magnesiumoxide al heel lang bekend, maar pas in 1755 werd door de Schotse wetenschapper Joseph Black onderkend dat men bij magnesiumoxide (het werd toen nog niet zo genoemd) met een nieuwe stof te maken had. Tot die tijd werden magnesiumoxide en calciumoxide met elkaar verward en beide ongebluste kalk genoemd.
Toen in 1803 in Moravië een aanzienlijke afzetting van natuurlijk magnesiumcarbonaat werd ontdekt, werd dit door C.F. Ludwig aanvankelijk talcum carbonatum genoemd. De term magnesiet werd voor het eerst gebruikt in 1808 door L.G. Karsten. In datzelfde jaar werd door Humphry Davy ontdekt dat magnesiumoxide het oxide was van een metaal dat tot dan toe onbekend was. Naar verluidt zou hij ook de eerste persoon zijn geweest die een kleine hoeveelheid metallisch magnesium (als een amalgaan met kwik) wist te winnen door elektrolytische reductie van magnesiumoxide. De ontdekking van magnesium in zijn zuivere vorm zou echter op het conto komen van de Franse chemicus Antoine Bussy, die er in 1828 of 1831[1] in slaagde om niet alleen een grotere, maar ook een zuiverder hoeveelheid magnesium te prepareren.
Om magnesium te verkrijgen, liet Bussy magnesiumchloride (MgCl2) reageren met metallisch kalium. In 1833 probeerde Michael Faraday eveneens magnesium te produceren en wel door gedehydrateerd vloeibaar MgCl2 te elektrolyseren tot vloeibaar magnesium en chloorgas. In 1852 bouwde de Duitser Robert Bunsen een kleine cel voor de elektrolyse van MgCl2. Deze vinding leidde in Duitsland in 1886 tot de eerste commerciële productie van magnesium en tot uitgebreid onderzoek naar de toepassing van het materiaal. Tijdens de Tweede Wereldoorlog resulteerde dit in een relatief veelvuldig gebruik van magnesium in de oorlogsindustrie. Gebaseerd op Duitse patenten waarin dolomiet onder vacuüm gereduceerd was met een ijzer-siliciumverbinding, zette de Canadees Lloyd Montgomery Pidgeon in 1940 de eerste industrie op rond metallothermische magnesiumextractie. Dit zogeheten Pidgeonproces zou 60 jaar later nog steeds op grote schaal gebruikt worden.
Productie en recycling[bewerken | brontekst bewerken]
Magnesium kan geproduceerd worden middels elektrolyse van MgCl2 of door metallothermische reductie van MgO. Anno 1988 was de totale productie van magnesium afkomstig uit de omzetting van dolomiet (42%), metaalzouten (36%), zeewater (18%) en magnesiet (4%). Het productieproces voor de vorming van één kilo magnesium kost relatief veel energie, vergeleken met de conventionele materialen in de lichtgewicht-materiaal-industrie. Gekeken naar het volume is het echter juist energiezuiniger dan aluminium of zink en kan het zelfs de concurrentie met polymeren aan.
Bij het recyclen van magnesium zijn er meerdere problemen die omzeild moeten worden:
- Ongewenste insluitsels in het materiaal: niet-metallische deeltjes, intermetallische verbindingen en delen van oxidehuid.
- reactiviteit van magnesium: de smelt moet goed afgeschermd worden om de vorming van een oxidehuid te voorkomen. Hiervoor worden smeltzouten gebruikt.
Legering/naamgeving[bewerken | brontekst bewerken]
De naam van een magnesiumlegering bestaat uit vier delen.
- twee letters, die slaan op de twee legeringselementen die het meest in het materiaal aanwezig zijn.
- een (afgerond) getal, dat aangeeft hoeveel procent van de legering uit de twee belangrijkste legeringselementen bestaat.
- een letter uit het alfabet, die aan de legering wordt toegekend zodra hij voortaan als standaardlegering beschouwd wordt. De letters worden in oplopende volgorde uitgereikt, behalve de letter I en O.
- een letter, gevolgd door een nummer, dat iets zegt over de warmtebehandeling of versteviging die het materiaal heeft ondergaan.
Een gangbare magnesiumlegering is bijvoorbeeld de gietlegering AZ91A, die onder meer wordt toegepast in de auto-industrie. Het bevat 90 (88,2-91,2) %(m/m) Mg (magnesium), 9 (8,3-9,7) % Al (aluminium) en minimaal 0,13 % Mn (mangaan). Verder maximaal 0,5 % Si (silicium), maximaal 0,1 % Cu (koper), maximaal 0,03 % Ni (nikkel).
Kristalstructuur[bewerken | brontekst bewerken]
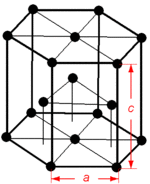
Zuiver magnesium heeft een hexagonale kristalstructuur, zoals is weergegeven in de afbeelding hiernaast. Door deze ingewikkelde structuur (ten opzichte van die van bijvoorbeeld aluminium of staal, die respectievelijk de kvg- en de krg-structuur bezitten) heeft het slechts beperkte mogelijkheden tot vervorming. In de jaren 30 en 40 ontdekte men dat magnesium bij kamertemperatuur tweelingen kan vormen aan de {}-vlakken in de -richting, en dat er afschuiving optreedt aan het (0001)-vlak in de -richting.
Toepassingen[bewerken | brontekst bewerken]

Omdat het met een fel wit licht brandt, wordt magnesium dikwijls in vuurwerk gebruikt als reductor en werd het in het verleden veel in flitslichten voor de fotografie toegepast.
Het metaal speelt een belangrijke rol in de organische synthese. Het reageert met een organohalogenide tot een organomagnesiumhalogenide: een klasse verbindingen die bekendstaan als de Grignard-reagentia.
Op het gebied van gewicht, sterkte en verwerkingseigenschappen voldoet magnesium aan de eisen om toe te passen in (lichtgewicht) constructies. Een voorbeeld van een constructieve toepassing van magnesium is de stadsfiets van de Engelse ontwerper Richard Thorpe. Een keramische deklaag beschermt het magnesium daar tegen corrosie. Een ander vlak waar magnesium als relevant gezien wordt, is de auto-industrie. Lichtgewicht voertuigen van magnesium zouden het brandstofverbruik sterk kunnen terugdringen. Experimenten met magnesium in de auto-industrie worden al gedaan sinds de ontwikkeling van de "Auto van de Toekomst" van 1952, de Buick LeSabre, maar vooralsnog blijft het toepassen van magnesium grotendeels voorbehouden aan onderdelen in voertuigen die op kleine schaal geproduceerd worden. De technieken voor het vervormen van magnesium en de bescherming van het materiaal die nodig is tegen corrosie, maken het metaal vooralsnog namelijk erg kostbaar.
Verder is het aantal bestaande legeringen nog niet zo uitgebreid en wordt er nog actief onderzoek verricht naar de verschillende vormingstechnieken van magnesium. Doordat de kennis over magnesium nog niet zo groot is, is men in de industrie nog geneigd tot het uitwijken naar de conventionele materialen zoals plastic en aluminium. Onderzoek wordt onder meer gedaan naar de extrusie van magnesium tot profielen in constructies en naar het spuitgieten van magnesium in thixotrope toestand (thixomoldingproces). Magnesium is thixotropisch (stroperig) bij 100 graden onder het smeltpunt.
Opmerkelijke eigenschappen[bewerken | brontekst bewerken]
Het metaal is nog een derde lichter dan aluminium en het is onontbeerlijk voor lichtgewicht legeringen met dit metaal. Deze legeringen worden veel gebruikt in de luchtvaartindustrie.
Magnesiumchemie wordt gekenmerkt door de elektronenconfiguratie [Ne]3s2: Het is een aardalkalimetaal. Het atoom raakt bij voorkeur de twee buitenste elektronen kwijt om het tweewaardige ion Mg2+ te vormen. Het metaal is een sterke reductor, hoewel minder sterk dan de alkalimetalen. In tegenstelling tot het beryllium ion Be2+ is Mg2+ niet bijzonder klein en het heeft dan ook niet de bijzonder giftige eigenschappen van zijn buurelement.
Magnesiumverbindingen spelen een beduidende biologische rol. Zo bevat chlorofyl, het pigment dat in planten zorgdraagt voor de fotosynthese, een magnesiumatoom. Het hydroxide Mg(OH)2 is een matige base en wordt wel als middel tegen maagzuur gebruikt. Het magnesiumsulfaat MgSO4.7H2O (bitterzout) werd als laxeermiddel en wordt bij toxicose (zwangerschapsvergiftiging) gebruikt. Bitterzout wordt ook gebruikt om te voorkomen dat naaldgewassen bruine naalden krijgen. Kieseriet is een magnesiumhoudende kunstmeststof en wordt gebruikt in de tuinbouw.
Normaal bevat een mol magnesiumsulfaat 7 mol kristalwater. Anhydrisch magnesiumsulfaat (dus zonder kristalwater) is sterk hygroscopisch en wordt in de organische chemie als droogmiddel gebruikt.
Verschijning[bewerken | brontekst bewerken]
Magnesium komt niet in zijn vrije vorm in de natuur voor, daar is het metaal veel te onedel voor. Het is het achtste element naar voorkomen op aarde. Er zijn wijdverspreide afzettingen van dolomiet en magnesiet waarin het in grote hoeveelheden voorkomt. Het wordt meestal gewonnen uit pekel die uit ondergrondse zoutlagen gehaald wordt. Het metaal kan daaruit door elektrolyse van het chloride MgCl2 gewonnen worden.
Het vormt een dun oxidehuidje aan de lucht, maar het metaal kan gemakkelijk tot ontbranden gebracht worden en brandt dan verwoed met een helle witte vlam. Een magnesiumbrand kan niet met water geblust worden doordat het metaal ook met water reageren kan via:
Het gevormde waterstof is ook brandbaar. Magnesiumbranden kunnen alleen met zand worden geblust.
Isotopen[bewerken | brontekst bewerken]
| Meest stabiele isotopen | |||||
|---|---|---|---|---|---|
| Iso | RA (%) | Halveringstijd | VV | VE (MeV) | VP |
| 23Mg | syn | 11,317 s | β+ | 4,057 | 23Na |
| 24Mg | 78,99 | stabiel met 12 neutronen | |||
| 25Mg | 10,00 | stabiel met 13 neutronen | |||
| 26Mg | 11,01 | stabiel met 14 neutronen | |||
| 27Mg | syn | 9,458 min | β− | 2,610 | 27Al |
| 28Mg | syn | 20,91 u | β− | 1,832 | 28Al |
Magnesium komt in de natuur als drie stabiele isotopen voor. 24Mg maakt daarvan ongeveer 80% uit. De overige 20 procent bestaat uit 25Mg en 26Mg. 26Mg is een vervalproduct van aluminium-26 dat een halveringstijd van 717 duizend jaar heeft. 26Mg wordt regelmatig in grote hoeveelheden aangetroffen in sommige meteorieten. Uit de verhouding tussen aluminium-26 en magnesium-26 kan dus bepaald worden hoe oud een meteoriet is.
Toxicologie en veiligheid[bewerken | brontekst bewerken]

Magnesium en zijn legeringen oxideren snel. Zowel fijn verdeeld als in gesmolten toestand kan het zeer heftig reageren met water en is het materiaal uiterst brandbaar. Bij verbranding ontstaat een opmerkelijk fel wit licht dat schade aan de ogen kan toebrengen. Om tijdens de verwerking van vloeibaar magnesium te voorkomen dat er een reactie met zuurstof optreedt, wordt er een beschermend gas gebruikt om het materiaal mee af te dekken. Fijn verdeeld magnesium wordt gedroogd en samengedrukt opgeslagen om zelfontbranding of een explosie te voorkomen. Deze eigenschappen van magnesium zorgen er overigens wel voor dat het geschikt is voor gebruik in de pyrotechniek.
Klinische betekenis[bewerken | brontekst bewerken]
Magnesium is een mineraal dat aanwezig is in iedere cel van het lichaam. Het is onmisbaar voor de energieproductie, de werking van spieren en zenuwen en voor het behoud van de stevigheid van botten. Magnesium speelt een belangrijke rol bij de werking van enzymen in het lichaam en is betrokken bij de aanmaak van hormonen. Ongeveer de helft van de magnesiumvoorraad in het lichaam bevindt zich (in combinatie met calcium en fosfaat) in het bot.
Voeding is de bron van magnesium. Het is aanwezig in vele voedingsmiddelen, met name in noten, granen, groene groenten zoals postelein, spinazie en erwten. De hoeveelheid magnesium in bloed, cellen en bot wordt door het lichaam constant gehouden. De regulatie gebeurt door aanpassing van opname (via de darmen) en uitscheiding (met de urine, via de nieren).
De dokter kan een bepaling van magnesium aanvragen als de patiënt aanhoudend een verlaagd calcium of kalium heeft, voor patiënten met symptomen die passen bij een verlaagd magnesium, onderzoek naar malabsorptie, ondervoeding, diarree of alcoholmisbruik, bij gebruik van sommige geneesmiddelen die de uitscheiding van magnesium door de nieren bevorderen of ter controle van de nierfunctie.
Afhankelijk van de voeding kan een magnesiumtekort ontstaan. Dit is bijvoorbeeld het geval in veel voedselproducten in de Westerse maatschappij. Door het voortdurend gebruik van eenzijdige kunstmest kan de grond zo arm worden aan magnesium, dat er een tekort in onze voeding kan ontstaan. De symptomen van een tekort zijn algehele lusteloosheid of vermoeidheid. Bij een langdurig tekort aan magnesium treden klachten op als irritatie van de zenuwen in de spieren, hartritmestoornissen en maagkrampen. Een lage concentratie magnesium (hypomagnesiëmie) kan het gevolg zijn van:
- onvoldoende inname van magnesium via de voeding, vooral bij ouderen, mensen met ondervoeding en bij alcoholmisbruik
- onvoldoende opname van magnesium via de darmen bijvoorbeeld als gevolg van de ziekte van Crohn (ontstekingen in het slijmvlies van de darmen)
- te hoge uitscheiding van magnesium via de nieren
- te hoge of te lage hoeveelheden glucose (suiker) in het bloed (ongecontroleerde diabetes)
- verminderde activiteit van de bijschildklier (hypoparathyreoïdie)
- langdurig gebruik van plaspillen (diuretica)
- langdurige diarree
- na een chirurgische ingreep
- bij ernstige brandwonden
- bij zwangerschapsvergiftiging
Bij een teveel aan magnesium kan lichte diarree ontstaan. Een verhoogde concentratie magnesium is zelden aan de voeding te wijten. Meestal is een verhoogd magnesium het resultaat van problemen bij uitscheiding of van kunstmatige toediening. Een verhoogd magnesium kan worden gevonden bij:
- nierfalen
- overactieve bijschildklier (hyperparathyreoïdie)
- slecht werkende schildklier
- uitdroging
- verzuring (te lage pH) van het bloed bij diabetes (diabetische acidose)
- ziekte van Addison
- gebruik van magnesium bevattende laxeermiddelen
- gebruik van magnesium als (onnodig) voedingssupplement
Externe link[bewerken | brontekst bewerken]
- Lenntech.nl - magnesium
- (en) EnvironmentalChemistry.com - magnesium
- (en) WebElements.com - magnesium
Bronnen, noten en/of referenties
|





