Grubbs' katalysator
| Grubbs' katalysator - 1e generatie | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
| ||||
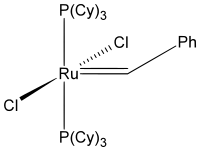
Structuurformule van Grubbs' katalysator - 1e generatie
| ||||

| ||||
Molecuulmodel van Grubbs' katalysator - 1e generatie
| ||||
| Algemeen | ||||
| Molecuulformule | C43H72Cl2P2Ru | |||
| IUPAC-naam | benzylideen-bis(tricyclohexylfosfine)dichloor-ruthenium | |||
| Wikidata | Q414452 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H315 - H319 - H335 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P261 - P305+P351+P338 | |||
| Fysische eigenschappen | ||||
| Smeltpunt | 153 °C | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
| Grubbs' katalysator - 2e generatie | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuurformule van Grubbs' katalysator - 2e generatie
| ||||

| ||||
Molecuulmodel van Grubbs' katalysator - 2e generatie
| ||||
| Algemeen | ||||
| Molecuulformule | C46H65Cl2N2PRu | |||
| IUPAC-naam | benzylideen[1,3- bis(2,4,6-trimethylfenyl)-2-imidazolidinylideen]dichloor (tricyclohexylfosfine)ruthenium | |||
| CAS-nummer | 246047-72-3 | |||
| Wikidata | Q414452 | |||
| Beschrijving | Paars-bruine vaste stof | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H228 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P210 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | paars-bruin | |||
| Smeltpunt | 143,5-148,5 °C | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Een Grubbs' katalysator is een coördinatieverbinding van het overgangsmetaal ruthenium met een alkeen, vernoemd naar de eerste chemicus die een dergelijk complex synthetiseerde: Robert Grubbs. Er zijn inmiddels twee generaties van deze katalysator bekend.[1][2] In tegenstelling tot andere katalysatoren voor de alkeenmetathese is het bij de Grubbs' katalysator mogelijk functionele groepen in de katalysator in te bouwen. Ook het gebruikte oplosmiddel is weinig kritisch.[3][4] Deze eigenschappen maken de Grubbs' katalysatoren zeer breed inzetbaar.
In 2005 ontvingen Robert H. Grubbs, Richard R. Schrock en Yves Chauvin de Nobelprijs voor de Scheikunde voor hun bijdragen in de ontwikkeling van dit type katalysatoren.
Eerste generatie
[bewerken | brontekst bewerken]De eerste generatie katalysator wordt vooral toegepast in de organische synthese bij het realiseren van:
- alkeenmetathesereacties
- ringopeningmetathesepolymerisaties
- acyclische dieenmetathesepolymerisaties
- ringsluitingsmetathese
De synthese van de katalysator is eenvoudig: uitgaande van RuCl2(PPh3)3,[5] fenyldiazomethaan en tricyclohexylfosfine in een one-pot-synthese.[6] Grubbs' katalysator is een tamelijk stabiele verbinding ten opzichte van lucht (dizuurstof en water), waardoor de verwerking ervan relatief makkelijk is.
Alkeenmetathese is een reactie tussen twee moleculen die beiden over een dubbele binding beschikken. De groepen die aan de koolstofatomen van de dubbele binding gebonden zijn worden uitgewisseld tussen de moleculen. Of een cis- of een trans-isomeer gevormd wordt in deze reactie is afhankelijk van de oriëntatie van de uitgangsstoffen aan de katalysator en van de ruimtelijke configuratie van de nieuwe molecule. Ook andere katalysatoren zijn in deze reactie werkzaam zoals die door Richard Schrock (Schrock-carbeen) ontwikkeld zijn. Katalysatoren van de eerste generatie zijn, evenals die van de tweede generatie, commercieel leverbaar.
Tweede generatie
[bewerken | brontekst bewerken]De tweede generatie Grubbs' katalysatoren heeft hetzelfde toepassingsgebied in de organische synthese, maar een hogere activiteit. De prijs voor de hogere reactiviteit is echter ook een grotere zuurstof- en vochtgevoeligheid en ze moeten dus in een inerte atmosfeer bewaard en verwerkt worden. Een katalysator gebaseerd op een onverzadigd stikstofhoudend heterocyclisch carbeen (1,3-bis(2,4,6-trimethylphenyl)dihydro-imidazool) is in deze groep als eerste in 1999 beschreven door een onderzoeksgroep rond Steven Nolan.[7] Grubbs beschreef later in hetzelfde jaar een katalysator gebaseerd op een verzadigd N-heterocyclisch carbeen: (1,3-bis(2,4,6-trimethylfenyl)imidazolidine).[5] Een fosfineligand is vervangen door N-heterocyclisch carbeen, waarbij ruthenium dus door twee carbenen gecoördineerd wordt. Katalysatoren van de tweede generatie zijn, evenals die van de eerste generatie, commercieel leverbaar.
Grubbs-Hoveyda katalysator
[bewerken | brontekst bewerken]Grubbs-Hoveyda-katalysatoren zijn een variatie op de Grubbs' katalysatoren, ontwikkeld door Amir H. Hoveyda. In de eerste generatie is een van de fosfineliganden vervangen door een aan de benzeenring gekoppelde isopropyloxygroep. In de tweede generatie van dit type is de tweede fosfineligand ook vervangen, maar door een stikstofhoudende heterocyclische groep.
Wateroplosbare Grubbs' katalysatoren zijn ook beschreven. Door een polyethyleenglycolketen te koppelen aan de imidazolinering wordt de verbinding wateroplosbaar. Het imidazoliniumzout wordt met behulp van kaliumhexamethyldisilazide (KHMDS) gedeprotoneerd tot het N-heterocyclisch carbeen, dat een van de fosfineliganden vervangt waardoor het aangepaste rutheniumcomplex ontstaat:[8]
Deze katalysator is gebruikt in de ringsluitingsmetathese van een dieen dat via zijn ammoniumzout ook wateroplosbaar was gemaakt:
Toepassing in de ruimtevaart
[bewerken | brontekst bewerken]Een interessant toepassingsgebied van Grubbs' katalysatoren zou de ruimtevaartindustrie kunnen worden. De buitenzijde van de romp van een ruimteveer moet van een zeer sterk soort materiaal gemaakt zijn, maar ook daarin ontstaan met de tijd microscheurtjes. Een nieuw materiaal waarin een Grubbs' katalysator is verwerkt, samen met capsules met dicyclopentadieen vormt hier een oplossing. Als een microscheurtje ontstaat, zullen de capsules breken waardoor het dicyclopentadieen in contact komt met de Grubbs' katalysator en via een ringopeningmetathesepolymerisatie het scheurtje afdicht.[9]
- ↑ R.H. Grubbs. (2003). GEEN TITEL OPGEGEVEN Handbook of Metathesis – Wiley-VCH, Germany ISBN 3-527-30616-1
- ↑ R.H. Grubbs, T.M. Trnka,. (2004). Ruthenium-Catalyzed Olefin Metathesis Ruthenium in Organic Synthesis" (S.-I. Murahashi, Ed). – Wiley-VCH, Germany DOI:10.1002/3527603832.ch6
- ↑ G.C. Vougioukalakis, R.H. Grubbs. (2010). Ruthenium-Based Heterocyclic Carbene-Coordinated Olefin Metathesis Catalysts Chem. Rev.. 110 pag.: 1746 - 1787 DOI:10.1021/cr9002424
- ↑ T.M. Trnka, R.H. Grubbs. (2001). The Development of L2X2Ru=CHR Olefin Metathesis Catalysts: An Organometallic Success Story Accounts of Chemical Research. 34 pag.: 18–29 DOI:10.1021/ar000114f
- ↑ a b M. Scholl, S. Ding, C.W. Lee, R.H. Grubbs. (1999). Synthesis and Activity of a New Generation of Ruthenium-Based Olefin Metathesis Catalysts Coordinated with 1,3-Dimesityl-4,5-dihydroimidazol-2-ylidene Ligands Organic Letters. 1 pag.: 953–956 DOI:10.1021/ol990909q
- ↑ P. Schwab, R.H.Grubbs, J.W. Ziller. (1996). Synthesis and Applications of RuCl2(=CHR')(PR3)2: The Influence of the Alkylidene Moiety on Metathesis Activity J. of the Amer. Chem. Soc.. 118 pag.: 100–110 DOI:10.1021/ja952676d
- ↑ Jinkun Huang, Edwin D. Stevens, Steven P. Nolan, Jeffrey L. Petersen. (1999). Olefin Metathesis-Active Ruthenium Complexes Bearing a Nucleophilic Carbene Ligand J. Amer. Chem. Soc.. 121 pag.: 2674–2678 DOI:10.1021/ja9831352
- ↑ Soon Hyeok Hong, Robert H. Grubbs. (2006). Highly Active Water-Soluble Olefin Metathesis Catalyst J. Amer. Chem. Soc.. 128 pag.: 3508–3509 DOI:10.1021/ja058451c
- ↑ S.R. White, N.R. Sottos, P.H. Geubelle, J.S. Moore, M.R. Kessler, S.R. Sriram, E.N. Brown, S. Viswanathan. (2001). Autonomic healing of polymer composites Nature. 409 pag.: 794–797 DOI:10.1038/35057232




