3-methyl-2-butanon
| 3-methyl-2-butanon | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
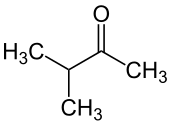
| ||||
Structuurformule van 3-methyl-2-butanon
| ||||
| Algemeen | ||||
| Molecuulformule | C5H10O | |||
| IUPAC-naam | 3-methylbutaan-2-on | |||
| Andere namen | isopropylmethylketon, methylbutanon, 2-acetylpropaan, methylisopropylketon | |||
| Molmassa | 86,1323 g/mol | |||
| SMILES | CC(C)C(=O)C
| |||
| InChI | 1S/C5H10O/c1-4(2)5(3)6/h4H,1-3H3
| |||
| CAS-nummer | 563-80-4 | |||
| EG-nummer | 209-264-3 | |||
| PubChem | 11251 | |||
| Wikidata | Q2747560 | |||
| Beschrijving | Kleurloze vloeistof met kenmerkende geur | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H225 - H319 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P210 - P305+P351+P338 | |||
| Opslag | Gescheiden van ontvlambare stoffen en sterk oxiderende stoffen. Brandveilig en goed gesloten bewaren. | |||
| EG-Index-nummer | 606-007-00-0 | |||
| VN-nummer | 2397 | |||
| ADR-klasse | Gevarenklasse 3 | |||
| MAC-waarde | 200 ppm 70 mg/m³ | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos | |||
| Dichtheid | 0,803 - 0,805 g/cm³ | |||
| Smeltpunt | −92 °C | |||
| Kookpunt | 93-95 °C | |||
| Vlampunt | −1 °C | |||
| Zelfontbrandings- temperatuur | 475 °C | |||
| Dampdruk | (bij 20 °C) 5500 Pa | |||
| Oplosbaarheid in water | (bij 20 °C) 6 g/L | |||
| Goed oplosbaar in | alcohol, di-ethylether | |||
| Matig oplosbaar in | water | |||
| Brekingsindex | 1,3880 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
3-methyl-2-butanon is een zeer ontvlambare organische verbinding met als brutoformule C5H10O. De stof komt voor als een kleurloze vloeistof met een kenmerkende geur, die matig oplosbaar is in water. De verbinding kent 2 structuurisomeren: 2-pentanon en 3-pentanon.
3-methyl-2-butanon wordt voornamelijk gebruikt als organisch oplosmiddel en in organische syntheses.
Naamgeving
[bewerken | brontekst bewerken]Strikt genomen zijn de locanten niet noodzakelijk. Met de stamnaam butaan zijn vier koolstofatomen gegeven. De uitgang ~on geeft aan dat een dubbel-gebonden zuurstof-atoom als substituent niet aan het eind van de keten aanwezig is (de uitgang zou dan ~al zijn). Dit zuurstofatoom moet dus aan een van de twee koolstof-atomen in het midden van de keten aanwezig zijn. Op welk van de twee atomen maakt niet uit, het betreffende koolstof-atoom zal altijd als locant nummer 2 krijgen. De locant is dus niet noodzakelijk.
Het feit dat de methylgroep apart genoemd wordt betekent dat de groep niet aan een van de eindstandige koolstofatomen aanwezig is. Dan zou hij meegeteld worden in de langste keten en zou de stamnaam van de verbinding pentaan zijn. Omdat de substitutieplaatsen op koolstof-atoom 2 volledig bezet zijn, moet deze groep dus aan het enige overgebleven niet-eindstandige koolstof-atoom gebonden zijn, dus nummer 3. Ook hier is de lokant dan niet nodig.
Toxicologie en veiligheid
[bewerken | brontekst bewerken]De stof ontleedt bij verhitting, met vorming van irriterende dampen. Ze reageert hevig met oxidatoren.
De stof is irriterend voor de ogen, de huid en de luchtwegen. De stof kan effecten hebben op het centraal zenuwstelsel, met als gevolg algemene verdoving en zwakte.
Externe links
[bewerken | brontekst bewerken] 3-methyl-2-butanon - International Chemical Safety Card
3-methyl-2-butanon - International Chemical Safety Card- (en) MSDS van 3-methyl-2-butanon
- (en) Gegevens van 3-methyl-2-butanon in de GESTIS-stoffendatabank van het IFA


