Ureum-waterstofperoxide
| Carbamideperoxide | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
| Algemeen | ||||
| Molecuulformule | ||||
| IUPAC-naam | Hydrogen peroxide–urea (1/1) | |||
| Andere namen | > Peroxol–carbonyl diamide (1/1) >Urea peroxide >percarbamide >UHP | |||
| Molmassa | 94,070 g/mol | |||
| SMILES | O=C(N)N.OO
| |||
| CAS-nummer | 124-43-6 | |||
| PubChem | 31294 | |||
| Wikidata | Q2633879 | |||
| Beschrijving | Witte, vaste stof | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H272 - H315 - H318 | |||
| P-zinnen | P210 - P220 - P264 - P280 - P302+P352 - P305+P351+P338 | |||
| Fysische eigenschappen | ||||
| Dichtheid | 1,50 g/cm³ | |||
| Smeltpunt | 75 - 91,5 °C(ontleedt) | |||
| Vlampunt | 60 °C | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Ureum-waterstofperoxide (UHP = Engelse afkorting voor Urea Hydrogen Peroxide), ook bekend onder de namen waterstofperoxide–ureum, Hyperol, artizone en in de tandheelkunde als carbamideperoxide, is een witte, kristallijne verbinding, een complex of adduct, van equimolaire hoeveelheden ureum en waterstofperoxide. Het kan gezien worden als een vaste, watervrije vorm van waterstofperoxide. Opgelost in water fungeert het als een bron van waterstofperoxide bij bleken, desinfectie en oxidatie.
Synthese[bewerken | brontekst bewerken]
Voor de productie van UHP wordt ureum opgelost in 30% waterstofperoxide (molverhouding 2:3) bij een temperatuur van maximaal 60 °C, bij afkoelen slaat de stof neer.[3]
Net als bij kristalwater in hydraten, kristalliseert waterstofperoxide samen met ureum uit. Er is maar één molecuul per ureum-molecuul. De verbinding wordt eenvoudig bereid in honderden tonnen per jaar door ureum op te lossen in een overmaat warme waterstofperoxide-oplossing en deze dan te laten afkoelen waarbij de stof neerslaat.[4] Op laboratoriumschaal verloopt de synthese op de zelfde manier.[5]
Structuur[bewerken | brontekst bewerken]
De structuur van de vaste fase van UHP is bepaald met behulp van neutronendiffractie.[6]
Eigenschappen[bewerken | brontekst bewerken]
Ureum-waterstofperoxide is een makkelijk in water oplosbare kleur- en geurloze kristallijne vaste stof die geleverd wordt als wit poeder, kleurloze naalden of in pellets.[3] Bij het oplossen in de diverse oplosmiddelen dissocieert het 1:1-complex in ureum en waterstofperoxide, net als zouthydraten waarbij de hydraterende watermoleculen ook niet aan de zout-ionen gekoppeld blijven. De stof is dus, net als waterstofperoxide, een oxidator, maar wel een die veel veiliger, beter te controleren en te doseren is. Ook de stabiliteit bij hogere temperaturen is beter.[7]
De oplosbaarheid van commerciële monsters kan variëren 0,05 g/mL[8] tot meer dan 0,6 g/mL.[9]
Toepassingen[bewerken | brontekst bewerken]
Desinfentie en bleken[bewerken | brontekst bewerken]
UHP wordt vooral vanwege zijn desinfecterende en blekende werking gebruikt in de cosmetische en farmaceutische industrie[4] In sommige soorten bleekmiddelen voor tanden komt het voor.[4][10][11] Het wordt ook gebruikt in de bestrijding van kleinere infecties van tandvlees, het mondslijmvlies, de lippen (aften)[12] en om oorsmeer minder droog te maken.[13]
Reagens in de organische synthese[bewerken | brontekst bewerken]
In het laboratorium wordt het toegepast als een makkelijker hanteerbare vervanging voor waterstofperoxide.[5][14][15] Het blijkt een stabiel, makkelijk toepasbaar en effectief oxiderend reagens te zijn, dat zich goed laat sturen door een juiste keuze van reactie-omstandigheden. Het geeft oxidatieproducten op een milieuvriendelijke manier en vaak in goede tot zeer goede opbrensten, vooral in aanwezigheid van katalysatoren als maleïnezuuranhydride[16] of natriumwolframaat.[17]
Thiolen worden door UHP selectief omgezet in disulfides,[16] secondaire alcoholen in ketonen,[17] Sulfides in sulfoxides en sulfonen,[18] nitrilen tot amides,[18][19] en N-heterocyclische verbindingen in amineoxides.[18][20]
Hydroxybenzaldehydes worden door UHP omgeze in dihydroxybenzenen (Dakin-oxidatie)[18][21] en onder de juiste reactieomstandigheden ontstaan de overeenkomstige benzoëzuren.[21]

Ketonen, met name cyclische, worden in een Baeyer-Villiger-reactie door UHP omgezet in esters, zoals uit onderstaand voorbeeld blijkt:[22][23]
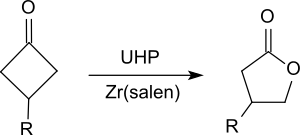
Met verschillende alkenen geeft UHP, in aanwezigheid van benzonitril, goede opbrensten aan epoxides (79 tot 96%).[24]
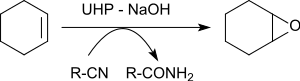
Het zuurstof-atoom dat aan het alkeen gekoppeld wordt is afkomstig van het peroxoimidezuur dat als intermediair gevormd wordt uit benzonitril. Het resterende imidezuur tautomeriseert naar het benzamide.
Overzicht van de verschillende reactie van UHP[bewerken | brontekst bewerken]
In onderstaand overzicht zijn de verschillende hierboven genoemde reacties in één figuur weergegeven:

Veiligheid[bewerken | brontekst bewerken]
Hoewel UHP een goed hanteerbare verbinding is, blijft het een sterke oxidator die huidirritatie en ernstig oogletsel kan veroorzaken.[25] UHP bleek ook een, wel is waar stabiel, explosief dat, indien sterk samengedrukt, slaggevoelig is.[26][27]
Zie ook[bewerken | brontekst bewerken]
Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Hydrogen peroxide–urea op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
Externe links
- Hydrogen peroxide urea adduct, UHP. Organic Chemistry Portal.
- Carbamide Peroxide Monograph. Drugs.com.
Verwijzingen in de tekst
- ↑ GHS: Sigma-Aldrich 289132
- ↑ External MSDS
- ↑ a b C.-S. Lu, E.W. Hughes, P.A. Giguère (1941). The crystal structure of the urea-hydrogen peroxide addition compound 63 (6): 1507–1513. DOI: 10.1021/ja01851a007.
- ↑ a b c Harald Jakob; Stefan Leininger; Thomas Lehmann; Sylvia Jacobi; Sven Gutewort. "Peroxo Compounds, Inorganic". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a19_177.pub2. ISBN 978-3527306732.
- ↑ a b Yu, Lei, Meng, Bo, Huang, Xian (2008). Urea-Hydrogen Peroxide Complex: A Selective Oxidant in the Synthesis of 2-Phenylselenyl-1,3-butadienes. Synthetic Communications 38 (18): 3142. DOI: 10.1080/00397910802109224.
- ↑ Fritchie, C. J. Jr., McMullan, R. K. (1981). Neutron Diffraction Study of the 1:1 Urea:Hydrogen Peroxide complex at 81 K. Acta Crystallographica Section B 37 (5): 1086. DOI: 10.1107/S0567740881005116.
- ↑ Waterstofperoxide begint spontaan te ontleden bij 82°C.
H. Heaney, F. Cardona, A. Goti, A.L. Frederick. 2013 Encyclopedia of Reagents for Organic Synthesis. , hoofdstuk Hydrogen Peroxide-Urea – DOI:10.1002/047084289X.rh047.pub3 geraadpleegd op 2013 - ↑ Sigma-Aldrich specification sheet
- ↑ Chemicalland data sheet
- ↑ Mokhlis, G. R., Matis, B. A., Cochran, M. A., Eckert, G. J. (2000). A Clinical Evaluation of Carbamide Peroxide and Hydrogen Peroxide Whitening Agents during Daytime Use. Journal of the American Dental Association 131 (9): 1269–77. PMID 10986827. DOI: 10.14219/jada.archive.2000.0380. Gearchiveerd van origineel op 23 februari 2013.
- ↑ Toothwhitening Sjabloon:Webarchive from the University of Medicine and Dentistry of New Jersey website
- ↑ Center for Integrative Medicine: Carbamide Peroxide from the University of Maryland Medical Center website Sjabloon:Webarchive
- ↑ . Ear Drops GENERIC NAME(S): CARBAMIDE PEROXIDE geraadpleegd op 3 juli 2021 WebMD
- ↑ Varma, Rajender S., Naicker, Kannan P. (1999). The Urea−Hydrogen Peroxide Complex: Solid-State Oxidative Protocols for Hydroxylated Aldehydes and Ketones (Dakin Reaction), Nitriles, Sulfides, and Nitrogen Heterocycles. Organic Letters 1 (2): 189. DOI: 10.1021/ol990522n.
- ↑ Harry Heaney, Francesca Cardona, Andrea Goti, "Hydrogen Peroxide–Urea" Encyclopedia of Reagents for Organic Synthesis 2008. DOI:10.1002/047084289X.rh047.pub2
- ↑ a b (de) B. Karami, M. Montazerozohori, M. H. Habibi. Urea-Hydrogen Peroxide (UHP) oxidation of thiols to the corresponding disulfides promoted by maleic anhydride as mediator Molecules. 10 (10): 1358–1363 DOI:10.3390/10101385 PubMed Central: 6147623
- ↑ a b (en) M. LukasiewiczD. BogdalJ. Pielichowski. Microwave-assisted oxidation of alcohols using urea hydrogen peroxide10 mei 2016 8th International Electronic Conference on Synthetic Organic Chemistry. ECSOC-8. geraadpleegd op 10 mei 2016
- ↑ a b c d (de) R.S. Varma, K.P. Naicker. The Urea-Hydrogen Peroxide Complex: Solid-State Oxidative Protocols for Hydroxylated Aldehydes and Ketones (Dakin Reaction), Nitriles, Sulfides, and Nitrogen Heterocycles Org. Lett.. 1 (2): 189–191 DOI:10.1021/ol990522n Nitrillen in amides
- ↑ WO patent 2012069948, : 4-(5-Cyano-pyrazol-1-yl)-piperidine derivatives as GPR 119 modulators
- ↑ (de) D. Rong, V.A. Phillips, R.S. Rubio. A safe, convenient and efficient method for the preparation of heterocyclic N-oxides using urea-hydrogen peroxide Tetrahedron Lett.. 49 (48): 6933–6935 DOI:10.1016/j.tetlet.2008.09.124
- ↑ a b (de) H. Heaney, A.J. Newbold. The oxidation of aromatic aldehydes by magnesium monoperoxyphthalate and urea-hydrogen peroxide Tetrahedron Lett.. 42 (37): 6607–6609 DOI:10.1016/S0040-4039(01)01332-6
- ↑ (de) A. Watanabe, T. Uchida, K. Ito. Highly enantioselective Baeyer-Villiger oxidation using Zr(salen) complex as catalyst Tetrahedron Lett.. 43 (25): 4481–4485 DOI:10.1016/S0040-4039(02)00831-6
- ↑ (de) M.Y. Rios, E. Salazar, H.F. Olivo. Baeyer–Villiger oxidation of substituted cyclohexanones via lipase-mediated perhydrolysis utilizing urea–hydrogen peroxide in ethyl acetate Green Chem.. 9 (5): 459–462 DOI:10.1039/B618175A
- ↑ (de) L. Ji, Y.-N. Wang, C. Qian, X.-Z. Chen. Nitrile-promoted alkene epoxidation with urea-hydrogen peroxide (UHP) Synth. Commun.. 43 (16): 2256–2264 DOI:10.1080/00397911.2012.699578
- ↑ . merckmillipore.com: Hydrogen peroxide urea SDS geraadpleegd op 16 mei 2023
- ↑ Halleux, Francis, Pons, Jean‐François, Wilson, Ian, Van Riet, Romuald, Lefebvre, Michel (2022). Small-Scale Detonation of Industrial Urea-Hydrogen Peroxide (UHP). Propellants, Explosives, Pyrotechnics 47 (2). DOI: 10.1002/prep.202100250.
- ↑ Halleux, Francis, Pons, Jean‐François, Wilson, Ian, Simoens, Bart, Van Riet, Romuald (2023). Detonation performance of urea‐hydrogen peroxide (UHP). Propellants, Explosives, Pyrotechnics 48 (6). DOI: 10.1002/prep.202300011.





