Biotine
| (+)-Biotine | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuurformule van (+)-biotine
| ||||
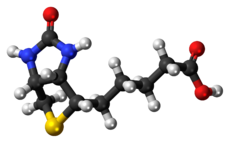
| ||||
Molecuulmodel van biotine
| ||||
| Algemeen | ||||
| Molecuulformule | C10H16N2O3S | |||
| Andere namen | vitamine B7; vitamine B8; vitamine H; co-enzym R; bios IIb; bioepiderm; factor S | |||
| Molmassa | 244,31064 g/mol | |||
| CAS-nummer | 58-85-5 | |||
| EG-nummer | 200-399-3 | |||
| PubChem | 171548 | |||
| Wikidata | Q181354 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos | |||
| Smeltpunt | 232-233 °C | |||
| Oplosbaarheid in water | 0,2 g/L | |||
| Nutritionele eigenschappen | ||||
| Type nutriënt | Wateroplosbaar B-vitamine | |||
| Essentieel? | Ja, aanbevolen dosis 0,03–0,06 mg daags. Wordt geproduceerd door darmbacteriën. | |||
| Komt voor in | Eieren, lever, melk, pinda's | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Biotine, ook wel vitamine H genoemd, is een van de B-vitaminen. Het is een heterocyclische verbinding die een belangrijke rol speelt bij diverse stofwisselingsreacties. Het vervult als co-enzym een essentiële functie bij de metabolisatie van voornamelijk suiker, vet en aminozuren. De naam biotine is afgeleid van het Griekse woord 'bios' (leven) en het achtervoegsel '-ine' (een algemeen chemisch achtervoegsel).
Beschrijving van de functie[bewerken | brontekst bewerken]
Biotine speelt bij mensen een belangrijke rol bij de vet- en suikerstofwisseling en de productie van vetzuren. Biotine is nodig voor de opname van vitamine C uit de ingewanden.
Biotine heeft co-enzym-eigenschappen die het in staat stellen koolhydraten en eiwitten om te zetten in energie en deel te nemen in de productie van prostaglandinen uit essentiële vetzuren.
Biotine is de co-factor (prosthetische groep) van de enzymen carboxylasen (specifieker: carboxytransferasen). Biotine is via zijn COOH-groep op een specifiek lysine-residue verbonden van de carboxylase. De werking van dit enzym zorgt ervoor dat in het organisme koolstofdioxide gefixeerd wordt.
Andere belangrijke toepassingsgebieden van biotine zijn groei en herstelprocessen van de huid, het haar, de nagels, de zenuwen en het beenmerg. Om die reden wordt het vaak ingezet bij haaruitval en haargroeiproblemen. Het wordt soms in shampoos verwerkt, maar het effect daarvan is twijfelachtig, aangezien biotine niet door de huid wordt geabsorbeerd.
Voorkomen[bewerken | brontekst bewerken]
Hoewel dieren het vermogen missen om biotine aan te maken, wordt het wel aangemaakt door micro-organismen en planten. Daardoor komt het in veel verschillende voedingsmiddelen voor, maar in het algemeen in lage concentraties. Er zijn maar enkele voedingsmiddelen die biotine in grote hoeveelheden bevatten, zoals koninginnengelei en bakkersgist.
De beste natuurlijke bronnen van biotine in de menselijke voeding zijn orgaanvlees, zoals lever en nieren, evenals eierdooier en sommige groenten. Lever bevat ongeveer 1 mg/kg biotine. Fruit, de meeste groenten en (spier)vlees zijn slechte bronnen en bevatten slechts ongeveer 0,01 mg biotine per kg.
Voor wat betreft groenten zijn peulvruchten, sojabonen, pinda's, bieten, tomaten, sla en wortelen goede bronnen, alhoewel de concentraties daar ook relatief laag zijn. Verder nog havervlokken en rijst.
Opgemerkt moet worden dat het biotinegehalte van voeding kan variëren. Het wordt onder meer beïnvloed door factoren als plantensoort, seizoen en raffinage (in geval van granen).[1]
Biologische beschikbaarheid[bewerken | brontekst bewerken]
De biologische beschikbaarheid van biotine varieert enorm, maar is gemiddeld genomen minder dan 50%. In sommige granen, zoals maïs, is de biologische beschikbaarheid bijna 100%, terwijl deze in andere granen, zoals tarwe, niet meer dan 5% is.[1]
Synthese in de darm[bewerken | brontekst bewerken]
Darmbacteriën kunnen biotine samenstellen, maar de synthese van deze vitamine kan worden aangetast door antibiotica en andere medicijnen.
Deficiëntie[bewerken | brontekst bewerken]
Biotinetekort kan optreden bij het eten van grote hoeveelheden rauw ei, omdat ei-eiwit avidine bevat, dat aan biotine bindt en de opname daarvan in de darm blokkeert. Verhitting inactiveert avidine, waardoor bij consumptie van gekookte of gebakken eieren geen gevaar meer bestaat voor biotinedeficiëntie. Biotine bindt aan avidine en aanverwante eiwitten (streptavidine en neuravidine), met een affiniteitsconstante K van 1015 M−1.
Een biotinetekort uit zich in huidverstoringen, haaruitval, zwakke nagels, bloedarmoede, depressies, vermoeidheid, spierpijn, verhoogde cholesterol, ontsteking van de tong, en tintelingen of gevoelloosheid in armen en benen.
Er bestaat een erfelijke ziekte, biotinidasedeficiëntie (BIO), waarbij te weinig biotine wordt aangemaakt.[2] Ook deze erfelijke ziekte wordt opgespoord middels de hielprik.
Geschiedenis[bewerken | brontekst bewerken]
De ontdekking van biotine:
- 1898 - Steinitz - vitamine H (van huid)
- 1901 - Wildiers - bios
- 1931 - Paul György - vitamine H
- 1936 - Fritz Kögl en Benno Tönnis - isolatie van biotine uit 1000 verse eierdooiers
- 1940 - Ontdekking (door György) dat biotine identiek is met vitamine H en co-enzym R
- 1942 - Vincent du Vigneaud - vaststellen van de chemische structuur
- 1943 - Harris - de eerste chemische synthese van biotine
Externe link[bewerken | brontekst bewerken]
- Biotine op voedingscentrum.nl
Bronnen, noten en/of referenties
|
