Autoprotolyse van water
| ZUREN en BASEN |
|---|
 |
| Algemene begrippen |
| pH Zuur-basereactie Zuur-basetitratie Zuurconstante Buffer Waterevenwicht Hammett-zuurfunctie |
| Zuren |
|
Sterk · Zwak · Lewiszuur · Anorganisch zuur · Organisch zuur · Superzuur · Oxozuur · Halogeenzuurstofzuur |
| Basen |
|
Sterk · Zwak · Lewisbase · Organische base |
| Portaal |
Autoprotolyse van water (ook wel aangeduid als auto-ionisatie of auto-dissociatie van water) of het waterevenwicht is een chemische reactie waarbij een waterstofion (H+) overgedragen wordt van de ene watermolecule naar de andere. Daarbij ontstaan twee ionen: het hydroxonium- en het hydroxide-ion. De reactie is een evenwichtsreactie die kan worden geschreven als:
Hierbij wordt duidelijk dat water als zuur en als base kan optreden: water is dus een amfotere verbinding. Het zuurstofatoom in water bezit twee vrije elektronenparen en kan daarmee een waterstofion van een andere watermolecule opnemen. Hierdoor wordt een coördinatief covalente binding tussen zuurstof en een waterstofion gevormd.
Er komt ook een gedeelte H4O2+-ionen voor, maar dit is verwaarloosbaar: de concentratie van dit ion ligt in een grootte-orde van 10−49 mol/L.
Beschrijving van het evenwicht[bewerken | brontekst bewerken]
Volledig chemisch zuiver water bezit een elektrische geleidbaarheid van 0,055 µS·cm−1. Deze geleidbaarheid wordt volgens de theorieën van Svante Arrhenius veroorzaakt door ionen die afkomstig zijn van autoprotolyse van water:
De evenwichtsconstante (in evenwichtsconcentraties) voor dit autoprotolyse-evenwicht wordt gegeven door:
De waarde voor deze evenwichtsconstante bedraagt (bij 25 °C) 3,24 × 10−18. In het geval van zuiver water kan de evenwichtsconcentratie aan water als constant worden beschouwd, namelijk 55,5 mol/L. Hierdoor kan de uitdrukking voor de evenwichtsconstante worden herschreven tot de uitdrukking:
Dit wordt het ionenproduct van water genoemd. Bij 25 °C bedraagt dit ionenproduct ongeveer 1,0 × 10−14. De negatieve logaritme van deze waarde wordt de pKw genoemd en wordt gegeven door de uitdrukking:
Aangezien iedere watermolecule dissocieert in een gelijke hoeveelheid hydroxonium- en hydroxide-ionen, kunnen beide evenwichtsconcentraties worden vastgesteld op 1,0 × 10−7 mol/L.
Een oplossing waarin het aantal hydroxonium- en hydroxide-ionen gelijk is, wordt een neutrale oplossing genoemd en bezit per definitie een pH van 7. De pH wordt immers gedefinieerd als
Het evenwicht kan echter verstoord worden door een hoeveelheid zuur of base toe te voegen aan water, zodat de concentraties van de hydroxonium- en hydroxide-ionen van elkaar gaan verschillen. Bovendien is water gevoelig voor opname van koolstofdioxide, waarmee het onstabiele zuur diwaterstofcarbonaat wordt gevormd. Hierdoor wordt water dat aan de lucht wordt blootgesteld op den duur licht zuur. Omdat daarbij de concentratie aan hydroxoniumionen stijgt, zal de concentratie aan hydroxide-ionen afnemen, opdat aan de constante waarde van het ionenproduct voldaan wordt.
Kinetisch mechanisme[bewerken | brontekst bewerken]
De snelheid van de reactie
hangt af van de activeringsenergie ΔE‡. Volgens de Boltzmann-verdeling wordt de hoeveelheid watermoleculen met voldoende energie gegeven door (met k de Boltzmannconstante):
De activeringsenergie kan verhoogd worden door de temperatuur te verhogen. Dit leidt tot vorming van meer ionen.
Afhankelijkheid van temperatuur, druk en ionsterkte[bewerken | brontekst bewerken]
Het autoprotolyse-evenwicht kan verschoven worden door de temperatuur te veranderen. In het geval van een temperatuursverhoging zal de ionisatiegraad toenemen, waardoor pKw afneemt. Het minimum wordt bereikt bij ongeveer 250 °C. Vanaf dan neemt de waarde toe tot aan de kritische temperatuur van water (ongeveer 374 °C).
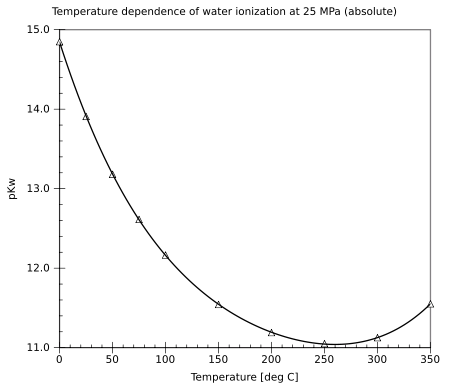
Daarnaast kan worden vastgesteld dat de pKw afneemt met toenemende druk:

Het evenwicht is ook afhankelijk van de ionsterkte van water (bijvoorbeeld in elektrolytoplossingen). Voor lage ionsterktes neemt de pKw af, maar bij hogere waarden zal de pKw stijgen.
Isotoopeffect[bewerken | brontekst bewerken]
Zwaar water (gedeutereerd water) of D2O ondergaat veel minder de autoprotolyse dan gewoon water. De reden hiervoor is dat zuurstof een iets sterkere binding vormt met deuterium omdat deuterium een hogere massa heeft dan protium en dus ook een lagere nulpuntsenergie bezit. Onderstaande tabel geeft enkele pKw-waarden voor gewoon water en zwaar water bij verschillende temperaturen:
T (°C) 10 20 25 30 40 50 H2O 14,535 14,167 13,997 13,830 13,535 13,262 D2O 15,439 15,049 14,869 14,699 14,385 14,103


![{\displaystyle K_{eq}={\frac {\mathrm {[H_{3}O^{+}][OH^{-}]} }{\mathrm {[H_{2}O]^{2}} }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b3aecc7c9bb29ff4efed99baa700b3e5d3ca0d36)
![{\displaystyle K_{w}=\mathrm {[H_{3}O^{+}][OH^{-}]} =K_{eq}\times \mathrm {[H_{2}O]^{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/861396fb6a69654307e7294bc33386b655e89948)

![{\displaystyle \mathrm {pH} =-\log \left(\mathrm {[H_{3}O^{+}]} \right)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a708346772491b3c62faf09b9d5ca9444c54aa48)

