Benzylideenaceton
| Benzylideenaceton | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
| ||||
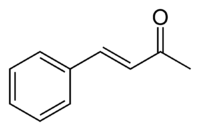
Structuurformule van benzylideenaceton
| ||||
| ||||
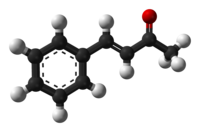
Molecuulmodel van benzylideenaceton
| ||||
| Algemeen | ||||
| Molecuulformule | C10H10O | |||
| IUPAC-naam | 4-fenyl-3-buten-2-on | |||
| Andere namen | benzalaceton, methylstyrylketon | |||
| Molmassa | 146,1858 g/mol | |||
| SMILES | CC(=O)C=CC1=CC=CC=C1
| |||
| InChI | 1S/C10H10O/c1-9(11)7-8-10-5-3-2-4-6-10/h2-8H,1H3/b8-7+
| |||
| CAS-nummer | 122-57-6 | |||
| PubChem | 637759 | |||
| Wikidata | Q4380955 | |||
| Beschrijving | Lichtgele kristallen | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H315 - H317 - H319 - H335 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P261 - P280 - P305+P351+P338 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | lichtgeel | |||
| Dichtheid | 1,008 g/cm³ | |||
| Smeltpunt | 39-42 °C | |||
| Kookpunt | 260-262 °C | |||
| Vlampunt | 116 °C | |||
| Oplosbaarheid in water | 1,3 g/L | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Benzylideenaceton is een organische verbinding met als brutoformule C10H10O. Hoewel in principe rond de dubbele binding cis-trans-isomerie kan bestaan, is alleen het trans-isomeer beschreven. De eerste beschrijving van deze verbinding, en zijn bereiding, in 1881, toonde duidelijk de mogelijkheden van de aldolcondensatie als manier om nieuwe koolstof-koolstofbindingen te maken.[1]
Synthese[bewerken | brontekst bewerken]
Een efficiënte synthese van benzylideenaceton gaat uit van de reactie tussen aceton en benzaldehyde, onder invloed van een milde base (natriumhydroxide):[2]
De reactie is een aldolcondensatie, gevolgd door de eliminatie van water. Als storend nevenproduct kan dibenzylideenaceton ontstaan. Door een grote overmaat van het (goedkope) aceton in te zetten wordt dit probleem ondervangen. Aceton is bovendien door zijn lage kookpunt makkelijk van de andere reactieproducten ter scheiden, bijvoorbeeld via destillatie of door middel van een draaiverdamper.
Eigenschappen en reacties[bewerken | brontekst bewerken]
In de verbinding is een grote verscheidenheid aan functionaliteiten aanwezig, waardoor tal van reacties mogelijk zijn:
- Dibroom addeert aan de dubbele binding
- Het heterodieen geeft diels-alderreacties met elektronrijke alkenen in de synthese van dihydropyranen
- De methylgroep reageert makkelijk met een volgende equivalent benzaldehyde, hetgeen aanleiding geeft tot de vorming van dibenzylideenaceton
- De carbonylfunctie kan omgezet worden in een hydrazon
- Met methylmagnesiumbromide wordt door een Grignard-reactie 1-fenyl-1,3-butadieen verkregen[3]
- Selectieve hydrogenering van de dubbele binding leidt tot de vorming van benzylaceton
Door reactie met lithiumbis(trimethylsilyl)amide (een sterke base) wordt het enolaat van benzylideenaceton verkregen, dat verder gefunctionaliseerd kan worden:[4]
Externe links[bewerken | brontekst bewerken]
- (en) MSDS van benzylideenaceton
- (en) Gegevens van benzylideenaceton in de GESTIS-stoffendatabank van het IFA
Bronnen, noten en/of referenties
|



