Ammoniumperchloraat
| Ammoniumperchloraat | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
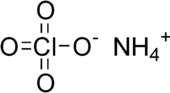
| ||||
Structuurformule van ammoniumperchloraat
| ||||

| ||||
Ammoniumperchloraat-kristallen
| ||||
| Algemeen | ||||
| Molecuulformule | NH4ClO4 | |||
| IUPAC-naam | ammoniumperchloraat | |||
| Molmassa | 117,48906 g/mol | |||
| SMILES | [NH4+].[O-]Cl(=O)(=O)=O
| |||
| InChI | 1S/ClHO4.H3N/c2-1(3,4)5;/h(H,2,3,4,5);1H3
| |||
| CAS-nummer | 7790-98-9 | |||
| Wikidata | Q410203 | |||
| Beschrijving | Wit kristallijn poeder | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H201 - H271 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P220 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit | |||
| Dichtheid | 1,95 g/cm³ | |||
| Oplosbaarheid in water | (bij 20°C) 234 g/L | |||
| Goed oplosbaar in | water, methanol | |||
| Matig oplosbaar in | aceton | |||
| Onoplosbaar in | di-ethylether | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Ammoniumperchloraat is een anorganische verbinding met als brutoformule NH4ClO4. Het is een zout van ammoniak en perchloorzuur. De stof komt voor als kleurloos tot wit kristallijn poeder, dat redelijk goed oplosbaar is in water. Net als andere perchloraten is het een krachtige oxidator, maar tegelijk bevat het een reducerend ammoniumion.
Synthese[bewerken | brontekst bewerken]
Op industriële schaal wordt ammoniumperchloraat bereid door elektrolyse in een zogenaamde perchloraatcel. Daartoe wordt natriumchloride (in waterige oplossing) geoxideerd tot natriumperchloraat. Vervolgens wordt dit met ammoniumchloride behandeld, zodat via een metathesereactie ammoniumperchloraat wordt gevormd:
Beide zouten bezitten een verschillende oplosbaarheid in water en kunnen daarom worden gescheiden. Het ontstane natriumchloride kan opnieuw worden gebruikt.
Eigenschappen[bewerken | brontekst bewerken]
Ammoniumperchloraat behoort tot de minder oplosbare ammoniumzouten: bij 20°C kan ongeveer 20 gram worden opgelost in 100 mL water. Bij verhitting boven 200°C ontleedt de verbinding en ontstaan chloor, stikstofgas, zuurstofgas en water:
Bovenstaande reactie is niet de enig mogelijke reactie bij ontleding. Er kan ook waterstofchloride vrij komen en er komen veelal ook kleine hoeveelheden van stikstofoxiden vrij.
Sterkere verhitting of de inwerking van sterke zuren kunnen leiden tot explosies, omdat het volume ingenomen door de grotendeels gasvormige producten veel groter is dan van de vaste stof waaruit zij ontstaan. Bovendien komt bij de ontleding een niet onaanzienlijke hoeveelheid warmte vrij.
In de PEPCON-ramp op 4 mei 1988 veroorzaakte een explosie in een ammoniumperchloraatfabriek een aardschok van 3,5 op de schaal van Richter.
Toepassingen[bewerken | brontekst bewerken]
Ammoniumperchloraat wordt toegepast in vastebrandstofmotoren zoals de hulpraketten van de Spaceshuttle en Space Launch System, modelraketten, vuurwerkraketten, ruimteraketten en raketten voor militaire doeleinden.
Toxicologie en veiligheid[bewerken | brontekst bewerken]
Ammoniumperchloraat kan ontbranden in contact met reductoren zoals zwavel en fosfor, metaalpoeder en organische verbindingen. Bij verbranding ontstaan giftige gassen. De stof irriteert de slijmvliezen, alsook de huid, ogen en het ademhalingsstelsel. Ammoniumperchloraat is toxisch voor het bloed en de nieren.
Externe links[bewerken | brontekst bewerken]
- (en) MSDS van ammoniumperchloraat
- (en) Gegevens van ammoniumperchloraat in de GESTIS-stoffendatabank van het IFA



