Onderfosforigzuur
| Onderfosforigzuur | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuurformule van onderfosforigzuur
| ||||
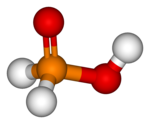
| ||||
Molecuulmodel van onderfosforigzuur
| ||||
| Algemeen | ||||
| Molecuulformule | H3PO2 | |||
| IUPAC-naam | fosfienzuur | |||
| Andere namen | hypofosforigzuur | |||
| Molmassa | 66,0 g/mol | |||
| SMILES | O=PO
| |||
| InChI | 1S/H3O2P/c1-3-2/h3H2,(H,1,2)
| |||
| CAS-nummer | 6303-21-5 | |||
| Wikidata | Q409658 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H314 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P280 - P305+P351+P338 - P310 | |||
| Hygroscopisch? | ja | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,493 g/cm³ | |||
| Smeltpunt | 26,5 °C | |||
| Kookpunt | (ontleedt) 130 °C | |||
| Goed oplosbaar in | ethanol, di-ethylether | |||
| Matig oplosbaar in | water | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Onderfosforigzuur of hypofosforigzuur is een anorganische verbinding met als brutoformule H3PO2. Het wordt ook wel aangeduid met de benaming fosfienzuur.
Synthese[bewerken | brontekst bewerken]
Onderfosforigzuur kan bereid worden door reactie van witte fosfor met water, in basisch milieu:
Een alternatief is de reactie van fosfine met di-jood:
Onderfosforigzuur kan ook in twee stappen verkregen worden. In de eerste stap wordt witte fosfor behandeld met een oplossing van bariumhydroxide, zodat bariumhypofosfiet ontstaat:
Daarna wordt zwavelzuur toegevoegd dat onderfosforigzuur verdrijft uit zijn bariumzout:
Het voordeel hierbij is dat bariumsulfaat neerslaat in de oplossing, zodat de opzuivering vlot verloopt.
Eigenschappen[bewerken | brontekst bewerken]
Onderfosforigzuur is een kleurloze hygroscopische kristallijne vaste stof met een smeltpunt van 26,5 °C. Na het smelten wordt een lichtgele vloeistof gevormd. De kristallen zijn matig in water oplosbaar. Deze oplossing is een eerder viskeuze kleurloze vloeistof met een karakteristieke zure geur. Onderfosforigzuur is een matig sterk zuur met een pKa van 1,2. Het vormt een H2PO2−-ion dat een tetraëdrische geometrie heeft en twee P-H-bindingen bevat. Het oxidatiegetal van fosfor is +I. De zouten van het zuur, de hypofosfieten, zijn in het algemeen goed oplosbaar, maar zijn bij verhitting niet erg stabiel en ontleden onder vorming van orthofosfaten, fosfine en waterstofgas.
Onderfosforigzuur en zijn zouten, zoals natriumhypofosfiet, zijn vrij sterke reductoren.
Toepassingen[bewerken | brontekst bewerken]
Een praktische toepassing van onderfosforigzuur is gelegen in de eigenschap dat bepaalde metaalzouten (zoals van nikkel en koper) ermee tot het metaal gereduceerd kunnen worden. Bij deze reactie wordt het onderfosforigzuur omgezet in fosforigzuur:
Met behulp van deze reactie kunnen metaallagen afgezet worden op niet-geleidende oppervlakken die niet langs elektrochemische weg bedekt kunnen worden, zoals glas, keramiek en polymeren.
Een andere toepassing is het diazoteren van diazoniumverbindingen.






