Prins-reactie
De Prins-reactie is een reactie uit de organische chemie tussen een carbonylverbinding (aldehyde of keton, 2 in het schema) en een onverzadigde koolwaterstofverbinding (alkeen of alkyn, 1) met een zuur als katalysator.

De Prins-reactie bestaat uit een elektrofiele additie gevolgd door de additie van een nucleofiel aan het gevormde intermediair product. Het uiteindelijke product hangt af van de reactieomstandigheden:
- in aanwezigheid van water en een zuur is het reactieproduct van een alkeen met formaldehyde een 1,3-diol (3)
- bij afwezigheid van water vindt dehydratie plaats tot het corresponderende allylalcohol 4[1].
- met een overmaat formaldehyde en bij lage reactietemperatuur is het product een dioxaan 5.
De Prins-reactie kan ook uitgevoerd worden in een carbonzuur als oplosmiddel; dan worden de overeenkomstige esters gevormd.
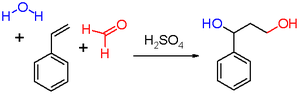
De Nederlandse scheikundige Hendrik Jacobus Prins beschreef de reactie voor het eerst in 1919 in een artikel in het Chemisch Weekblad[2]. Hij voerde de reactie uit met formaldehyde en styreen, pineen, kamfer, eugenol, isosafrol en amethol. De reactie met styreen is:
Reactiemechanisme[bewerken | brontekst bewerken]

- Het zuur protoneert de carbonylverbinding 2, zodat een oxonium-ion 3 ontstaat.
- Het alkeen 1 voert een elektrofiele additie hierop uit, waaruit een carbokation-intermediair 4 ontstaat. Dit carbokation kan op verschillende manieren verder reageren:
- zwart: eliminatie tot het allylalcohol 7
- blauw: met water of een ander geschikt nucleofiel wordt het intermediair ion 5 gevormd en ten slotte het diol 6
- groen: in een overmaat van de carbonylverbinding reageert het met een tweede carbonylverbinding tot het intermediair ion, waarin de positieve lading verdeeld is over zuurstof en koolstof in de resonantiestructuren 8 en 8b. Ringsluiting geeft via het intermediair 9 het dioxaan 10.
- grijs: enkel in zeer specifieke gevallen, en wanneer het carbokation zeer stabiel is, kan een oxetaan 12 ontstaan via het intermediair 11.
Toepassingen[bewerken | brontekst bewerken]
In 1937 werd de Prins-reactie van isobuteen met formaldehyde tot 4,4-dimethyl-1,3-dioxaan en 3-methyl-1,3-butaandiol gebruikt als onderdeel van de synthese van isopreen waarmee synthetisch rubber kan vervaardigd worden:

Een latere ontwikkeling hiervan is het "IFP-proces" (Institut Français du Pétrole)[3][4]. Isobuteen reageert met een overmaat formaldehyde tot de cyclische ether 4,4-dimethyl-1,3-dioxaan. De pyrolyse daarvan levert isopreen, water en formaldehyde, dat opnieuw kan ingezet worden[5].
De Prins-reactie wordt veel toegepast voor de synthese van aroma- en parfumstoffen[6]. Een voorbeeld is de intramoleculaire Prins-reactie van citronellal (citronellal is zowel een alkeen als een aldehyde) tot isopulegol[7].
De Prins-reactie vormt ook een stap in de totaalsynthese van een aantal natuurlijke stoffen, zoals in die van exiguolide :[8]

