Sonogashira-koppeling
De Sonogashira-koppeling is een organische reactie waarbij een terminaal alkyn en een aryl- of vinylhalogenide worden gekoppeld met behulp van een op palladium en koper gebaseerde katalysator:[1]
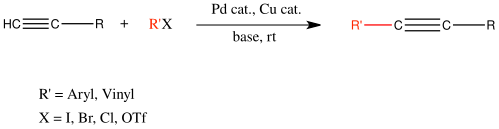
De reactie werd vernoemd naar de Japanse scheikundige Kenkichi Sonogashira, die de reactie in 1975 samen met Yasuo Tohda en Nobue Hagihara voor het eerst publiceerde.[2] De koppelingsreactie wordt toegepast in tal van onderzoeksdomeinen en bij de synthese van complexe verbindingen. Toepassingsdomeinen zijn onder andere de farmaceutische industrie (synthese van Tazaroteen en Altinicline), de synthese van natuurproducten, organische verbindingen en nanomaterialen.
De Sonogashira-koppeling is verwant met onder andere de Heck-reactie en de Suzuki-reactie.
Reactiemechanisme[bewerken | brontekst bewerken]

Het volledige mechanisme van de koppelingsreactie is nog niet volledig opgehelderd, maar ze blijkt te bestaan uit een palladiumgekatalyseerde cyclus en een kopergekatalyseerde cyclus. Deze laatste is het minst gekend.[3][4]
Palladiumcyclus[bewerken | brontekst bewerken]
De actieve katalystor op basis van palladium is de verbinding Pd0L2 (A) die via een oxidatieve additie complexeert met het aryl- of vinylhalogenide tot het intermediair palladium(II)complex (B). Aangenomen wordt dat deze stap de snelheidsbepalende stap van de reactie is.[4] Complex B ondergaat een transmetallatie met het koperacetylide (F), dat in de kopercyclus is gevormd, tot het palladiumacetylide (C). Zowel het aryl- of vinylligand als het alkynligand ondergaan een isomerisatie tot het complex D. De daaropvolgende reductieve eliminatie is de werkelijke koppeling van beide koolstoffragmenten. Het oorspronkelijke palladium(0)complex (A) wordt hervormd.
Kopercyclus[bewerken | brontekst bewerken]
De kopercyclus is minder goed begrepen dan de palladiumcyclus, maar aangenomen wordt dat uitgaande van het terminaal alkyn en een koperhalogenide (G) een intermediair pi-alkyncomplex met koper (E) wordt gevormd. Zodoende wordt de aciditeit van het waterstofatoom op de drievoudige binding verhoogd, zodat onder invloed van een milde organische base deprotonering en ligandvorming met koper optreedt tot het koperacetylide F.
Katalysatoren[bewerken | brontekst bewerken]
De tweede benodigde katalysatoren bij de koppelingsreactie zijn een palladium(0)katalysator en een koper(I)halogenide. Voorbeelden van palladiumcomplexen zijn fosfinecomplexen van het type Pd(PPh3)4. Daarnaast zijn ook bidentate katalysatoren bekend met 1,2-bis(difenylfosfino)ethaan, 1,3-bis(difenylfosfino)propaan en 1,1'-bis(difenylfosfino)ferroceen, met respectievelijke brutoformules Pd(dppe)Cl, Pd(dppp)Cl2 en Pd(dppf)Cl2. Echter, hieraan zijn enkele nadelen verbonden. Het belangrijkste nadeel is dat dergelijke palladium(0)complexen niet zo stabiel zijn. Daarom wordt meestal uitgegaan van de overeenkomstige palladium(II)verbinding. Vlak voor de reactie wordt de verbinding gereduceerd door complexering met een amine- of een fosfine-ligand.[5]
Als koper(I)verbinding wordt frequent koper(I)jodide aangewend. Daarnaast treedt de koper(I)verbinding ook op als co-katalysator om de reactiesnelheid te verhogen.[4]
Reactieomstandigheden[bewerken | brontekst bewerken]
De Sonogashira-koppeling verloopt onder relatief milde omstandigheden,[6] zoals bij kamertemperatuur en met een milde base (zoals di-ethylamine, DABCO of DMAP). Deze base kan eveneens dienstdoen als oplosmiddel, maar vaak worden andere oplosmiddelen aangewend, zoals dimethylformamide, di-ethylether of tolueen. De base dient niet alleen aanwezig te zijn om het pi-alkynkopercomplex te deprotoneren, maar eveneens om het gevormde waterstofhalogenide te neutraliseren. Soms worden andere basen, zoals kaliumcarbonaat of cesiumcarbonaat gebruikt. Aangezien het palladium(0)complex onstabiel is en onder invloed van lucht kan ontleden, dient de reactie onder inerte gasatmosfeer (stikstofgas of argon) plaats te grijpen.
Type substraat[bewerken | brontekst bewerken]
De reactiviteit van het substraat bepaalt in belangrijke mate de snelheid en het gemak waarmee de koppeling verloopt. De reactiviteitsvolgorde (van meest naar minst reactief) is hieronder voorgesteld:[3]

Daaruit blijkt dat vinylhalogeniden over het algemeen sneller reageren dan arylhalogeniden. Binnen beide groepen wordt nog de volgorde jodide, triflaat, bromide en chloride duidelijk.
