Fosfaan (stofklasse)


De fosfanen (soms ook wel fosfines genoemd, hoewel niet geheel correct conform de IUPAC-nomenclatuur) vormen een stofklasse van fosforverbindingen, structureel gezien afgeleid van fosfine, waarin trivalent fosfor voorkomt dat gebonden is aan waterstof, aan een ander fosforatoom en/of aan een alkyl- of arylgroep.
Er wordt globaal gezien een onderscheid gemaakt tussen organische en anorganische fosfanen. De organische fosfanen, zoals trifenylfosfine, omvatten de subklasse van organische fosforverbindingen waarin een trivalent fosforatoom gebonden is aan een organische restgroep. Anorganische fosfanen, zoals difosfaan, bezitten de algemene brutoformule PnHn+2 en bestaan dus uitsluitend uit fosfor en waterstof.
IUPAC-nomenclatuur[bewerken | brontekst bewerken]
De nomenclatuur volgens de IUPAC omtrent deze verbindingen is relatief ingewikkeld en niet eenduidig. De officiële benaming van de stofklasse is fosfanen, hoewel ook de term fosfines in zwang is.[1] Deze wordt gehanteerd om te duiden op de overeenkomst met de amines: organische fosfanen kunnen namelijk beschouwd worden als de fosforanaloga van amines. De IUPAC erkent echter wel de benaming fosfines, namelijk die groep van verbindingen waarin één of meerdere waterstofatomen in fosfine (PH3) is vervangen door een organische restgroep, maar stelt duidelijk dat de voorkeur wordt gegeven aan de benaming als een fosfaan.[2] Zo is de officiële IUPAC-naam van trifenylfosfine eigenlijk trifenylfosfaan, hoewel die eerste term dusdanig ingeburgerd is in de scheikundige literatuur, dat enkel deze gehanteerd wordt. Idem dito is de officiële aanduiding van de stamverbinding fosfine eigenlijk fosfaan. Ook die naam wordt weinig gebruikt in de courante literatuur.
Voor de anorganische fosfanen wordt enkel de voorkeur gegeven aan de benaming als fosfaan.[1]
Verbindingen afgeleid van PH5 worden aangeduid als fosforanen of (in delta-lambda-notatie) λ5-fosfanen.[3] Dit zijn hypervalente fosforverbindingen.
Organische fosfanen[bewerken | brontekst bewerken]
Structuur en reactiviteit[bewerken | brontekst bewerken]

De organische fosfanen, die vaak fosfines worden genoemd, zijn gebaseerd op de structuur van fosfine, maar waarbij één of meerdere van de waterstofatomen zijn vervangen door alkyl- of arylgroepen. Een voorbeeld is trifenylfosfine, dat 3 fenylgroepen bezit. Afhankelijk van de substitutiegraad wordt, net zoals bij amines, gesproken over primaire (PH2R), secundaire (PHR2) en tertiaire (PR3) fosfanen.
Het komt ook voor dat een alkylketen een brugstructuur vormt tussen twee fosforatomen, zoals bijvoorbeeld het geval is in bis(difenylfosfano)methaan.
Fosfor bezit een vrij elektronenpaar, hetgeen van belang is voor zijn reactiviteit. Daar waar fosfine zelf niet als nucleofiel kan optreden vanwege de aard van de binding tussen fosfor en waterstof, is de situatie geheel anders bij trifenylfosfine en andere trigesubstitueerde fosfanen. Die verbindingen kunnen vlot een SN2-reactie aangaan met halogeenalkanen, met vorming van het overeenkomstig quaternair fosfoniumzout. Een voorbeeld is de reactie van trifenylfosfine met methyljodide, waarbij trifenylmethylfosfoniumjodide ontstaat:
Dergelijke fosfoniumzouten zijn van bijzonder belang in de organische synthese: door ze met een sterke base te laten reageren, worden yliden gevormd, die een groot aantal toepassingen kennen bij onder andere de Wittig-reactie.
Nomenclatuur[bewerken | brontekst bewerken]
De organische fosfanen worden meestal als fosfine aangeduid. De naamgeving start met de benoeming van de organische zijketens, gevolgd door ofwel de benaming fosfaan ofwel fosfine. Dit hangt af van de mate waarin de benaming ingeburgerd is. Zo zal trifenylfosfine, dat veelvuldig gebruikt wordt in de organische synthese, zelden benoemd worden als trifenylfosfaan, hoewel dat de officiële IUPAC-benaming is.
Synthese[bewerken | brontekst bewerken]
Organische fosfanen kunnen bereid worden uit fosfine zelf of uit fosfortrichloride. Bij deze laatste worden door substituties de chlooratomen vervangen door organische zijketens.
Trimethylfosfine kan bereid worden door behandeling van fosfine met methylchloride:
Trifenylfosfine kan op laboratoriumschaal gesynthetiseerd worden door de reactie van fosfortrichloride met fenyllithium of een Grignard-reagens, zoals fenylmagnesiumbromide:
Eigenschappen[bewerken | brontekst bewerken]
Fosfanen met korte alkylgroepen, zoals trimethylfosfine, zijn typisch vloeistoffen met een zeer onaangename en indringende visachtige of knoflookachtige geur. Ze zijn zeer reactief en worden door de aanwezigheid van het beschikbare vrije elektronenpaar op fosfor gemakkelijk geoxideerd tot de overeenkomstige fosfineoxiden (vergelijkbaar met de amineoxiden):
De drijvende kracht voor deze reactie is de vorming van een zeer sterke binding tussen fosfor en zuurstof. De oxidatiegevoeligheid neemt af door de aanwezigheid van grotere of elektronenzuigende substituenten. Zo wordt trifenylfosfine, dat een witte geurloze vaste stof is, veel moeilijker geoxideerd. Het kan langere tijd aan de lucht blootgesteld bewaard worden. De aanwezigheid van fosfineoxiden kan eenvoudig worden aangetoond door het opmeten van een 31P-NMR-spectrum, waarbij naast de karakteristieke fosfaanresonantie ook een extra fosfineoxideresonantie zichtbaar is.
De basiciteit van de organische fosfanen neemt toe met toename van het aantal en de lengte van de alkylgroepen, in hogere mate dan het geval is bij de overeenkomstige amines. Zo bedraagt de pKb van fosfine ongeveer 27, terwijl die van tri-ethylfosfine 5,31 bedraagt.[4]
Anorganische fosfanen[bewerken | brontekst bewerken]



Structuur[bewerken | brontekst bewerken]
Anorganische fosfanen, die ook wel fosforhydriden worden genoemd, zijn opgebouwd zoals de alkanen: fosforatomen zijn via sigma-bindingen met elkaar verbonden en vormen het skelet van de verbinding, dat verzadigd is met waterstofatomen. Ze kunnen voorkomen in een lineaire vorm: er zijn fosfanen bekend met een lengte tot 6 fosforatomen (hexafosfaan). Aangezien fosfor - anders dan koolstof in alkanen - een vrij elektronenpaar bezit, herleid de algemene brutoformule van anorganische lineaire fosfanen zich tot PnHn+2. Net zoals bij alkanen kunnen fosfanen ook voorkomen in cyclische vorm. Ook kooiachtige structuren zijn bekend, hoewel deze een stuk onstabieler zijn.
Nomenclatuur[bewerken | brontekst bewerken]
De anorganische fosfanen worden benoemd via een Grieks telwoord, dat aangeeft hoeveel fosforatomen in de verbinding voorkomen, gevolgd door de benaming fosfaan en tussen haakjes het aantal waterstofatomen. Zo wordt P4H6 betiteld als tetrafosfaan(6), omdat het 4 fosforatomen en 6 waterstofatomen bevat.
Synthese[bewerken | brontekst bewerken]
Fosfine[bewerken | brontekst bewerken]
Fosfine is de stamverbinding van de anorganische fosfanen en kan op verschillende manieren bereid worden. De industriële syntheseroute gaat uit van witte fosfor, die in reactie gebracht wordt met natriumhydroxide. Daarbij ontstaat natriumhypofosfiet en natriumfosfiet als nevenproduct. Het ontstane natriumhypofosfiet ontleedt bij verhitting tot natriumwaterstoffosfaat en fosfine:
Een alternatieve methode is de zuur-gekatalyseerde disproportionering van witte fosfor, waarbij fosforzuur en fosfine ontstaan. Deze methode wordt meestal verkozen wanneer uit het ontstane fosfine verdere gesubstitueerde fosfines dienen bereid te worden. Het nadeel is echter dat veel moet opgezuiverd worden en dat het proces onder verhoogde druk verloopt.
In het laboratorium kan het op kleine schaal bereid worden door de hydrolyse van een metaalfosfide, zoals calciumfosfide of aluminiumfosfide:
Met calciumfosfide ontstaat echter een grotere hoeveelheid difosfaan.
Hoogzuiver fosfine, vrij van difosfaan, kan bereid worden door de inwerking van kaliumhydroxide op fosfoniumjodide:[5]
Analoog aan het Haber-Boschproces voor de productie van ammoniak kan fosfine bereid worden door witte fosfor in reactie te brengen met waterstofgas:
Difosfaan[bewerken | brontekst bewerken]
Difosfaan ontstaat tijdens de hydrolyse van calciummonofosfide.[6]
Eigenschappen[bewerken | brontekst bewerken]
De anorganische fosfanen staan bekend als extreem giftige verbindingen. Zo is fosfine een dodelijk gas. Difosfaan komt bij kamertemperatuur voor als een kleurloze en pyrofore vloeistof, die spontaan explodeert bij contact met de lucht. Fosfine kan bij 150°C geoxideerd worden tot fosforzuur met behulp van zuurstofgas:
Daarbij komt een zeer grote hoeveelheid energie vrij (1270 kJ).
Fosfanen zijn typische reductoren en zeer reactief. Zuiver fosfine is relatief onschadelijk, maar omdat het vaak gecontamineerd is met difosfaan (afkomstig van het productieproces of van spontane dimerisatie), kan het gas spontaan ontbranden. Alle fosfanen hebben een indringende, typische knoflookachtige geur, die reeds bij zeer lage concentraties waarneembaar is.
Toepassingen[bewerken | brontekst bewerken]
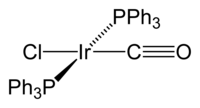
Organische fosfanen worden in de organometaalchemie toegepast als stabiliserende liganden voor overgangsmetalen. Vooral trifenylfosfine wordt vaak gebruikt, omdat het een makkelijk te hanteren vaste stof is, die weinig schadelijk en daarenboven weinig oxidatiegevoelig is. De gevormde complexen, zoals met palladium, worden gebruikt bij homogene katalyse van diverse reacties. Chirale fosfanen, zoals DuPhos of DIPAMP, doen dienst als liganden voor enantioselectieve katalysatoren in de asymmetrische synthese van verbindingen.
Daarnaast worden organische fosfanen toegepast als reagens bij verschillende organische reacties, waaronder de Appel-reactie, de Mitsunobu-reactie, de Staudinger-reactie en de Wittig-reactie. Bij deze reacties wordt telkens gebruikgemaakt van de oxofilie van fosfor.
Fosfine wordt gebruikt als doteermiddel in de halfgeleiderindustrie (onder andere van silicium) en kan als reductor ingezet worden. Een belangrijke toepassing hiervan is de reductie van nikkelionen uit waterige oplossing tot een fosforhoudende nikkellaag die goed kan hechten aan geprofileerde oppervlakken.
Trimethylfosfine wordt gebruikt om selectief de ketonfunctie in een α-keto-ester te reduceren tot een hydroxylgroep:

Zie ook[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|

![{\displaystyle \mathrm {P(C_{6}H_{5})_{3}\ +\ CH_{3}I\ \longrightarrow \ [P(C_{6}H_{5})_{3}CH_{3}]^{+}\ +\ I^{-}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/7d43921d94780344d395067680053bd34e31d0b9)







