Piperazine
| Piperazine | ||||||
|---|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||||

| ||||||
Structuurformule van piperazine
| ||||||
| Algemeen | ||||||
| Molecuulformule | C4H10N2 | |||||
| IUPAC-naam | piperazine | |||||
| Andere namen | 1,4-diazacyclohexaan, 1,4-di-ethyleendiamine, hexahydropirazine, hexahydro-1,4-diazine | |||||
| Molmassa | 86,1356 g/mol | |||||
| SMILES | C1CNCCN1
| |||||
| InChI | 1S/C4H10N2/c1-2-6-4-3-5-1/h5-6H,1-4H2
| |||||
| CAS-nummer | 110-85-0 | |||||
| EG-nummer | 203-808-3 | |||||
| PubChem | 4837 | |||||
| Wikidata | Q409292 | |||||
| Waarschuwingen en veiligheidsmaatregelen | ||||||
| ||||||
| H-zinnen | H314 - H317 - H334 - H361 | |||||
| EUH-zinnen | geen | |||||
| P-zinnen | P261 - P280 - P305+P351+P338 - P310 | |||||
| Hygroscopisch? | ja | |||||
| EG-Index-nummer | 612-057-00-4 | |||||
| VN-nummer | 2579 | |||||
| Fysische eigenschappen | ||||||
| Aggregatietoestand | vast | |||||
| Kleur | wit | |||||
| Dichtheid | 1,1 g/cm³ | |||||
| Smeltpunt | 106 °C | |||||
| Kookpunt | 146 °C | |||||
| Vlampunt | 65 °C | |||||
| Zelfontbrandings- temperatuur | 320 °C | |||||
| Dampdruk | (bij 20°C) 21 Pa | |||||
| Oplosbaarheid in water | (bij 20°C) 150 g/L | |||||
| Onoplosbaar in | di-ethylether, ethanol | |||||
| Evenwichtsconstante(n) | pKa = 9,8 | |||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||||
| ||||||
Piperazine is heterocyclische verbinding met als brutoformule C4H10N2. De stof komt in watervrije toestand voor als een kleurloze kristallijne vaste stof met een scherpe geur. De waterige oplossing ervan gedraagt zich als een matig sterke base.
Piperazine stof is sterk hygroscopisch en absorbeert water uit de lucht. Daarbij wordt het hexahydraat gevormd. Dit hexahydraat, alsook de zouten, zoals piperazinecitraat, zijn aanzienlijk stabieler dan watervrij piperazine.
Synthese[bewerken | brontekst bewerken]
Er bestaan tal van synthesemethoden voor piperazine. Het wordt gevormd door reactie van 1,2-dibroomethaan met ammoniak in ethanol:
In plaats van 1,2-dibroomethaan kan ook 1,2-dichloorethaan gebruikt worden. Dit wordt onder meer gedaan bij de industriële productie van piperazine.
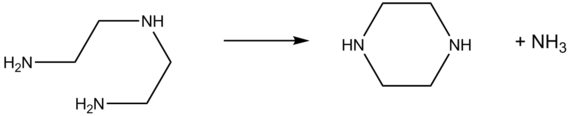
Piperazine wordt gevormd wanneer gasvormig ethyleendiamine bij hoge temperatuur over een katalysator wordt geleid:[1][2]
In plaats van ethyleendiamine kan ook di-ethyleentriamine aangewend worden:
Toepassingen[bewerken | brontekst bewerken]
Piperazine (vooral onder de vorm van het stabiele zout piperazinecitraat) wordt in de (dier)geneeskunde gebruikt als anthelminthicum (wormafdrijvend middel), om parasitaire wormen uit het maag-darmstelsel te verdrijven.
Piperazine is een belangrijke grondstof in de farmaceutische nijverheid. Het wordt gebruikt in de synthese van vele farmaceutische stoffen, waaronder imatinib, sildenafil en olanzapine, maar ook van hallucinogene en stimulerende middelen zoals BZP (benzylpiperazine).
Piperazinederivaten worden ook gebruikt voor bepaalde polyesters. Piperazinefosfaten en –pyrofosfaten worden gebruikt als vlamvertragers in polymeren.[3][4]
Toxicologie en veiligheid[bewerken | brontekst bewerken]
Piperazine is brandbaar en vormt bij verbranding giftige of corrosieve gassen (onder meer stikstofoxiden, koolstofmonoxide en koolstofdioxide).
Piperazine is corrosief voor de ogen, de huid en de luchtwegen. Inslikken of inademing ervan kan longoedeem veroorzaken (de symptomen worden vaak pas na enkele uren merkbaar). De stof kan effecten hebben op het zenuwstelsel en (bij inslikken van een grote dosis) bewusteloosheid veroorzaken.
Herhaald of langdurig contact kan de huid overgevoelig maken en allergische reacties uitlokken. Herhaalde of langdurige inademing van piperazine kan astma veroorzaken.
In Nederland en België gelden volgende grenswaarden voor blootstelling aan piperazine:[5][6]
- 0,1 mg/m³ als tijdgewogen gemiddelde over 8 uur
- 0,3 mg/m³ als tijdgewogen gemiddelde over 15 minuten
Externe links[bewerken | brontekst bewerken]
 piperazine - International Chemical Safety Card
piperazine - International Chemical Safety Card- (en) Gegevens van piperazine in de GESTIS-stoffendatabank van het IFA
- (en) MSDS van piperazine