Oxoanion
Een oxoanion is een anion van het type AxOyz-, waarbij A voor een willekeurig chemisch element staat en O zuurstof voorstelt.[1] Een groot aantal chemische elementen vormt oxoanionen. De oxoanionen kunnen worden ingedeeld naargelang hun structuur en samenstelling. Grofweg wordt een onderscheid gemaakt tussen monomere en polymere oxoanionen.
Monomere oxoanionen[bewerken | brontekst bewerken]
Monomere oxo-anionen worden gevormd door een covalente binding van een centraal element met omringende zuurstofatomen. Het aantal zuurstofatomen en de lading van het anion worden bepaald door de oxidatietoestand van het centraal element en de positie ervan in het periodiek systeem. Zo zijn elementen uit de tweede periode beperkt tot een maximaal coördinatiegetal van 4. Echter, geen van deze elementen vormt oxoanionen met zo'n hoog coördinatiegetal. Meer voorkomend is het coördinatiegetal 3, zoals in carbonaat (CO32−) en nitraat (NO3−). Beide oxoanionen (respectievelijk met koolstof en stikstof als centraal element) bezitten een trigonaal planaire structuur.
Elementen van de derde periode zijn veel flexibeler bij het vormen van oxoanionen en ze komen ook voor in polymere vormen. Wanneer het betrokken element zijn meest voorkomende oxidatietoestand bezit, worden tetraëdrische oxoanionen gevormd. Voor silicium, fosfor, zwavel en chloor zijn dat respectievelijk silicaat (SiO44−), fosfaat (PO43−), sulfaat (SO42−) en perchloraat (ClO4−). Deze oxoanionen komen in talloze zouten voor en worden ook in de natuur aangetroffen in minerale vorm. Lagere oxidatietoestanden van het centraal element leiden tot andere oxoanionen, zoals bijvoorbeeld bij chloor:
| Oxidatietoestand | +1 | +3 | +5 | +7 |
|---|---|---|---|---|
| Benaming | hypochloriet | chloriet | chloraat | perchloraat |
| Brutoformule | ClO− | ClO2− | ClO3− | ClO4− |
| Molecuulmodel | 
|

|

|

|
| Moleculaire geometrie | lineair | gebogen | trigonaal piramidaal | tetraëdrisch |
De moleculaire geometrie wijzigt met een veranderde oxidatietoestand. Dit is een gevolg van het feit dat met toenemend oxidatiegetal het aantal vrije elektronenparen afneemt. Deze observatie is in overeenstemming met hetgeen voorspeld wordt door de VSEPR-theorie.
Nomenclatuur[bewerken | brontekst bewerken]
De oxoanionen krijgen ieder een eigen naam, waarbij een suffix de oxidatietoestand van het centraal element aangeeft. Bij de nomenclatuur wordt een onderscheid gemaakt tussen de halogenen en de andere elementen:
Halogeen-oxoanionen[bewerken | brontekst bewerken]
| Oxidatiegetal centraal atoom | Prefix | Suffix | Voorbeelden |
|---|---|---|---|
| +VII | per- | -aat | perchloraat, perbromaat, perjodaat |
| +V | − | -aat | chloraat, bromaat, jodaat |
| +III | − | -iet | chloriet, bromiet, jodiet |
| +I | hypo- | -iet | hypofluoriet, hypochloriet, hypobromiet, hypojodiet |
Niet-halogeen-oxoanionen[bewerken | brontekst bewerken]
| Oxidatiegetal centraal atoom | Prefix | Suffix | Voorbeelden |
|---|---|---|---|
| = groepsnummer | − | -aat | boraat, carbonaat, nitraat, fosfaat, sulfaat, chromaat, arsenaat, selenaat, molybdaat, orthowolframaat, vanadaat, manganaat |
| = groepsnummer − 2 | − | -iet | nitriet, fosfiet, sulfiet, arseniet, seleniet, telluriet |
| = groepsnummer − 4 | hypo- | -iet | hypofosfiet, hyposulfiet |
Een uitzondering op deze regels vormen permanganaat, perrenaat en pertechnetaat. Het voorvoegsel per- verwijst hier naar het feit dat de betrokken metalen zich in hun hoogste oxidatietoestand (namelijk +VII) bevinden.
Polymere oxoanionen[bewerken | brontekst bewerken]
Verscheidene transitiemetalen - en ook enkele niet-metalen (met name fosfor en zwavel) - vormen polymere oxoanionen.[2] Hierbij treedt een zuurstofatoom op als een brugvormend ligand tussen de metaalcentra, zoals in het dichromaat-, pyrofosfaat- en pyrosulfaat-anion. Wanneer dit herhaaldelijk gebeurt, kunnen ketens of ringstructuren ontstaan. Voorbeelden van dit soort structuren zijn polyfosfaten en inosilicaten. Een extreem voorbeeld in de kristallografie vormen de tectosilicaten (zoals kwarts), waarbij silicium in een zuurstofnetwerk zit ingebouwd. De vier omringende zuurstofatomen dienen hier als brugvormend ligand. Metavanadaten vormen lange ketenstructuren, zoals in ammoniummetavanadaat. De coördinatiestructuur rondom vanadium is tetraëdrisch.
 |
 |
Ringstructuren kunnen gezien worden als polyoxoanionketens waarvan de uiteinden met elkaar zijn verbonden. Cyclisch trifosfaat (P3O93−) is hiervan een voorbeeld.
Bij grotere transitiemetalen komen octaëdrische oxoanionen voor. Deze kunnen als monomere vorm voorkomen, maar de polymere driedimensionale clusters - polyoxometalaten genoemd - zijn meer voorkomend. Deze clusters kunnen opgevat worden als bestaande uit octaëdrische bouwstenen met gemeenschappelijke zijden. De vorming van gemeenschappelijke zijden heeft twee voordelen: ten eerste wordt de brugspanning, veroorzaakt door de brugvormende zuurstofatomen, gereduceerd en ten tweede wordt de ladingsdichtheid van het anion verlaagd. Een typisch voorbeeld is het polymolybdaat-anion. De vorming van polyoxometalaten kan beschouwd worden als een hypothetische condensatiereactie van de monomere oxoanionen:
Zo leidt het aanzuren van een waterige oplossing van molybdaat-anionen tot vorming van polymolybdaten:
Een vergelijkbare reactie treedt op met waterige oplossingen van wolframaten. Wanneer een oplossing van natriumwolframaat wordt behandeld met waterstofchloride, slaan de gele polywolframaten neer.
Condensatie- en hydrolysereacties[bewerken | brontekst bewerken]
Oxoanionen met een relatief hoge lading (of hoge ladingsdichtheid) ondergaan in waterige oplossing vlot condensatiereacties. Veelal worden die reacties beheerst door toevoeging van zuren of basen, zoals het evenwicht tussen het chromaat- en dichromaat-anion:
De drijvende kracht van deze reactie is de reductie van de ladingsdensiteit op het dichromaat-anion en de verwijdering van het harde proton. De reactie is een voorbeeld van een zuur-basereactie waarbij het monomere oxoanion fungeert als base en het gecondenseerde oxoanion als geconjugeerd zuur.
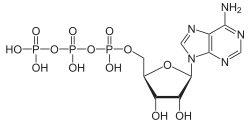
De tegenovergestelde reactie wordt ook waargenomen, namelijk de hydrolyse van polymere oxoanionen tot kleinere fragmenten. Een belangrijk voorbeeld in de biochemie is de hydrolyse van adenosinetrifosfaat (ATP) tot kleinere bouwstenen (adenosinedifosfaat en fosfaat), waarbij een aanzienlijke hoeveelheid energie (29,4 kJ/mol) vrijkomt. Bovendien stijgt de entropie na hydrolyse (wegens vorming van meer deeltjes) en kan de negatieve lading op zuurstof gestabiliseerd worden door resonantie. Adenosinedifosfaat kan nog verder gehydrolyseerd worden tot adenosinemonofosfaat (AMP), waarbij wederom 29,4 kJ/mol vrijkomt. De vrijgekomen energie kan aangewend worden voor het katalyseren van andere chemische reacties in het metabolisme die een hoge activeringsenergie hebben, bijvoorbeeld voor de synthese van organische moleculen, of voor actief transport van stoffen over het celmembraan via ionkanalen, bijvoorbeeld voor het opbouwen van een celpotentiaal.
Zuur-base-eigenschappen[bewerken | brontekst bewerken]
De meeste oxoanionen zijn zwakke basen die vrij vlot kunnen geprotoneerd worden tot de overeenkomstige zuren of zure zouten. Zo kan het fosfaat-anion in opeenvolgende stappen geprotoneerd worden tot fosforzuur:
De mate waarin deze reacties doorgaan wordt bepaald door de dissociatieconstanten (pKa) en de pH. Adenosinemonofosfaat bezit een pKa-waarde van 6,21 en zal dus bij pH 7 voor 10% geprotoneerd zijn. Een belangrijke drijvende kracht bij deze reacties is de neutralisering van de lading. Daartegenover staan oxoanionen zoals perchloraat en permanganaat die bijzonder moeilijk te protoneren zijn, zelfs niet met sterke zuren zoals zwavelzuur.
Zie ook[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|




