Sorbitol
| D-Sorbitol | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
Structuur van sorbitol
| ||||
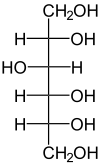
| ||||
Fischerprojectie van D-sorbitol
| ||||
| Algemeen | ||||
| Molecuulformule | C6H14O6 | |||
| IUPAC-naam | (2R,3R,4R,5S)-hexaan-1,2,3,4,5,6-hexol | |||
| Andere namen | D-glucitol, D-gulitol, E420 | |||
| Molmassa | 182,17176 g/mol | |||
| SMILES | C([C@H]([C@H]([C@@H]([C@H](CO)O)O)O)O)O
| |||
| InChI | 1/C6H14O6/c7-1-3(9)5(11)6(12)4(10)2-8/h3-12H,1-2H2/t3-,4+,5-,6-/m1/s1
| |||
| CAS-nummer | 50-70-4 | |||
| EG-nummer | 200-061-5 | |||
| PubChem | 5780 | |||
| Wikidata | Q245280 | |||
| LD50 (ratten) | (oraal) 15900[1] mg/kg | |||
| LD50 (muizen) | (oraal) 17800[1] mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit | |||
| Dichtheid | 1,49[2] g/cm³ | |||
| Smeltpunt | 94-96[2] °C | |||
| Kookpunt | 245 °C | |||
| Vlampunt | > 100[2] °C | |||
| Zelfontbrandings- temperatuur | 420[2] °C | |||
| Oplosbaarheid in water | 2350[2] g/L | |||
| Goed oplosbaar in | water, warme ethanol | |||
| Slecht oplosbaar in | de meeste organische oplosmiddelen | |||
| log(Pow) | −2,2[3] | |||
| Brekingsindex | 1,45831[4] | |||
| Nutritionele eigenschappen | ||||
| Type additief | stabilisator, vulmiddel, kunstmatige zoetstof | |||
| E-nummer | E420 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
D-Sorbitol of D-glucitol (E420) is een suikervervanger, waarbij de aldehydegroep vervangen is door een hydroxylgroep. Het is eigenlijk geen sacharide maar een polyalcohol: de gehydrogeneerde versie van sorbose.
Voorkomen[bewerken | brontekst bewerken]
D-sorbitol komt onder meer voor in de bessen van de wilde lijsterbes, waaruit het voor het eerst geïsoleerd werd.[5] Het komt ook voor in andere bessen (maar niet in druiven), kersen, pruimen, peren, appels, zeewier en algen.[4]
Synthese[bewerken | brontekst bewerken]
Sorbitol wordt bereid uit glucose via hydrogenering onder hoge druk[6] of elektrolytische reductie[7] of via katalytische hydrogenering.[8]
Toepassingen[bewerken | brontekst bewerken]
Sorbitol wordt veel gebruikt als zoetstof in lightproducten, suikervrije diëten en kauwgom. Het heeft een energetische waarde die een derde minder is dan gewone suiker, terwijl het de helft minder zoet is. Omwille van dit laag zoetend vermogen wordt er relatief veel toegevoegd om eenzelfde zoetkracht als 'normaal' te verkrijgen (bijvoorbeeld vergeleken met sacharose). Door deze grote hoeveelheden is het niet aangewezen voor diabetici, in tegenstelling tot wat men jarenlang verondersteld heeft. Een alternatief kan xylitol zijn, wat een groter zoetend vermogen heeft, maar in hoge doses aanleiding kan geven tot diarree en winderigheid.
Druiven bevatten geen sorbitol. Dit kenmerk van druiven kan worden gebruikt om wijn te onderscheiden van cider en andere vruchtenwijnen.
Sorbitol wordt ook gebruikt als vochtvasthoudend middel in tandpasta en cosmetica. Sorbitol heeft in bepaalde hoeveelheden een laxerend effect.
Sorbitol wordt beschouwd als een potentieel sleutelintermediair voor de synthese van alkanen[9] uit biomassa. Volledige reductie van sorbitol kan leiden tot alkanen zoals hexaan, die gebruikt kunnen worden als biobrandstof. De waterstof die nodig is voor deze transformatie komt grotendeels van sorbitol zelf, maar er komt dan wel CO2 vrij :
Deze reactie is exotherm en levert 1 mol hexaan uit 1,5 mol sorbitol. Bij toevoeging van waterstofgas komt geen koolstofdioxide vrij.
De dehydratie van sorbitol levert sorbitaan, waarmee niet-ionische oppervlakte-actieve stoffen gevormd worden door verestering met vetzuren, en emulgatoren zoals Polysorbaat 20, die ook in voedingsmiddelen mogen gebruikt worden.
Bronnen, noten en/of referenties
|

