Stabiel carbeen

Een stabiel carbeen is in tegenstelling tot de al langer bekende carbenen een deeltje dat een zodanig grote halfwaardetijd heeft dat directe observatie ervan mogelijk is. Van sommige van deze deeltjes is de stabiliteit zelfs zo groot dat ze thermodynamisch stabiel zijn.
Een algemeen kenmerk van stabiele carbenen is dat het carbeencetrum meestal geflankeerd wordt door twee atomen die over vrije elektronenparen beschikken, zoals stikstof, zuurstof, zwavel of fosfor.
Geschiedenis[bewerken | brontekst bewerken]
Vroege aanwijzingen[bewerken | brontekst bewerken]
In 1957 stelde Breslow voor dat een relatief stabiel nucleofiel carbeen, een thiazool-2-ylideen-derivaat, betrokken zou kunnen zijn bij de katalytische cyclus van vitamine B1 (thiamine) in de reactie van furfural naar furoine.[1] [2] In deze cyclus wordt een waterstofatoom van de thiazoliumring van het C2-atoom overgedragen aan een furfural-molecuul. Dat dit waterstof-atoom niet erg sterk gebonden is blijkt wanneer een thiazoliumzout wordt opgelost in gedeuteerd water: er stelt zich in snel een evenwicht in,.[3]
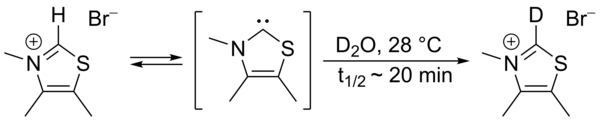
Deze uitwisseling werd verondersteld te verlopen via een thiazool-2-ylideen als intermediair. In 2012 is de isolatie van het, inmiddels als Breslow intermediair te boek staande deeltje, gerapporteerd.[4][5]
In 1960 deden Wanzlick en zijn groep experimenten waaruit zij concludeerden dat carbeen-derivaten van het type dihydroimidazool-2-ylideen ontstonden tijdens de vacuum pyrolyse van de overeenkomende 2-trichloormethyl-verbindingen onder uitstoting van een molecuul chloroform ().[6][7][8] Een andere conclusie was dat het genoemde carbeen in evenwicht, het Wanzlick evenwicht, was met zijn dimeer, een derivaat van tetra-aminoetheen. In 1964 werd door de researchgroep rond Lemal[9] en in 1965 door die rond Winberg[10] bewijs aangevoerd dat het dimeer niet dissocieerde. Tegenwoordig (2012) wordt geaccepteerd dat het evenwicht, zij het onder specifieke condities, inderdaad bestaat.[11][12]
Isolatie van stabiele carbenen[bewerken | brontekst bewerken]
In 1970 lukte het Wanzlick's groep imidazool-2-ylidene carbenen te maken door het deprotoneren van een imidazoliumzout.[13] Deze (toen) nieuwe groep verbindingen kreeg de naam: N-Heterocyclische Carbenen, afgekort als NHC's. Wanzlick, en ook Roald Hoffmann,[8][14] veronderstelden dat de imidazool-carbenen stabieler zouden zijn dan de 4,5-dihydro-analoge verbindingen, dit op basis van de in de imidazool-ring aanwezige Hückel-achtige aromaticiteit. De door Wanzlick geïsoleerde producten waren echter complexen van overgangsmetalen zoals kwik of met liganden als isothiocyanaat:
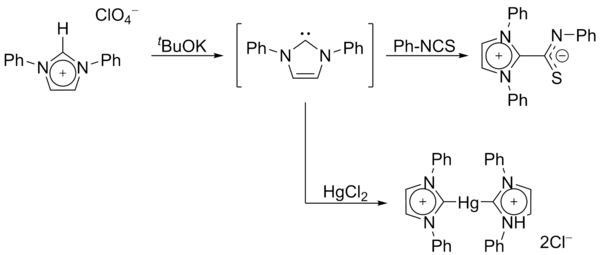
In 1988 werd door Bertrand en zijn groep een fosfinocarbeen geïsoleerd. Deze groep stoffen kan zowel als een λ3-fosfinocarbeen (zie "a" hieronder) of als een λ5-fosfa-acetyleen ("c") beschreven worden:[15][16]

Deze groep carbenen wordt aangeduid met de term "push-pull" (duw en trek) carbenen naar aanleiding van de tegengestelde elektron-affiniteiten van de twee substitueten. De reactiviteit van de stoffen bevat zowel elementen van de carbeen- als de alkyn-chemie. Van deze stoffen zijn nog geen gegevens uit de Röntgendiffractie bekend (2012) waardoor nog steeds enige controverse bestaat over het carbeenkarakter van de stoffen.
In 1991 verkregen Arduengo etal een kristalliseerbaar diaminocarbeen door een imidazolium-kation te deprotoneren:[17]

Dit carbeen, het eerste van een grote groep carbenen met een imidazool-kern, is bij kamertemperatuur onbeperkt stabiel (bij afwezigheid van zuurstof en vocht). Het heeft, zonder te ontleden, een smeltpunt van 240-241 °C. In zijn 13C-NMR is voor het carbeen-koolstofatoom een duidelijk herkenbaar signaal bij 211 ppm. aanwezig.[18] Uit de röntgendiffractiegegevens blijkt de koolstof-stikstofband in de ring duidelijk langer is dan in de uitgangsstof, een indicatie dat er weinig dubbele band-karakter in deze binding aanwezig is.[19]
Het eerste carbeen dat in lucht (zuurstof en vocht) stabiel is werd in 1997 gerapporteerd, een gechloreerd imidazool carbeen.[20]
In 2000 werd door Bertrand etal en serie nieuwe carbenen van het fosfanyltype beschreven, waaronder een (fosfanyl)(trifluormethyl)carbeen, dat in oplossing bij -30 °C stabiel bleek te zijn,[21] én een matig stabiel (amino)(aryl)-carbeen met slechts één hetero-atoom direct aan het carbeen-koolstofatoom.[22][23]
Factoren die de stabiliteit beïnvloeden[bewerken | brontekst bewerken]
Ter verklaring van de stabiliteit van deze carbenen in vergelijking met de al eerder bekende leden van deze stofgroep werden de volgende punten aangevoerd:
- Sterische hindering rond het carbeen-centrum.
- Deename van het carbeen-centrum aan een aromatisch systeem.
- Plaatsing van het carbeen-centrum in een cyclisch systeem.
- De aanwezigheid van twee stikstof-atomen direct aan het carbeen-centrum.
Sterische hindering[bewerken | brontekst bewerken]

De stabiliteit van de door Arduengo beschreven carbenen werd in eerst instantie toegeschreven aan de ruimtelijk veeleisende N-adamantyl-groepen die het carbeen door sterische hindering verhinderen te dimeriseren. Vervangen echter van de N-adamantylgroepen door methylgroepen leverde ook stabiele carbenen op.[25] De conclusie is dat imidazool-2-ylidenen thermodynamisch stabiel zijn.
Aromaticiteit[bewerken | brontekst bewerken]
Een tweede punt dat werd aangevoerd om de stabiliteit van deze carbenen te verklaren was de aromaticiteit van de imidazool-ring. Hiervoor is de dubbele band tussen de koolstof-atomen van de ring cruciaal. Ook dit punt bleek niet correct. Arduengo's groep kon in 1995 een derivaat van dihydroimidazool-2-ylidene, dus zonder de dubbele band tussen de atomen 4 en 5 van de ring - en daarmee dus ook zonder aromaticiteit, isoleren.[26] De blokkade voor dimerisatie bij deze stof en de relatieve rol die thermodynamische stabiliteit en sterische hindering daarin spelen is nog en onderwerp van discussie.[27][28]

Ringsysteem[bewerken | brontekst bewerken]
Het eerste gerapporteerde acyclische stabiele carbeen werd in 1996 beschreven,[29] daarmee ook de ringstructuur als stabiliserende factor afwijzend. In tegenstelling tot de cyclische carbenen zijn de acyclische derivaten flexibel: zij kunnen roteren om de banden van het carbeen-atoom. Door de grootte van de rotatiebarriere van deze bindingen te meten kon de mate van dubbele bandkarakter hierin bepaald worden. Net als de cyclische diaminocarbenen zijn de sterisch ongehinderde acyclische varianten gevoelig voor dimerisatie.[28][30][31]
Stikstof-atomen[bewerken | brontekst bewerken]
De meest estabiele carbenen worden gestabileseerd door twee stikstof-atomen naast het carbeen-centrum. Aminothiocarbenen[32] en aminooxycarbenen[33] zijn buitenbeentjes. In deze verbindingen ligt het carbeen-centrum tussen een stikstof en een zwavel- of zuurstof-atoom:
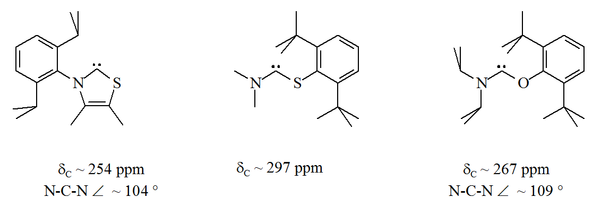
In tegenstelling tot de analoge NHC's zijn deze carbenen niet thermodynamisch stabiel, maar hebben de neiging te dimeriseren.
In Bis(di-iso-propylamino)cyclopropenylideen, dat bij kamertemperatuur stabiel is, is het carbeen-centrum gekoppeld aan twee koolstofatomen in een driering die de geometrie en de aromaticiteit van de cyclopropenylring behouden heeft. Dit voorbeeld illustreert dat ook de aanwezigheid van hetero-atomen geen noodzakelijke voorwaarde is voor stabiele carbenen.[35]
Soorten stabiele carbenen[bewerken | brontekst bewerken]
Hieronder volgt een aantal tot nu (2012)[36] toe gevonden soorten stabiele carbenen.
Imidazool-2-ylidenen[bewerken | brontekst bewerken]
De eerste geïsoleerde stabiele carbenen waren allemaal op basis van de imidazoolring, waarbij het waterstof-atoom op de 2-plaats (tussen de twee stikstofatomen) was verwijderd en de andere waterstofatomen door verscheidene groepen vervangen waren. Deze imidazool-2-ylidenen zijn nog steeds de meest stabiele en de best onderzochte en begrepen groep in de stabiele carbenen.
Een uitgebreid scala van derivaten van imidazool-2-ylideen is inmiddels gesynthetiseerd, inclusief die waarbij de 1 en de 3 posities (de stikstofatomen) groepen dragen als alkyl, aryl,[25] alkoxy, alkylamino, alkylfosfino[37] en zelfs met chirale substituenten:[37]
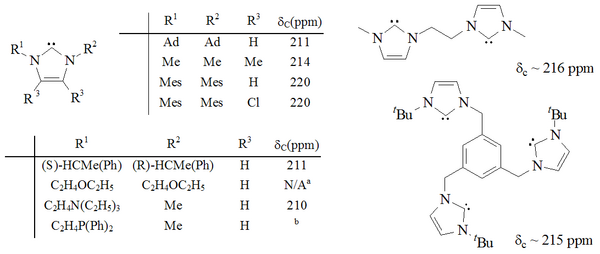
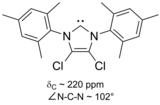
In het bijzonder de vervanging van de waterstofatomen op de plaatsen 4 en 5 door chloor-atomen was belangrijk in de synthese van het eerste luchtstabiele carbeen.[20] De extra grote stabiliteit heeft mogelijk te maken met het elektronenzuigende effect van de chloor-atomen via de σ-bindingen. De elektronendichtheid op het carbeen-koolstofatoom wordt daardoor lager, waardoor het vrije elektronenpaar sterker gebonden wordt en minder snel reageert.
Naast de monocarbenen zijn er nu ook di- en tri-carbenen bekend: moleculen waarin twee of drie imidazool-3-ylideenresten een plaats vinden.[40][41]
Op imidazool gebaseerde carbenen zijn thermodynamisch stabiel. In het algemeen wordt het 13C-NMRsignaal van het carbeen-koolstaf-atoom gevonden tussen 210 and 230 ppm. Op basis van röntgendiffractie is de N–C–N bindingshoek 101–102°, vergeleken met 108° voor de regelmatige vijfhoek.
Triazool-5-ylidenen[bewerken | brontekst bewerken]
Afhankelijk van de rangschikking van de stikstof-atomen zijn er twee typen triazolen mogelijk: de twee resterende koolstofatomen liggen naast elkaar in de ring, of zij worden van elkaar gescheiden door een stikstof-atoom. De van deze triazolen afgeleide stabiele carbenen zijn dan: 1,2,3-triazool-5-ylideen (alle stikstofatomen bij elkaar, en dus de koolstof-atomen ook)) en 1,2,4-triazool-5-ylideen (met een stikstof-atoom tussen de twee koolstoffen).
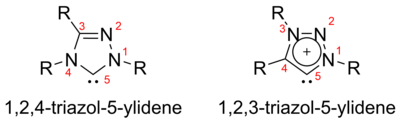
De op de 1,2,4-triazoolring gebaseerde triazool-5-ylidenen die hieronder zijn weergegeven zijn als eerste bereid.[42] via vacuum pyrolyse op basis van 2-methoxytriazolen onder verlies van methanol. Van deze groep carbenen is slechts een beperkt aantal gesynthetiseerd. De stabiliteit ervan is echter zo groot dat het trifenylderivaat commercieel verkrijgbaar is.
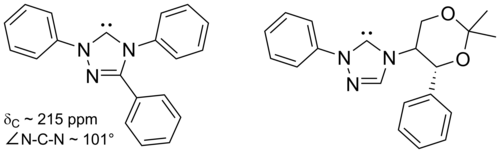
Op triazool-gebaseerde carbenen zijn thermodynamisch stabiel en hebben 13C-NMRsignalen voor het carbeen-koolstaf-atoom tussen 210 and 220 ppm. Op basis van röntgendiffractie is voor het trifenylderivaat een de N–C–N bindingshoek van 101° gevonden. De uitgangsstoffen, 5-methoxytriazolen, worden gemaakt uit triazoliumzout met natriummethoxide, dat als nucleofiel reageert.[42] Dit zou kunnen betekenen dat deze carbenen minder aromatisch zijn dan de uitgangsstoffen want de imidaloliumzouten reageren niet met nucleofielen. Dit zou verlies van aromaticiteit betekenen.
Andere diaminocarbenen[bewerken | brontekst bewerken]
De twee hierboven beschreven groepen kunnen gezien worden als speciale gevallen van een breder spectrum van verbindingen met een carbeen-centrum tussen twee stikstof-atomen. Een aantal voorbeelden van variaties op dit thema zijn door Alder's researchgroep bereid. In sommige van deze verbindingen is de N–C–N-eenheid onderdeel van een vijf- of niet aromatische zesring,[26][27][43] inclusief een bicyclisch voorbeeld. In andere gevallen worden de twee stikstof-atomen alleen met elkaar verbomden via het carbeen, en ze zijn wel of niet deel van eigen ringsystemen.[29][30][31]

In tegenstelling tot de imidazool-2-ylidenen en triazool-5-ylidenen blijken deze carbenen niet thermodynamisch stabiel: een aantal van de niet sterisch gehinderde cyclische en acyclische voorbeelden vertoont dimerisatie.[27][30] Experimentele gegevens wijzen in de richting van een zuur-gekatalyseerde reactie zoals in het Wanzlick evenwicht.[28]
Deze diaminocarbenen hebben in het 13C-NMR chemische verschuivingen voor het carbeen-koolstof-atoom tussen de 230 en 270 ppm. De röngendiffractie geeft voor de N-C-N-hoek een waarde van ongeveer 106° voor dihydroimidazool-2-ylideen, terwijl voor het acyclische carbeen een waarde van 121° gevonden wordt. Voor de eerste verbinding kan hierbij gewezen worden op de nog steeds aanwezige ring die de bindingshoeken iets kleiner maakt dan standaard, terwijl door de langere band tussen de atomen 4 en 5 van de ring, de dubbele band in imidazool is door een enkele binding vervangen waardoor meer ruimte ontstaat aan de andere zijde van het molecuul om bindingshoeken meer spanningsvrij te maken. De tweede waarde is erg dicht bij de verwachte waarde voor een sp2 gehybridiseerd koolstof-atoom. Beide waarden zijn daarmee groter dan voor de imidazool-2-ylidenen gevonden wordt.
Heteroamino carbenen[bewerken | brontekst bewerken]
Zoals bij Factoren die de stabiliteit beïnvloeden al is aangegeven is stikstof niet de enige atoomsoort die optreedt als buur van een stabiel carbeen: zuurstof, zwavel en fosfor kunnen ook als zodanig optreden.[15][16][32][33]
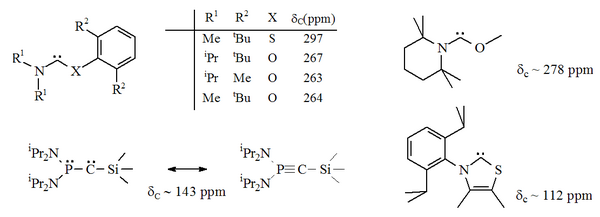
Vooral de formele vervanging van een stikstof-atoom door zwavel zou de imidazool-kern omzetten in een thiazool. Daarmee is een stof gesynthetiseerd die in principe gelijk is aan het door Breslow (Zie geschiedenis) voorgestelde carbeen.[44] Het röntgendiffractiepatroon van deze stof is bepaald.[32] Ook andere, niet aromatische aminocarbenen met O, S en P aan de andere zijde van he carbeen zijn inmiddels bekend: op thio- en oxyiminium-gebasserde carbenen zijn beschreven en met röntgendiffractie gekarakteriseerd.[33]
Omdat zuurstof en zwavel slechts divalent zijn is sterische bescherming in deze verbinding nauwelijks aan de orde, vooral als de N-C-X-eenheid onderdeel is van een ring. Voor de niet-cyclische carbenen worden 13C NMR-sigsnalen gevonden tussen 250 en 300 ppm, de hoogste waarden die tot nu (2012)[36] toe voor stabiele carbenen gevonden zijn. Op basis van de röntgen-gegevens is de N-C-X-hoek tussen de 104° en 109°.
Voor carbenen die formeel afgeleid zijn van imidazool-2-ylidenen waarin beide stikstof-atomen vervangen zijn door leden van de zuurstofgroep wordt verwacht dat ze niet stabiel zijn: ze zullen de neiging hebben te dissociëren naar een alkyn, , en een koolstofdioxide (of een variant daarop, waarin een of beide zuurstofatomen zijn vervangen door een van de andere leden van de zuurstofgroep).[45][46]
Niet-aminocarbenen[bewerken | brontekst bewerken]
De reactie van CS2 met elektrondeficiënte alkynen wordt verondersteld te verlopen via een intermediair 1,3-dithioliumcarbeen, dat vervolgens dimeriseert tot een tetrathiafulvaleen-derivaat. Het verloop van de omgekeerde reactie is daarom goed voorstelbaar in vergelijkbare carbenen.[45][46]
Bertrand's carbenen[bewerken | brontekst bewerken]
In Bertrand's stabiele carbenen is het carbeen-centrum gekoppeld aan zowel silicium als fosfor.[47] Deze verbindingen vertonen ook enige alkyn-achtige eigenschappen en ten tijde van de publicatie was er nog discussie over het exacte carbeen-karakter van de stoffen.[16]
Andere nucleofiele carbenen[bewerken | brontekst bewerken]
Een van de beschreven stabiele N-hetrocyclisch carbenen[48] heeft een aan borazine analoge structuur, waarbij een boor-atoom vervangen is door een methyleengroep, wat resulteert in een vlakke, zes-π-elektronen-verbinding.

Cyclopropenylidenen[bewerken | brontekst bewerken]
Een andere groep carbenen heeft de cyclopropenylideen-structuur as basis, een ring van drie koolstof-atomen met een dubbele binding tussen de twee niet-carbeen atomen. Als voorbeeld geldt Bis(di-iso-propylamino)cyclopropenylideen.[35]
Triplet carbenen[bewerken | brontekst bewerken]
Voor "gewone" carbenen is de elektronische grondtoestand een triplet: de twee elektronen op het carbeen-koolstofatoom bevinden zich in verschillende orbitalen en hebben parallelle spin. Voor de stabiele carbenen geldt juist dat de "normale" toestand een singlet staat is: beide elektronen bevinden zich in dezelfde orbitaal, hun spins zijn dan noodgedwongen anti-parallel. Voor de "normale" stabiele carbenen geldt juist het omgekeerde, staandaard zijn het singlet-moleculen, maar er zijn uitzonderingen.
In 2001 waren Hideo Tomioka etal in staat een stabiel carbeen te maken met een triplet grondtoestand: (bis(9-anthryl)carbene, met een halfwaardetijd van 19 minuten. Door gebruik te maken van de delokalisatie van de twee elektronen van he carbeen naar twee verschillende ringsystemen wordt het carbeen-centrum in een sp-hybridisatie gebracht. De twee p-orbitalen staan haaks op elkaar, maken deel uit van een identiek elektronen-systeem, en hebben dus dezelfde energie. Het is nu energetisch gunstiger de twee elektronen in verschillende orbitalen te plaatsen, waardoor de triplet-toestand ontstaat.[49][50]

In 2006 werd door dezelfde groep een triplet-carbeen beschreven met een halfwaardetijd van 40 minuten.[51] Dit carbeen ontstaat, onder uitstoting van stikstofgas, in de fotochemische ontledingsreactie van een diazomethaan-uitgangsstof precursor. De in onderstaande figuur aangegeven gehoekte structuur moet ook hier, net als in de figuur hierboven, lineair zijn. De twee fenyl-ringen staan haaks op elkaar en conjugeren elk met een van de orbitalen waarin de elektronen zich bevinden.
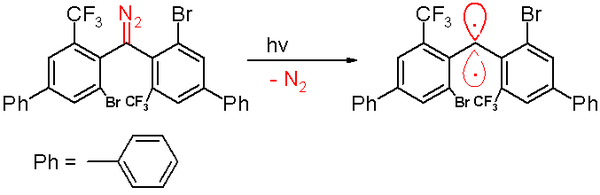
Blootstelling van dit laatste carbeen aan zuurstofgas (een triplet diradicaal) leidt tot het overeenkomstige benzofenon. Net als bij andere stabiele carbenen bevat dit voorbeeld sterisch grote groepen (broom en de trifluormethylgroep aan de fenylringen. Zij voorkomen, of in ieder geval vertragen, de reactie naar een 1,1,2,2-tetra(fenyl)alkeen. Op basis van berekeningen is de bindingslengte tussen het carbeen-centrum en het C1-atoom 138 pm. De bindingshoek op het carbeen-centrum is 158.8°. De vlakken van de twee fenylringen staan bijna haaks op alkaar: 85.7°.
Mesoionic carbenes[bewerken | brontekst bewerken]
Meso-ionische carbenen (MICs) zijn vergelijkbaar met de N-heterocyclische carbenen (NHCs) met dit verschil dat er geen standaard resonantiestructuren getekend kunnen worden, zonder ook ladingen in het molecuul te introduceren. Vanuit het perspectief van eerder bekende NHC's worden ze wel als abnormale NHC's (aNHC) benoemd.
Chemische eigenschappen[bewerken | brontekst bewerken]
Base en nucleofiel[bewerken | brontekst bewerken]
De imidazool-2-ylidenen zijn sterke basen met (in DMSO) pKz-waarden van ongeveer 24.[52]

DMSO bleek echter een onverwachte "grap" in petto te hebben: diaminocarbenen zijn in staat DMDSO te deprotoneren, waarna de ontstane ionen (het DMSO-anion en amidiniumzout) met elkaar reageren.
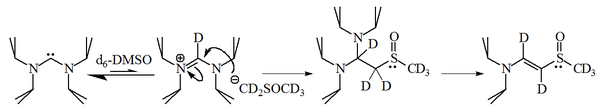
De reactie van imidazool-2-ylidenen met 1-broomhexaan leverde 90% van het 2-gubstitueerde product en slechts 10% van het overeenkomstige alkeen. Het carbeen is dus ook een redelijk sterk nucleofiel.
De pKz-waarden van de geconjugeerde zuren van verschillende groepen NHC's zijn in water bepaald. Voor de triazolium-ionen gelden waarden van 16.5–17.8,[53] ongeveer 3 pKz-eenheden hoger dan voor de overeenkomstige imidazolium-ionen.[54]
Dimerisatie[bewerken | brontekst bewerken]
Er is een tijd geweest dat men aannam dat stabiele carbenen reversibel dimeriseerden via het Wanzlick evenwicht. Inmiddels (2012)[36] is duidelijk dat imidazool-2-ylidenen en triazool-5-ylidenen thermodynamisch stabiel zijn en niet dimeriseren. In oplossing, watervrij en luchtdicht, zijn de carbenen jaren stabiel. Het aromatische karakter van deze carbenen is daar waarschijnlijk de achtergrond van. In feite zijn de carbenen zo stabiel dat ze alleen in zeer speciale gevallen gedwongen worden te dimeriseren.
Chen en Taton[55] maakten dubbel gebrugde di-imidazool-2-ylidenen door de respectievelijke di-imidazoliumzouten te deprotoneren. Alleen de dubbelgebrugde carbenen met de kortere alkylydeenbruggen resulteerden in dimeren. De grens ligt blijkbaar tussen 3 en 4 koolstof-atomen in de bruggen.

Als dit dimeer als dicarbeen zou bestaan, dan worden de vrije elektronenparen zeer dicht tegen elkaar aan geforceerd. De resulterende elektrostatische interactie zou dan een zeer groot destabiliserend effect hebben. Het dicarbeen ontsnapt daarom naar het dimeer.
Aan de andere kant is ook bekend dat heteroaminocarbenen, zoals R2N–C–OR en R2N–C–SR) en de niet-aromatische diaminocarbenen als R2N–C–NR2, hoewel langzaam, dimeriseren.[56] Verondersteld wordt dat de hoge barriere tegen dimerisatie het gevolg is van de singlet-toestand van deze carbenen.

Diaminocarbenen dimeriseren zelf niet echt, eerder wordt het dimeer gevormd via een formamidinium-zout, een geprotoneerd intermediair.[28] Het gevolg hiervan is dat de reactie zuur gejkatalyseerd is. Deze reactie kan verlopen omdat, in tegenstelling tot de op imidazolium gebaseerde carbenen, protoneren geen verlies van aromaticiteit betekent.
In tegenstelling tot de triplet-carbenen naderen de twee singlet-carbenen elkaar niet rechtstreeks ("kleinste beweging"), eerder reageert het vrije carbeen elektronenpaar met de onbezette p-orbitaal op het andere carbeen. Ook metalen kunnen de dimerisatie katalyseren.
Reactiviteit[bewerken | brontekst bewerken]
De chemie van de stabiele carbenen is nog lang niet volledig onderzocht. Een eerste overzicht van triazool-5-ylidenen is echter wel al mogelijk.[42][57][58]

| a | 3,6-difenyl-1,2,4,5-tetrazine, tolueen | 92% | e | 2 equiv., ΦNCO[59], tolueen, reflux | 92% | |
|---|---|---|---|---|---|---|
| b | RXH, RT[60] | 95–97% | f | CS2, tolueen, or ΦNCS[59], THF, RT[60] | 71–90% | |
| c | O2, S8, or Se, tolueen, reflux | 54–68% | g | Maleimide, THF, RT[60] | 47–84% | |
| d | R1CH=CHR2, THF, RT[60] | 25–68% | h | Dimethylacetylene dicarboxylate, THF, reflux | 21% |
Deze carbenen reageren vooral op een nucleofiele manier (e and f), ze vertonen inschuifreacties (b), addities (c), [2+1] cycloaddities (d, g en h), [4+1] cycloaddities (a) zowel als eenvoudige deprotonering. De insertie (b) is mogelijk een vervolgreactie na deprotoneren, waarbij een nucleofiel ontstaat (−XR) dat vervolgens reageert met het ook ontstane zout. Hierbij ontstaat de indruk van een H–X insertie.
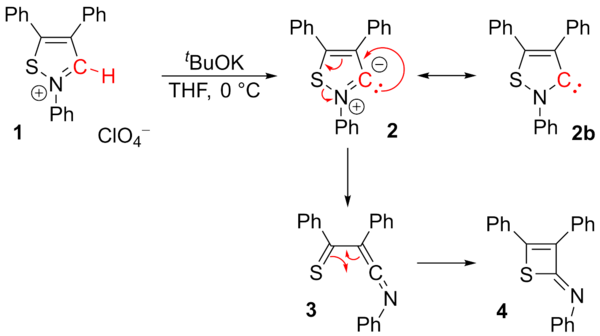
Bij het in 2007 als stabiel beschreven isothiazool-carbeen (zie hieronder: 2b), afgeleid van een isothiazoliumperchloraat (1),[61] werden vragen gesteld ten aanzien van die stabiliteit.[62] De onderzoekers konden alleen 2-imino-2H-thieet (4) isoleren. Het intermediair 3 werd verondersteld op te treden via een omleggingsreactie. Tegenwoordig (2012[36] 0 wordt carbeen 2b niet meer als stabiel beschouwd.[63]
Complexen met carbenen[bewerken | brontekst bewerken]
Van imidazool-2-ylidenen, triazool-5-ylidenen (en in mindere mate, diaminocarbenen) is aangetoond dat ze met een grote verscheidenheid van elementen complexen vormen, van alkalimetalen, hoofdgroepelementen, en overgangsmetalen tot lanthanides en actinides. Een in het periodiek systeem gerangschikte tabel geeft een grof idee van de inmiddels beschreven complexen. Veel van de complexen zijn via röntgendiffractie gekarakteriseerd.[43][64][65] de indruk bestaat dat stabiele carbenen zich wat ligand-eigenschappen betreft, op dezelfde manier reageren als de organofosfines. Via het vrije elektronenpaar op het carbeen-atoom zijn het goede σ-donors, maar slechte π-acceptoren. Dit laatste door de in de NHC's gegeven interne π-backbonding vanuit de stikstofatomen naast het carbeen-centrum. Enders[66] en Hermann[67][68] hebben aangetoond dat deze carbenen bruikbare vervangers zijn voor de fosfine-liganden in verschillende katalytische cycli. Hoewel is vastgesteld dat de gevormde katalysator minder actief is dan het fosfine-analogon, is de katalysator wel robuuster. Verschillende katalytische systemen zijn door Hermann en Enders onderzocht met imidazool- en triazool-carbeen houdende katalysatoren. De resultaten waren matig succesvol.[64][66][67][68] Van Grubbs[69] is de melding over een succesvolle vervanging van een fosfine-ligand () door een imidazool-2-ylideen in de alkeenmetathese-reactie die beschreven is met als katalysator. Zij noteerden een hogere ringsluitings-metathese, evenals een "opmerkelijke lucht en waterstabiiteit".
Moleculen met twee en drie stabiele carbeen-eenheden zijn gemaakt als mogelijke bidentaat en tridentaat-carbeen-liganden.[40][41]
| Elementen waarmee stabiele carbenen complexen vormen | ||||||||||||||||||
| 1 Ia |
2 IIa |
3 IIIb |
4 IVb |
5 Vb |
6 VIb |
7 VIIb |
8 VIIIb |
9 VIIIb |
10 VIIIb |
11 Ib |
12 IIb |
13 IIIa |
14 IVa |
15 Va |
16 VIa |
17 VIIa |
18 0 | |
| 1 | H | He | ||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe |
| 6 | Cs | Ba | * | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | ** | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Uus | Og |
| *Lanthaniden | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | |||
| **Actiniden | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | |||
| Legenda | ||||||||||||||||||
| Geen complex bekend | ||||||||||||||||||
| Complex beschreven | ||||||||||||||||||
Carbenen in de organometaalchemie en katalyse[bewerken | brontekst bewerken]
Carbenen kunnen worden gestabiliseerd als organometaal-componenten. Voor de overgangsmetalen vallen deze complexen in twee groepen uiteen:
- Fischer-carbenen, waarin het carbeen gekoppeld is aan een metaal en een elektronenzuigende groep, meestal een carbonylgroep.
- Schrock-carbenen, waarin het carbeen gekoppeld is aan een metaal en een elektronenstuwende groep.
De reacties van deze carbenen verschillen zeer sterk van die waarin geen metaal-complex aanwezig zijn.
Chemie van triplet-carbenen[bewerken | brontekst bewerken]
De chemie van de stabiele triplet-carbenen is, zo wordt verwacht, weinig verschillend van die van "normale" triplet-carbenen.
Fysische eigenschappen[bewerken | brontekst bewerken]

De tot nu toe geïsoleerde carbenen zijn kleurloze of witte vaste stoffen met een laag smeltpunt. In hoog vacuüm kunnen ze bij relatief lage temperaturen gesublimeerd worden.
Een van de zeer bruikbare fysische eigenschappen van stabiele carbenen is de chemische verschuiving van het carbeen-koolstof-atoom die optreedt in het 13C-NMR-spectrum. De waarde voor deze veerschuiving is tussen de 200 and 300 ppm. Het spectrum vertoont in dit gebied releatief weinig andere pieken. In het voorbeeld rechts is het 13C-NMR weergegeven van een cyclisch diaminecarbeen met de carbeenpiek bij 238 ppm.
Toepassingen[bewerken | brontekst bewerken]

NHC's worden ruim toegepast als ligand in de organometaalchemie. Een praktsche toepassing is de op ruthenium gebaseerde Grubbs' katalysator en de NHC-Palladium Complexen voor koppelingsreacties.[70][71][72] NHC-metaalcomplexen, met name de Ag(I)-NHC complexen, zijn uitgebreid getest ten behoeve van mogelijk biologische toepassingen.[73]
Synthese[bewerken | brontekst bewerken]
Zoals eerder genoemd zijn NHC's vaak sterk basisch metpKz-waarden van ongeveer 24 voor het geconjugeerde zuur.[52] Bovendien reageren ze snel met zuurstof. Het is duideijk dat de synthese plaats moet vinden in luchtvrije (met name zuurstofvrije) omstandigheden, terwijl stoffen die zelfs maar een beetje zuur kunnen reageren ook vermeden moeten worden.[74]
Hier zullen ook sterke, sterisch niet gehinderde nucleofielen vermeden moeten worden, of ze nu ter plekke ontstaan, of als verontreiniging in gebruikte reagentie aanwezig zijn (zoals LiOH in BuLi).
Hieronder volgt een, niet uitputtende, lijst van uitgewerkte benaderingen voor de synthese van stabiele carbenen.
Deprotoneren[bewerken | brontekst bewerken]
Deprotonering van uitgangsstoffen voor carbenen is een betrouwbare syntheseroute gebleken.:
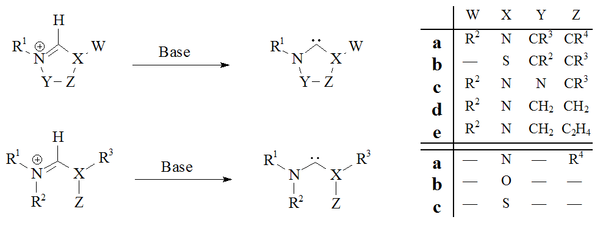
(Dihydro)imidazool-2-ylidenen zijn toegankelijk via het deprotoneren van dihydroimidazolium- en imidazolium-zouten. De acyclische[29][30] en de op tetrahydropyrimidinyl[43] gebaseerde carbenen ontstaan onder invloed van opgeloste, sterke basen (nBuLi).
Met wisselend succes is een groot aantal reactie-omstandigheden gebruikt om de carbenen te maken. De mate van succes werd vooral bepaald door de gebruikte uitgangsstof. Het voornaamste probleem bij deze routes is het scheiden van de metaal-ionen (de tegenionen van de gebruikte base) van het gevormde carbeen.
Hydride als base[bewerken | brontekst bewerken]
Een eerste gedachte zou zijn dat natrium- of kaliumhydride[26][32] de ideale basen zouden zijn. Deprotoneren vindt plaats met ontwikkeling van waterstofgas, een irreversibele reactie. Het gewenste carbeen ontstaat, samen met wat anorgaische bijproducten. Deze, en een teveel aan hydride, laten zich via filtreren verwijderen. In de praktijk blijkt deze reactie echter zeer traag. Toevoegen van DMSO versnelt de reactie, maar heeft ook het risico in zich van onbedoelde zijreacties (zie: onderste figuur in Base en nucleofiel)[17][25]
Deprotoneren met natrium- of kaliumhydride in een mengsel van vloeibare ammoniak en THF bij −40 °C is beschreven voor imidazool-derivaten.[37] Arduengo etal[32] beschreven het gebruik van in de bereiding van dihydroimidazool-2-ylidenen. Deze methode is niet gebruikt in de synthese van de diaminocarbenen. In een aantal gevallen kan kalium-tert-butoxide gebruikt worden.[25]
Alkyllithium-verbindingen als base[bewerken | brontekst bewerken]
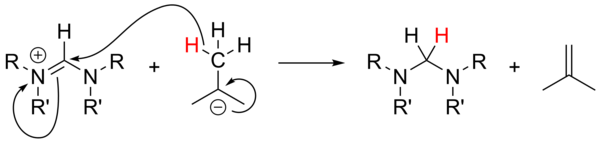
De toepassing van alkyllithium-verbindingen als sterke base[17] is niet uitgebreid bestudeerd, maar bleek wel een onbetrouwbare keuze voor het deprotoneren van van de uitgangsstoffen. Met niet-aromatische zouten kunnen n-BuLi en ΦLi[59] zich as nucleofiel gedragen, terwijl tBuLi als hydride-bron kan fungeren, waarbij isobuteen als bijproduct optreedt:
Amides als base[bewerken | brontekst bewerken]
Lithiumamides, met als bekendste voorbeeld lithiumdi-isopropylamide, LDA maar ook (lithiumtetramethylpiperidide (LiTMP)),[29][30] werken in het algemeen om allerlei soorten uitgangs-ionen te deprotoneren naar stabiele carbenen. Voorwaarde is wel dat er niet te veel LiOH als verontreiniging aanwezig is in het bij de in situ bereiding van de amides gebruikte n-butyllithium. Met metaalzouten van hexamethyldisilazaan[43] kunnen alle types zouten als uitgangstof voor de carbenen in een schone reacie gedeprotoneerd worden. Alleen bij ongehinderde formamidinium-zouten reageert de base als nucleufiel, en ontstaan triaminomethane gesubstitueerde producten.
Metaal-vrije carbeensynthese[bewerken | brontekst bewerken]

In verband met het bestuderen van stabiele carbenen zonder de metalen afkomstig uit hun bereiding, is uitgebreid gezocht naar metaalvrije syntheseroutes. Ten gevolge van de stabiliteit van veel van de metaal-carbeen-complexen is een scheiding van metaal en carbeen vaak problematisch. De eenvoudigste oplossing is dan het carbeen in afwezigheid van metalen maken. Daarnaast is ook vastgesteld dat sommige metalen de carbenen noch binden noch stabiliseren maar optreden als katalysator in het dimerisatie-proces van vooral ongehinderde voorbeelden.
In de figuur rechts is de kristalstructuur op basis van röntgendiffractie te zien van een complex van kalium-HMDSA. Dit complex ontstaat als een overmaat KHMDSA gebruikt wordt als sterke base om het als uitgangsstof gebruikte formamidiniumzout te deprotoneren. Kalium- en natrium-zouten die als bijproduct ontstaan kunnen vaak via filtratie verwijderd worden, voor lithium is het gebruik van cryptanden of kroonethers meestal noodzakelijk.
Verwijderen van elementen uit de zuurstofgroep[bewerken | brontekst bewerken]
Een andere benadering wordt gevonden door het carbeen te maken op basis van het verwijderen van zwavel uit een thioureum met behulp van kalium in THF.[27][75] Een bijkomend voordeel van deze benadering is dat het bijproduct van de reactie, kaliumsulfide onoplosbaar is in het gebruikte oplosmiddel. De in deze methode gebruikte hogere temperatuur maakt deze methode wel minder geschikt voor carbenen die gevoelig zijn voor dimerisatie. Er is een voorbeeld bekend van het verwijderen van zuurstof uit een ureum-derivaat. Met behulp van een van fluoreen afgeleid carbeen wordt het bis(dimethylamino)carbeen verkregen, naast fluorenon:[76]
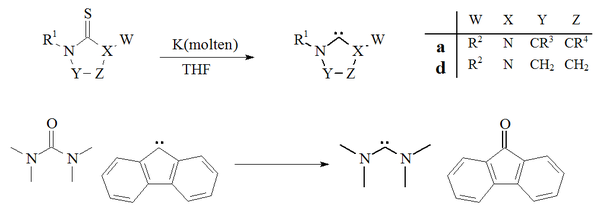
Het verwijdering van zwavel uit thiourea's met gesmolten kalium, waarbij imidazool-2-ylidenen ontstaan wordt niet breed toegepast. Een voorbeeld is wel de synthese van dihydroimidazoolcarbenen.[27]
Vacuum pyrolyse[bewerken | brontekst bewerken]
Vacuumpyrolyse, waarbij neutrale, vluchtige delen van het molecuul (methanol, chloroform) verwijderd worden is toegepast in de synthese van op dihydroimidazolen en triazolen gebaseerde carbenen. Historisch is het experiment van Wanzlick[7] een eerste poging tot de synthese van dihydroimidazool-2-ylidenen, maar vaak gebruikt is hij niet. Door Enders[42] is vacuümpyrroyse toegepast in de bereiding van een triazool-5-ylideen.

Bis(trimethylsilyl)kwik[bewerken | brontekst bewerken]
Bis(trimethylsilyl)kwik, , reageert met chloor-Iminium en chloor-amidiniumzouten, waarbij metaal-vrije carbenen en metalisch kwik ontstaan.[77] Bijvoorbeeld:
Fotochemische ontleding[bewerken | brontekst bewerken]
Stabiele triplet-carbenen zijn via de fotolyse van geschikte diazoniumverbindingen, onder gelijktijdige ontwikkeling van stikstofgas gemaakt. Standaard reactieomstandigheden zijn dan een oplossing van de uitgangsstof in benzeen en bestralen met UV-licht van 300 nm.
Zuivering[bewerken | brontekst bewerken]
Hoewel stabiel, zijn deze carbenen wel gevoelig. Een minimum aan handelingen vergroot de kans op succes bij de synthese. Daarbij geldt een strikt water- en zuurstofvrije omgeving, naast relatief zuurvrij werken als voorwaarde. Als daar rekening mee gehouden wordt zijn stabiele carbenen inderdaad stabiel tijdens diverse handelingen. Zo kan een met kaliumhydride bereid carbeen over een droog (= watervrij) filterbed van diatomeeënaarde gezuiverd worden van het overschot aan (vast) kaliumhydride. Op kleine schaal kan men een suspesie waarin in een carbeen is opgelost enige tijd laten staan om uit te zakken. Daarna kan de bovenstaande vloeistof door een droog membraan gefilterd worden. Stabiele carbenen zijn goed oplosbaar in apolaire oplosmiddelen als hexaan, waardoor omkristalliseren meestal lastig is ten gevolge van het ontbreken van een geschikt oplosmiddel(mengsel) waarin het carbeen bij lage temperatuur nauwelijks, bij hoge temperatuur goed oplosbaar is, en dat bovendien niet met het carbeen reageert.
Sublimatie kan een effectieve zuiveringsmethode zijn voor deze carbenen, hoewel de temperatuur bij voorkeur onder de 60 °C moet blijven: de carbenen zijn relatief vluchtig en zouden ook kunnen gaan ontleden. Sublimatie is in een aantal gevallen de bron geweest van de voor röntgendiffractie benodigde één-kristallen. Het metaalvrij, vooral lithium-vrij, zijn van het carbeen is dan een voorwaarde: de lithiumzouten zijn nauwelijks vluchtig.
Bronnen, noten en/of referenties
Verwijzingen in de tekst
|




![{\displaystyle {\ce {RuCl2[P(cC6H11)3]2CH(C6H5)}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1e6b13b326cb433813ea266f7fe54c1bc84e5676)


![{\displaystyle {\ce {(CH3)3Si-Hg-Si(CH3)3\ +\ [R2N=C(Cl)NR2^{+}][Cl^{-}]\ ->\ R2N-C-NR2\ +\ Hg_{l}\ +\ 2(CH3)3SiCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/bfc6a35bccf052bcbe106824c450e5358a1bfaab)