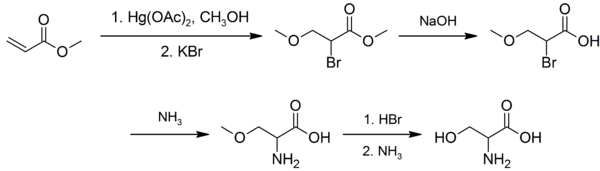Serine
| L-serine | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||

| ||||
▵ Structuurformule van L-serine
| ||||

| ||||
▵ Molecuulmodel van L-serine
| ||||
| Algemeen | ||||
| Molecuulformule | ||||
| IUPAC-naam | Serine | |||
| Andere namen | β-hydroxyalanine | |||
| Molmassa | 105,09258 g/mol | |||
| CAS-nummer | 56-45-1 | |||
| EG-nummer | 200-274-3 | |||
| Wikidata | Q183290 | |||
| Beschrijving | Witte kristallen | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Dichtheid | (bij 20°C) 1,603 g/cm³ | |||
| Smeltpunt | 222 °C | |||
| Oplosbaarheid in water | 364 g/L | |||
| Goed oplosbaar in | water | |||
| Onoplosbaar in | ethanol, di-ethylether | |||
| Evenwichtsconstante(n) | pKz1 = 2,21 (carboxyl)[1] pKz2 = 9,15 (amino) | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Serine (afgekort als Ser of S) is een van de twintig natuurlijk voorkomende aminozuren. Serine is een α-aminozuur dat gebruikt wordt voor de synthese van eiwitten. De zijketen van serine bevat een polaire hydroxylgroep, waardoor het aminozuur goed oplost in water. Het is een niet-essentieel aminozuur, wat betekent dat het onder normale omstandigheden in het menselijk lichaam wordt aangemaakt.
Serine vervult verschillende biologische functies. Het wordt bij de stofwisseling gebruikt als precursor voor verschillende metabolieten, zoals purines en pyrimidines. Het aminozuur speelt daarnaast een belangrijke rol in de eiwitstructuur, doordat het gemakkelijk waterstofbruggen kan vormen met andere delen van de eiwitketen. Ten slotte worden isomeren van serine in het zenuwstelsel gebruikt voor de overdracht van signalen, met name door middel van glutamaatreceptoren.
Structuur en eigenschappen[bewerken | brontekst bewerken]
Het residu van serine is een alcoholfunctie die via een methyleengroep verbonden is met het centraal α-koolstofatoom. Serine wordt geclassificeerd als een hydrofiel aminozuur. Het is goed oplosbaar in water, maar niet in di-ethylether en ethanol.
De zuurconstanten van serine zijn:[1]
- pKa1 (carboxylgroep) = 2,21
- pKa2 (aminegroep) = 9,15
Het iso-elektrisch punt ligt bij pH 5,68.[1]
Door de aanwezigheid van een hydrofiele hydroxylgroep in het residu kan serine gefosforyleerd worden. In die context speelt het aminozuur een niet onbelangrijke rol bij de activering of inhibitie van enzymen. Wanneer serine addeert aan palmitaldehyde (het aldehyde van palmitinezuur) en dehydrogeneerd worden, dan vormt zich een sfingolipide.
Serine wordt gecodeerd door de codons UCU, UCC, UCA, UCG, AGU en AGC.
Synthese[bewerken | brontekst bewerken]
Op industriële schaal wordt serine bereid door vergisting. De jaarlijkse hoeveelheid die op deze manier wordt geproduceerd wordt geschat op 100 tot 1000 ton. In het laboratorium kan het als racemaat worden bereid uit methylacrylaat in verschillende stappen:[2]
De eerste stap betreft een oxidatie met kwik(II)acetaat in methanol, gevolgd door behandeling met kaliumbromide. De hierdoor ontstane α-broomester wordt vervolgens verzeept met behulp van natriumhydroxide, waarna het bromide met ammoniak wordt omgezet in een amine. De hydrolyse van de methylether leidt vervolgens tot de vorming van serine.
Voorkomen, biosynthese en metabolisme[bewerken | brontekst bewerken]
Serine is een niet-essentieel aminozuur, omdat het in het lichaam wordt gevormd uit andere metabolieten, zoals glycine. Het aminozuur werd voor het eerst geïsoleerd in 1865 uit proteïnen in zijde. De naam is afgeleid van het Latijnse woord voor zijde, namelijk sericum.
De biosynthese van serine start met de oxidatie van 3-fosfoglyceraat tot 3-fosfopyruvaat en NADH. De reductieve aminering van dit keton, gevolgd door hydrolyse, levert serine. Het enzym serine-hydroxymethyltransferase katalyseert de reversibele omzetting van L-serine naar glycine (via een retro-aldol-reactie).[3]
Biologische functies[bewerken | brontekst bewerken]
Serine is een belangrijke verbinding, omdat het deelneemt aan de biosynthese van purines en pyrimidines. Daarnaast is het een precursor voor de synthese van andere aminozuren, zoals glycine, cysteïne en tryptofaan. Zo start de biosynthese van cysteïne in dieren met serine en homocysteïne. Tevens is het aminozuur een precursor voor talloze andere metabolieten, waaronder sfingolipiden en foliumzuur.
Het aminozuur maakt deel uit van het katalytische centrum van verschillende enzymen, waaronder chymotrypsine en trypsine.
Bronnen, noten en/of referenties
|