Immuunsysteem: verschil tussen versies
Ziektes en kwalen Label: bewerking met nieuwe wikitekstmodus |
|||
| Regel 147: | Regel 147: | ||
Een gezonde voeding is noodzakelijk om alle cellen van het lichaam optimaal te laten functioneren, ook die van het immuunsysteem. Sommige nutriënten uit voeding spelen een directe rol in de afweer: het aminozuur [[arginine]] is bijvoorbeeld nodig voor de aanmaak van stikstofmonoxide in macrofagen, en [[vitamine A]] en [[zink (element)|zink]] hebben een regulerende rol op de [[celdeling]], en zijn daarom van belang bij de proliferatie van lymfocyten.<ref name="eat">{{Citeer journal |auteur=Childs CE, Calder PC, Miles EA. |titel=Diet and Immune Function |jaargang=11 |tijdschrift=Nutrients |datum=2019 |taal=en |nummer=8 |doi=10.3390/nu11081933|pmid=31426423 |pagina's=1933}}</ref> [[Voedingsvezel]]s kunnen invloed hebben op de immuunfunctie door in te spelen op het [[microbioom|darm-microbioom]].{{Refn|group=kleine-letter|Darmbacteriën kunnen vezelrijk voedsel fermenteren, en produceren hierbij kleine [[vetzuren]] (''short-chain fatty acids'') die een ontstekingsremmend effect kunnen hebben, onder meer door neutrofielmigratie te beïnvloeden.<ref>{{Citeer journal |auteur=Vinolo MA, Rodrigues HG, Nachbar RT, Curi R. |titel=Regulation of Inflammation by Short Chain Fatty Acids |url=http://www.mdpi.com/2072-6643/3/10/858 |jaargang=3 |tijdschrift=Nutrients |datum=2011 |taal=en |nummer=10 |doi=10.3390/nu3100858 |pmid=22254083 |pagina's=858–876}}</ref>}} De impact van voeding op immunologische aandoeningen (infectie, chronische ontstekingsziekten, allergieën) is – ondanks veel onderzoek – slechts beperkt in kaart gebracht.<ref>{{Citeer tijdschrift |auteur=Venter C, Eyerich S, Sarin T, Klatt K. |titel=Nutrition and the Immune System: A Complicated Tango |url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7146186/|jaargang=12 |tijdschrift=Nutrients |datum=2020 |taal=en |nummer=3 |doi=10.3390/nu12030818|pmid=32204518 |pagina's=818}}</ref> Eenduidige voedingsadviezen om de weerstand te verbeteren zijn dan ook lastig te formuleren. |
Een gezonde voeding is noodzakelijk om alle cellen van het lichaam optimaal te laten functioneren, ook die van het immuunsysteem. Sommige nutriënten uit voeding spelen een directe rol in de afweer: het aminozuur [[arginine]] is bijvoorbeeld nodig voor de aanmaak van stikstofmonoxide in macrofagen, en [[vitamine A]] en [[zink (element)|zink]] hebben een regulerende rol op de [[celdeling]], en zijn daarom van belang bij de proliferatie van lymfocyten.<ref name="eat">{{Citeer journal |auteur=Childs CE, Calder PC, Miles EA. |titel=Diet and Immune Function |jaargang=11 |tijdschrift=Nutrients |datum=2019 |taal=en |nummer=8 |doi=10.3390/nu11081933|pmid=31426423 |pagina's=1933}}</ref> [[Voedingsvezel]]s kunnen invloed hebben op de immuunfunctie door in te spelen op het [[microbioom|darm-microbioom]].{{Refn|group=kleine-letter|Darmbacteriën kunnen vezelrijk voedsel fermenteren, en produceren hierbij kleine [[vetzuren]] (''short-chain fatty acids'') die een ontstekingsremmend effect kunnen hebben, onder meer door neutrofielmigratie te beïnvloeden.<ref>{{Citeer journal |auteur=Vinolo MA, Rodrigues HG, Nachbar RT, Curi R. |titel=Regulation of Inflammation by Short Chain Fatty Acids |url=http://www.mdpi.com/2072-6643/3/10/858 |jaargang=3 |tijdschrift=Nutrients |datum=2011 |taal=en |nummer=10 |doi=10.3390/nu3100858 |pmid=22254083 |pagina's=858–876}}</ref>}} De impact van voeding op immunologische aandoeningen (infectie, chronische ontstekingsziekten, allergieën) is – ondanks veel onderzoek – slechts beperkt in kaart gebracht.<ref>{{Citeer tijdschrift |auteur=Venter C, Eyerich S, Sarin T, Klatt K. |titel=Nutrition and the Immune System: A Complicated Tango |url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7146186/|jaargang=12 |tijdschrift=Nutrients |datum=2020 |taal=en |nummer=3 |doi=10.3390/nu12030818|pmid=32204518 |pagina's=818}}</ref> Eenduidige voedingsadviezen om de weerstand te verbeteren zijn dan ook lastig te formuleren. |
||
| ⚫ | |||
== Het menselijke immuunsysteem == |
|||
===Immuundeficiënties=== |
|||
| ⚫ | |||
Het immuunsysteem werkt niet altijd perfect. Het kan bijvoorbeeld een aangeboren afwijking hebben, of in de loop van het leven minder goed gaan functioneren door tal van omstandigheden, variërend van medicijngebruik tot ondervoeding. Een tekortschietend immuunsysteem is gevaarlijk. Er bestaat immers een verhoogde gevoeligheid voor infecties, zelfs voor micro-organismen die gewoonlijk geen ziekte kunnen veroorzaken.<ref>{{Citeer journal |auteur=Chapel H, Prevot J, Gaspar HB, Español T, Bonilla FA. |titel=Primary Immune Deficiencies – Principles of Care |jaargang=5 |tijdschrift=Frontiers in Immunology |taal=en|datum=2014 |doi=10.3389/fimmu.2014.00627 |pmid=25566243}}</ref> Men spreekt van [[opportunistische infectie]]s. |
|||
[[Immuundeficiëntie]] is een [[aandoening]] waarbij sprake is van een niet, of niet voldoende functionerend immuunsysteem; er zijn [[erfelijkheid|erfelijke]] (aangeboren) en [[epigenetica|verworven]] vormen van immunodeficiëntie. |
|||
[[Severe combined immunodeficiency]] (SCID) is een zeldzame aangeboren afwijking van het immuunsysteem. Kinderen die geboren worden met SCID hebben geen of weinig T- en B-lymfocyten in hun bloed, waardoor zij zich niet of nauwelijks kunnen verweren tegen micro-organismen. De oorzaak van SCID ligt in [[mutatie (biologie)|mutatie]]s van receptoren op de lymfocyten.<ref>{{Citeer journal |auteur=Cirillo E, Giardino G, Gallo V. |titel=Severe combined immunodeficiency-an update: Severe combined immunodeficiencies|jaargang=1356 |tijdschrift=Annals of the New York Academy of Sciences |datum=2015 |taal=en |nummer=1 |doi=10.1111/nyas.12849 |pagina's=90–106}}</ref> Ook mensen die met een goed functionerend immuunsysteem worden geboren, kunnen later in hun leven te maken krijgen met een verminderde afweer. Misschien wel het sprekendste voorbeeld hiervan is infectie met het [[humaan immunodeficiëntievirus]] (hiv). Dit virus infecteert helper T-cellen, waardoor de verworven afweer dermate ontregeld raakt dat zich levensbedreigende infecties kunnen ontwikkelen.<ref>{{Citeer web|titel=Hiv |datum= 23-06-2022 |uitgever=RIVM |url= https://www.rivm.nl/hiv|accessdate=28-01-2023}}</ref><ref>{{Citeer journal |auteur=Deeks SG, Overbaugh J, Phillips A, Buchbinder S. |titel=HIV infection |jaargang=1 |tijdschrift=Nature Reviews Disease Primers |datum=2015|taal=en |url=https://www.nature.com/articles/nrdp201535|nummer=1 |doi=10.1038/nrdp.2015.35|pagina's=15035}}</ref> |
|||
Een voorbeeld van een ''aangeboren'' afwijking van het immuunsysteem is [[SCID (ziekte)|SCID]] (Severe Combined Immuno Deficiency Syndrome), dat voorkomt bij zeer jonge kinderen. ''Verworven'' immunodeficiëntie komt voor bij ziekten van het immuunsysteem zoals [[aids]] (het "verworven immuun deficiëntie syndroom"), een besmettelijke ziekte, die door het [[Hiv]] wordt overgebracht, die degeneratie van het immuunsysteem van het lichaam veroorzaakt, maar het wordt ook wel veroorzaakt door medicijnen, bijvoorbeeld bij [[transplantatie]]patiënten. |
|||
=== Auto-immuunziekten === |
|||
Anderzijds is een "overactief" immuunsysteem een eigenschap van een groot aantal verschillende soorten [[auto-immuunziekte]]n, zoals [[diabetes mellitus]] type I, [[multiple sclerose]] (MS), [[psoriasis]], [[reumatoïde artritis]] (reuma), en auto-immuunhepatitis. In deze ontbreekt de zelf-herkenningscapaciteit van het immuunsysteem, waardoor het een deel van het eigen lichaam van de patiënt aanvalt. |
|||
[[Bestand:Arthritic hands in pain.jpg|thumb|[[Reumatoïde artritis]] is een veelvoorkomende auto-immuunziekte van de [[gewricht]]en, waarbij vaak de handen zijn aangedaan]] |
|||
Onder normale omstandigheden wordt een immuunrespons tegen het eigen lichaam grotendeels voorkomen (en actief onderdrukt), door tolerantiemechanismen als [[klonale deletie]] en de werking van [[regulerende T-cellen|regulerende immuuncellen]].<ref name="Davidson" /> Wanneer deze tolerantie faalt of doorbroken wordt, en er antilichamen of effector T-cellen worden aangemaakt die tegen de eigen lichaamsweefsels actief zijn, kan dit leiden tot een [[auto-immuunziekte]].<ref name="Davidson">{{Citeer journal |auteur=Davidson A, Diamond B. |titel=Autoimmune Diseases |jaargang=345 |tijdschrift=New England Journal of Medicine |datum=2001 |taal=en |nummer=5 |doi=10.1056/NEJM200108023450506|pagina's=340–350}}</ref> |
|||
Auto-immuunziekten kunnen vrijwel ieder orgaan treffen en de klinische symptomen lopen dan ook ver uiteen. Sommige auto-immuunziekten zijn orgaanspecifiek, zoals de huidziekte [[psoriasis]]. Andere hebben een systemisch karakter, zoals [[systemische lupus erythematodes]] (SLE), waarbij vrijwel elk deel van het lichaam kan worden aangedaan. Bij SLE worden er antilichamen gevormd tegen het eigen dubbelstrengse DNA. Een ziekte als SLE kan zeer ernstig en zelfs fataal verlopen indien niet tijdig de diagnose wordt gesteld en een behandeling wordt gestart.<ref>{{Citeer journal |auteur=Dörner T, Furie R. |titel=Novel paradigms in systemic lupus erythematosus|jaargang=393 |tijdschrift=The Lancet |datum=2019 |taal=en |nummer=10188 |doi=10.1016/S0140-6736(19)30546-X |pagina's=2344–2358}}</ref> |
|||
In veel geïndustrieerde landen zoals Nederland en België vormen [[reumatoïde artritis]], de [[ziekte van Hashimoto]] en [[diabetes mellitus|diabetes type 1]] de top drie van auto-immuunziekten.<ref name="auto">{{nl}}{{sc|Rijkers}} ''et al'', pp. 21–22.</ref> Chronisch verlopende auto-immuunziekten zoals reumatoïde artritis kunnen leiden tot blijvende invaliditeit en vormen een zware ziektelast voor de patiënt en zijn omgeving. |
|||
===Allergie en overgevoeligheid=== |
|||
[[Bestand:Skin prick testing for allergies.jpg|thumb|De [[priktest|huidpriktest]] wordt gebruikt om te weten te komen of iemand allergisch reageert op bepaalde stoffen ([[allergeen|allergenen]])]] |
|||
Het lichaam staat voortdurend bloot aan onschuldige prikkels van buitenaf, zoals [[huisstofmijt]]en, [[voedingsstof|voedingsbestanddelen]] en [[pollen]]. Normaal gesproken komt het immuunsysteem niet in actie tegen deze prikkels omdat tolerantiemechanismen voorkomen dat een reactie optreedt. Sommige individuen vertonen echter wél een hevige respons, vaak met nare lichamelijke klachten tot gevolg.<ref>{{Citeer boek |titel=Allergies: Overview |url=https://www.ncbi.nlm.nih.gov/books/NBK447112/ |taal=en |uitgever=Institute for Quality and Efficiency in Health Care (IQWiG) |datum=2020}}</ref> Een overmatige reactie op een onschuldige prikkel ligt ten grondslag aan een [[allergie]]. De bekendste manifestaties van allergieën zijn [[contacteczeem|eczeem]], [[voedselallergie]] (bijvoorbeeld tegen gluten, noten of lactose), [[hooikoorts]] en [[astma]]. |
|||
Bij een allergische reactie spelen de cytokinen IL-4 en IL-5 een belangrijke rol. Deze cytokinen zetten onder andere B-lymfocyten aan tot de productie van IgE-antilichamen. IgE's die zich binden aan [[mestcel]]len, die na activatie krachtige ontstekingsmoleculen vrijgeven, zoals [[histamine]]n. Veel allergieremmende medicijnen gaan de overmatige werking van histamine tegen, de [[antihistaminica]].<ref>{{Citeer journal |auteur=Randall KL, Hawkins CA. |titel=Antihistamines and allergy |jaargang=41 |taal=en|tijdschrift=Australian Prescriber |datum=2018 |nummer=2 |doi=10.18773/austprescr.2018.013 |pmid=29670310 |pagina's=42–45}}</ref> |
|||
Vanaf het eind van de 20ste eeuw is het aantal mensen met een allergische ziekte sterk toegenomen, mogelijk als gevolg van toegenomen hygiëne en veranderingen in de omgeving. Het [[Rijksinstituut voor Volksgezondheid en Milieu]] (RIVM) heeft alle aandoeningen waarbij het immuunsysteem betrokken is voor Nederland in kaart gebracht. Het blijkt, exclusief infectieziekten, om drie miljoen patiënten te gaan.<ref name="auto" /> |
|||
==Immuunsysteem in de plant== |
==Immuunsysteem in de plant== |
||
Versie van 10 feb 2023 04:53

Het immuunsysteem is het geheel aan biologische processen dat een levend wezen beschermt tegen ziekte en infectie. Het immuunsysteem herkent vreemde binnendringende ziekteverwekkers, zoals bacteriën, virussen en parasieten, en activeert verschillende mechanismen om deze indringers te doden en veilig te verwijderen. Het immuunsysteem maakt hiervoor gebruik van cellen en gespecialiseerde eiwitten.
Bij gewervelde dieren, waaronder de mens, bestaat het immuunsysteem uit twee – nauw met elkaar samenwerkende – delen. Het aangeboren immuunsysteem, dat altijd en overal aanwezig is, vormt de eerste lijn van verdediging tegen een breed scala aan lichaamsvreemde invloeden. Het verworven immuunsysteem, dat later op gang gebracht wordt, is in staat zeer specifiek de infecterende ziekteverwekker te bestrijden, door middel van onder meer antilichamen en cytotoxische T-cellen.
Bijna alle levende wezens bezitten een vorm van afweer. Bacteriën hebben een rudimentair systeem van enzymen die beschermen tegen virusinfecties. Vroeg in de evolutie ontstonden er bij de eerste dieren mechanismen als fagocytose. Gewervelde dieren beschikken voorts over nog verfijndere afweermechanismen, zoals het vermogen om ziekteverwekkers heel precies te herkennen en herhaling van dezelfde infectie te voorkomen. Dit principe van verworven immuniteit is de basis van vaccinatie.
Stoornissen van de afweer kunnen leiden tot ernstige ziektebeelden. Wanneer het immuunsysteem onvoldoende functioneert, zoals bij immuundeficiënties, kunnen zich terugkerende en levensbedreigende infecties ontwikkelen. Dit is bijvoorbeeld het geval bij hiv/aids, erfelijke afwijkingen als SCID, en bij het gebruik van immuunsuppressiva. Een overactieve afweer kan ertoe leiden dat het immuunsysteem de lichaamseigen weefsels aanvalt. Voorbeelden van dergelijke auto-immuunziekten zijn reumatoïde artritis, diabetes type 1 en multipele sclerose.
Overzicht
De mens leeft in een wereld vol micro-organismen: bacteriën, schimmels, parasieten en virussen. Hoewel de meeste van deze organismen geen schade toebrengen en ongemerkt samenleven met hun gastheer, zijn er vele soorten die het lichaam binnendringen en ziekte kunnen veroorzaken. Het immuunsysteem heeft de taak het lichaam te verdedigen tegen de mogelijke bedreigingen van deze ziekteverwekkers (pathogenen).[1]
Het lichaam van dieren beschikt over fysieke barrières, zoals epitheelweefsels en slijmvliezen, die bacteriën en virussen normaal gesproken buitenhouden. Als een ziekteverwekker deze barrières toch doorbreekt, komt het in aanraking met het aangeboren immuunsysteem, dat een onmiddellijke, maar aspecifieke respons in gang zet. De ziekteverwekker wordt bijvoorbeeld door witte bloedcellen opgenomen en verteerd (fagocytose), of middels een ontstekingsreactie in zijn groei geremd. Terwijl het aangeboren immuunsysteem de infectie onder controle probeert de houden, brengt deze (bij gewervelden) een tweede lijn van afweer op gang: het verworven immuunsysteem.[2]
De cellen van het verworven immuunsysteem bezitten speciale receptoren op hun membraan, waarmee ze op een uiterst specifieke manier ziekteverwekkers herkennen en daarop reageren. Na herkenning zullen de cellen zich in hoog tempo delen en differentiëren, zodat de ziekteverwekker overal in het lichaam doeltreffend wordt bestreden, bijvoorbeeld via antilichamen of cytotoxische mechanismen.[2] Sommige cellen blijven na afloop nog lange tijd aanwezig in het bloed, teneinde herhaling van dezelfde infectie te voorkomen – een immunologisch geheugen.
| Aangeboren immuunsysteem | Verworven immuunsysteem |
|---|---|
| Respons is aspecifiek, werkt breed | Respons tegen een specifiek antigeen |
| Voortdurend en overal aanwezig | Komt na enkele dagen op gang |
| Cellulaire en humorale componenten | Cellulaire en humorale componenten |
| Geen geheugen | Geeft immunologisch geheugen |
| Komt voor bij vrijwel alle vormen van leven | Komt voor bij alle hogere gewervelde dieren |
Veel ziekteverwekkers brengen tijdens hun infectie schade toe aan een individu, bijvoorbeeld door toxines uit te scheiden of celprocessen te beïnvloeden. Ook het immuunsysteem zelf, dat de infectie probeert te bestrijden, kan schade toebrengen aan het lichaam.[3][4] Het is daarom van groot belang dat de afweer voortdurend onder controle wordt gehouden. Hiervoor beschikt het lichaam over diverse regulerende mechanismen. Hoewel het immuunsysteem primair gericht is op de bestrijding van infecterende agentia, speelt het ook een grote rol bij de afweer tegen kankercellen.[5]
Fysieke barrières
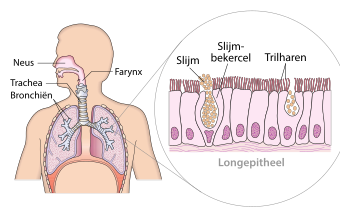
Het lichaam van gewervelde dieren wordt in de eerste plaats beschermd tegen ziekteverwekkers door fysieke barrières, zoals de huid, het epitheelweefsel rondom organen (zoals die van de long- of darmwand) en de slijmvliezen. De dicht op elkaar liggende epitheelcellen zijn moeilijk te passeren voor micro-organismen. Bovendien maken de biochemische omstandigheden van de slijmvliezen – zoals de lage pH van de maag, vetzuren op de huid – het lastig voor micro-organismen om deze plaatsen te overleven.[6]
In de slijmvliezen en lichaamsvloeistoffen komen vele antimicrobiële stoffen voor die in belangrijke mate bijdragen aan de afweer tegen infecties. Sommige van deze stoffen kunnen micro-organismen direct doden, andere zorgen ervoor dat hun groei sterk vertraagd wordt, of ondersteunen de immuunrespons ertegen. Epitheelcellen van de huid en luchtwegen produceren bijvoorbeeld kationische peptiden (defensinen) die zich aan de membranen van bacteriën en virussen hechten en deze ontwrichten.[7] Lysozymen in traanvocht splitsen de celwandcomponenten van bacteriën, en lactoferrinen in speeksel remmen groei van diverse pathogenen door ijzer weg te vangen.[6]
Op de huid en binnen de darmen komen van nature grote aantallen onschadelijke (en vaak nuttige) micro-organismen voor, de zogenaamde normale flora. Deze micro-organismen concurreren met pathogenen om ruimte en voedingsstoffen; sommige darmbacteriën produceren ook antimicrobiële metabolieten die de groei van pathogenen inhiberen.[8][9] Een achteruitgang van de darmflora, bijvoorbeeld bij gebruik van antibiotica, kan er soms voor zorgen dat pathogene bacteriën (zoals Clostridium) de darm vrijelijk koloniseren.[10]
Aangeboren immuunsysteem
Wanneer een ziekteverwekker ergens het lichaam binnendringt, komt het als eerst in aanraking met het aangeboren immuunsysteem, dat in principe overal en altijd klaarligt om direct in actie te komen. Het aangeboren immuunsysteem wordt gevormd door een aantal verschillende celtypen en honderden verschillende eiwitmoleculen die aanwezig zijn in het bloedplasma en de intercellulaire weefselvloeistof. Aangeboren immuuncellen en eiwitten kunnen een infecterend agens vrijwel direct (binnen enkele minuten tot uren) aanpakken en opruimen.
Herkenning
De cellen van het aangeboren immuunsysteem zijn in staat binnengedrongen virussen, bacteriën en andere pathogenen te herkennen op hun algemene kenmerken. Deze herkenning vindt plaats door middel van een diverse groep receptoren, de pattern-recognition-receptors.[11] Zij binden zich aan moleculen die typisch zijn voor micro-organismen, zoals virale nucleïnezuren of bacteriële koolhydraten. Dergelijke molecuulpatronen worden in de immunologie aangeduid als pathogen-associated molecular patterns (PAMPs).[a] Het zijn evolutionair geconserveerde structuren die nodig zijn voor het micro-organisme zelf. Omdat deze structuren nooit voorkomen op lichaamscellen, kunnen aangeboren immuuncellen een globaal onderscheid maken tussen lichaamseigen cellen en ziekteverwekkers.

Een van de belangrijkste groepen pattern-recognition-receptors zijn de Toll-like receptors, die voorkomen bij zowel dieren als planten. Toll-like receptors zijn grote, membraan-gebonden eiwitten die binding aangaan met (onderdelen van) diverse pathogenen, zoals lipopolysachariden, flagelline en bepaalde motieven in microbieel DNA.[12] Wanneer het bindingsdomein van een Toll-like receptor in contact komt met een lichaamsvreemd deeltje, brengt het binnen de cel een signaaltransductieketen op gang die uiteindelijk leidt tot de secretie van signaalstoffen (cytokinen). Ze alarmeren daarmee het immuunsysteem dat er een infectie gaande is.
Een andere grote familie van herkenningsreceptoren zijn de Nod-like receptors. Qua structuur lijken ze op Toll-like receptors, maar ze komen uitsluitend voor het cytoplasma, waar ze afbraakproducten van bacteriële peptidoglycanen detecteren.[13] Personen die een mutatie hebben in het gen voor Nod-like receptor 2 hebben een verhoogd risico op het ontwikkelen van de ziekte van Crohn, een chronische ontstekingsziekte van de dunne darm, die vermoedelijk veroorzaakt wordt door een bacteriële infectie.[14]
De meeste virussen worden gesignaleerd door RIG-I-like receptors.[15] Dit zijn een groep herkenningseiwitten die eveneens in het cytoplasma gelokaliseerd zijn en zich binden aan dubbelstrengs RNA, een vorm van RNA die algemeen optreedt tijdens de replicatie van virussen, maar zelden bij het lichaamseigen RNA. RIG-I-like receptors geven aanleiding tot een interferonrespons, die de replicatiecyclus van virussen op een effectieve, maar aspecifieke wijze verhindert.[15]
Aangeboren immuuncellen

Tot de celtypen van het aangeboren immuunsysteem behoren macrofagen, neutrofielen, dendritische cellen en verschillende soorten granulocyten. Dit zijn allemaal witte bloedcellen die ziekteverwekkers snel herkennen en elimineren, meestal door ze in zich op te nemen en intracellulair te verteren (fagocytose).[16]
Macrofagen zijn langlevende witte bloedcellen die zich in de meeste weefsels van gewervelde dieren bevinden; het zijn vaak de eerste immuuncellen die in aanraking komen met binnendringende micro-organismen. Neutrofielen zijn kortlevende bloedcellen die in grote aantallen voorkomen in het bloed maar niet in gezonde weefsels aanwezig zijn; ze worden snel gerekruteerd naar de plaats van infectie door signaalstofjes (chemokinen) die uitgescheiden worden door geactiveerde macrofagen.[17]
Macrofagen, dendritische cellen en neutrofielen zijn gespecialiseerd in het fagocyteren van ziekteverwekkers, en worden daarom ook wel professionele fagocyten genoemd. Deze cellen hebben receptoren op hun membraan die vreemde indringers herkennen, vastbinden, en vervolgens opnemen in een inwendig blaasje.[16] Binnen de cel wordt de opgenomen pathogeen blootgesteld aan een overweldigend arsenaal van hydrolases, lysozymen en giftige peroxiden. Fagocytose is een van oudste vormen van afweer: het proces is wijdverspreid onder het dierenrijk, en komt voor bij diverse eencelligen als voedselvergaringsmethode.[18][19]
Granulocyten zijn witte bloedcellen die granulen in hun cytoplasma hebben. Tot deze groep behoren mestcellen, basofielen en eosinofielen. Mestcellen komen voor in slijmvliezen en reguleren ontstekingsreacties, onder meer door histamine af te geven.[20] Als een ziekteverwekker te groot is om te worden gefagocyteerd – bijvoorbeeld een parasitaire worm – zullen eosinofielen zich rond de parasiet verzamelen. Ze scheiden dan defensines en andere schadelijke stoffen uit en geven giftige zuurstofradicalen vrij. Een dergelijke barrage is vaak genoeg om de parasiet te vernietigen.[17][21]

Ontsteking
Wanneer de aangeboren immuuncellen een binnengedrongen ziekteverwekker op het spoor komen, slaan ze alarm en geven ze aanleiding tot een ontstekingsreactie. Tijdens een ontsteking worden extra cellen en eiwitten van het afweersysteem aangemaakt en gedirigeerd naar de infectiehaard om deze te bestrijden.[22] De ontsteking wordt gekenmerkt door vijf klassieke klinische symptomen: pijn, roodheid, warmte, zwelling en functieverlies. De bloedvaten rond de infectiehaard verwijden zich en worden doorlaatbaar voor eiwitten, wat leidt tot de lokale zwelling. De endotheelcellen langs de lokale bloedvaten brengen celadhesie-eiwitten tot expressie, die ervoor zorgen dat neutrofielen (en later ook lymfocyten) aan de wand aanhechten en erdoorheen ontsnappen naar het geïnfecteerde weefsel.[23][17]
Een ontsteking wordt geregeld door een breed scala aan signaalmoleculen (cytokinen), die in snel tempo aangemaakt worden door immuuncellen wanneer zij met hun pattern-recognition-receptors lichaamsvreemd materiaal detecteren. De belangrijkste ontstekingsbevorderende cytokinen zijn tumornecrosefactor α (TNF-α), interferon-γ (IFN-γ), enkele chemokinen (stofjes die neutrofielen rekruteren) en verschillende interleukinen (met name IL1, IL6, IL12 en IL17).[22] Ook splitsingsproducten van het complementsysteem bevorderen de ontsteking. Wanneer een ontstekingsprikkel lange tijd aanhoudt, zoals bij een persisterende infectie of een auto-immuunziekte, kan de ontsteking een chronisch karakter krijgen. Aandoeningen als COPD, inflammatoire darmziekten en artrose zijn hiervan een vervelend gevolg.[24]
Complementsysteem
In het bloed en de weefselvloeistoffen bevinden zich talloze eiwitten met antimicrobiële activiteit. De componenten van het complementsysteem zijn hiervan een belangrijk voorbeeld. Het complementsysteem bestaat uit ongeveer dertig op elkaar inwerkende oplosbare eiwitten, die inactief zijn totdat een infectie of een andere trigger ze activeert.[25] Ze werden oorspronkelijk ontdekt door hun vermogen om de werking van antilichamen 'aan te vullen' (te complementeren). Het complementsysteem kent een ingewikkeld, drieledig initiatiemechanisme[c] dat een enzymcascade op gang brengt. Uiteindelijk wordt in deze cascade het complement-eiwit C3 gesplitst in twee actieve fragmenten (C3a en C3b) die uiteenlopende effectorfuncties hebben: aantrekking van ontstekingscellen, het vergemakkelijken van fagocytose en stimulatie van de verworven afweer.[17] Bovendien kunnen sommige complement-eiwitten poriën vormen in het membraan van pathogenen, waardoor deze met water vollopen en uiteenvallen (lyse). Personen met een deficiëntie voor het C3-eiwit lijden vaak aan terugkerende bacteriële infecties.[26]
Verworven immuunsysteem
Een enorme stap in de evolutie van afweermechanismen trad op toen gewervelde dieren ontstonden en een verworven immuunsysteem ontwikkelden. Het verworven immuunsysteem werkt uiterst specifiek: hieraan ontleent het dan ook zijn grote kracht. De verworven afweer hangt af van twee groepen witte bloedcellen, de T-lymfocyten en de B-lymfocyten.[d] B-lymfocyten produceren antilichamen; dit zijn grote eiwitmoleculen die aan de bloedbaan worden afgegeven en zich specifiek binden aan het lichaamsvreemde stofje waartegen ze zijn aangemaakt – het zogenaamde antigeen. Zo kan een antilichaam zich binden aan een extracellulair virus of microbieel toxine, waarna deze niet langer gastheercellen kunnen ingaan. T-lymfocyten daarentegen, detecteren ziekteverwekkers die zich binnen lichaamscellen verbergen. Ze kunnen de geïnfecteerde cel doden middels een cytotoxisch (celdodend) mechanisme, of de activiteit van fagocyten of B-cellen stimuleren om zo de infectie te helpen bestrijden. Hoewel het verworven immuunsysteem traag op gang komt, biedt het een langdurige, soms levenslange bescherming tegen een ziekteverwekker.
![Het verworven immuunsysteem wordt geactiveerd door fagocyten, veelal dendritische cellen.[27] Nadat een dendritische cel een pathogeen heeft gefagocyteerd, migreert deze naar een lymfeklier om daar fragmentjes van de pathogeen (de antigenen) aan T-lymfocyten te presenteren. De geactiveerde T-cellen delen zich snel. Een deel gaat naar de infectiehaard om deze te bestrijden. Andere T-cellen stimuleren B-cellen om antilichamen te produceren.](http://upload.wikimedia.org/wikipedia/commons/thumb/a/a9/Adaptief_immuunsysteem.svg/550px-Adaptief_immuunsysteem.svg.png)
Antigenen
De cellen van het verworven immuunsysteem herkennen specifieke details van pathogene micro-organismen, de zogenaamde antigenen. Antigenen werden oorspronkelijk ontdekt als stofjes die de aanmaak van antilichamen opwekken, en kregen daarbij de naam antibody generator (anti-gen).[28] Antigenen zijn doorgaans eiwitten op het oppervlak van een ziekteverwekker. Het spike-eiwit van coronavirussen is een notoir voorbeeld. Het kunnen ook polysachariden, lipiden of nucleïnezuren zijn. Sommige antigenen, zoals toxinen, worden door de ziekteverwekker uitgescheiden.

T- en B-lymfocyten hebben op hun membraan een unieke soort receptor: de T-celreceptor of B-celreceptor. Deze receptoren binden zich aan de antigenen die het lichaam zijn binnengedrongen. De binding van zo'n receptor op een antigeen is uiterst specifiek: zo specifiek, dat er zelfs onderscheid gemaakt kan worden tussen twee eiwitten die verschillen in slechts een enkel aminozuur, of twee vrijwel identieke optische isomeren. Op deze manier kan het verworven immuunsysteem elke ziekteverwekker herkennen en er specifiek op reageren, ook op nieuwe mutanten.
Het verworven immuunsysteem produceert miljoenen verschillende T- en B-celreceptoren. Iedere lymfocyt heeft één uniek type receptor op zijn membraan.[e] Tijdens de ontwikkeling van lymfocyten vinden er speciale genetische recombinaties plaats die zorgen voor een gigantische diversiteit aan antigeenreceptoren. Deze recombinaties, de zogenaamde V(D)J-recombinaties, maken mogelijk dat een mens ruim 1 miljoen B-celreceptoren kan maken, en meer dan 10 miljoen T-celreceptoren.
Tolerantie
Omdat het genetische herschikkingsproces willekeurig is, ontstaan er zowel receptoren die kunnen binden aan lichaamseigen moleculen als receptoren die kunnen binden aan lichaamsvreemde moleculen. Gewervelde dieren hebben dus speciale mechanismen moeten ontwikkelen om ervoor te zorgen dat B- en T-cellen niet reageren tegen het eigen lichaam. Lymfocyten komen tijdens hun ontwikkeling in contact met lichaamseigen moleculen. Alle lymfocyten die een receptor hebben die aan een lichaamseigen antigeen bindt, zullen doodgaan door apoptose (klonale deletie). Zelfreactieve receptoren worden op deze manier weggeselecteerd.[29] De enkele zelfreactieve lymfocyten die aan dit mechanisme ontsnappen, worden vaak elders in het lichaam nog onderdrukt door regulatoire T-cellen.[30] Wanneer tolerantiemechanismen tekortschieten, zullen er lymfocyten worden gemaakt die tegen de eigen cellen zijn gericht. Een auto-immuunziekte kan hiervan het gevolg zijn. In diabetes type 1 worden er bijvoorbeeld antilichamen gemaakt tegen bètacellen in de pancreas, wat leidt tot een ernstig verstoorde insulineproductie.[29]
Cellulaire afweer
Na hun ontwikkeling te hebben voltooid in de thymus, komen T-cellen in de bloedsomloop terecht. Ze circuleren door het bloed en de lymfevaten. In dit stadium worden ze naïeve T-cellen genoemd, omdat ze nog geen lichaamsvreemd antigeen zijn tegengekomen. Om deel te nemen aan de verworven immuunrespons, moet een naïeve T-cel eerst met zijn receptor een antigeen binden. De T-cel raakt dan geactiveerd, zal zich veelvuldig delen en differentiëren tot effectorcellen die kunnen bijdragen aan de bestrijding van de ziekteverwekker.
T-cellen worden geactiveerd door cellen van het aangeboren immuunsysteem, de zogenaamde antigeen-presenterende cellen. Dendritische cellen zijn veruit het belangrijkste antigeenpresenterende celtype in het lichaam. Nadat een dendritische cel een pathogeen op de plaats van infectie heeft gefagocyteerd, zal deze cel fragmentjes van de pathogeen (kleine peptiden) op zijn membraanoppervlak dragen. De cel is hiervoor uitgerust met speciale eiwitcomplexen die lichaamsvreemde peptiden kunnen binden, de MHC-eiwitten (MHC-II).[f] De dendritische cel circuleert rond de lymfeknopen en komt daarbij in contact met duizenden naïeve T-cellen. Wanneer de dendritische cel een T-cel tegenkomt die met hoge affiniteit aan het lichaamsvreemde antigeen bindt, krijgt de T-cel een signaal om zich vele malen te delen (klonale expansie). Zo ontstaan er duizenden identieke klonen van de cel met de juiste receptor. Sommige van de klonen differentiëren zich tot cytotoxische T-cellen, andere tot verschillende soorten helper-T-cellen.

Effector T-cellen
Cytotoxische T-cellen zijn gespecialiseerd in het herkennen van geïnfecteerde lichaamscellen, bijvoorbeeld cellen van de luchtwegen die een virus of andere intracellulaire pathogeen in zich dragen. Cytotoxische T-cellen kunnen de geïnfecteerde cel doden voordat de pathogeen zich verspreid naar naburige cellen. De herkenning van een geïnfecteerde lichaamscel gebeurt, net als bij antigeenpresentatie, door middel van een MHC-eiwit (MHC-I). Vrijwel alle cellen in het lichaam brengen MHC-I tot expressie. Wanneer er een infectie plaatsvindt, zal de cel peptiden van de pathogeen op zijn membraan presenteren via MHC-I. Langskomende cytotoxische T-cellen herkennen het lichaamsvreemde antigeen, en scheiden dan toxische eiwitten uit (perforines en granzymen) die de lichaamscel vernietigen.[31] Cytotoxische T-cellen zijn uitgerust met een co-receptor genaamd CD8, die specifiek de interactie met MHC-I stabiliseert.[32]

Helper-T-cellen zijn van groot belang voor het ondersteunen en sturen van de immuunrespons. Ze stimuleren zowel aangeboren als verworven immmuuncellen. Ze geven bijvoorbeeld macrofagen de kracht om efficiënter te fagocyteren; ze stimuleren B-cellen om over te gaan tot antilichaamproductie; ze bevorderen de antigeenpresentatie tussen dendritische cellen en naïeve T-cellen. In alle gevallen vindt de ondersteuning plaats door de uitscheiding van cytokinen. Alle T-helpercellen bezitten CD4, een co-receptor die nodig is voor stabiele interactie met MHC-II tijdens antigeenpresentatie.[32]
Differentiatie tot helpercellen is uiterst complex. Globaal zijn er vijf richtingen te onderscheiden waarnaar helpercellen zich specialiseren: Th1-, Th2-, Tfh-, Th17 en regulatoire T-cellen.[g] Elk van deze helpercellen ondersteunt een uniek deel van het immuunsysteem, en elk heeft daarvoor een eigen cytokine-expressiepatroon. Regulatoire T-cellen cellen remmen de immuunrespons af door ontstekingsremmende cytokinen af te geven. Hiermee voorkomen ze een excessieve immuunrespons die vaak schadelijk is voor het eigen lichaam.[33] De differentiatieroutes van helper-T-cellen zijn niet in steen gebeiteld; effector T-cellen zijn plastisch en kunnen veranderen van het ene naar het andere celtype als dat nodig is.[34]
Humorale afweer
De verworven afweer die door B-lymfocyten wordt verzorgd, noemt men de humorale afweer. Een B-celreceptor is een groot, Y-vormig eiwit dat opgebouwd is uit vier polypeptiden: twee identieke zware ketens en twee identieke lichte ketens. Een B-celreceptor heeft aan de N-terminus een hypervariabele regio waarin zich de antigeen-bindingsplaats bevindt. Nadat een B-celreceptor een antigeen bindt, raakt de B-cel geactiveerd. De B-cel zal zich vervolgens veelvuldig delen en differentiëren tot plasmacellen. Dit zijn de antilichaamproducenten van het lichaam. Voor de productie en sturing van antilichamen zijn helper-T-cellen essentieel: de B-cel zal zijn antigeen bijvoorbeeld niet gepresenteerd krijgen via een dendritische cel, maar via een gespecialiseerde helper-T-cel.
Antilichamen

Een antilichaam, ook wel immunoglobuline (Ig) genoemd, is in wezen een uitgescheiden B-celreceptor. Het heeft, net als de receptor, een karakteristieke Y-vorm en bindt zich met dezelfde specificiteit aan antigenen. De antilichamen komen in de bloedsomloop terecht en verspreiden zich gemakkelijk over alle weefselvloeistoffen van het lichaam. Omdat de feitelijke beschermende werking uitgaat van de in het serum aanwezige antilichamen, wordt dit deel van het verworven immuunsysteem de 'humorale afweer' genoemd (humoris = lichaamsvloeistof).[28]
Antilichamen zorgen er op verschillende manieren voor dat een pathogeen wordt bestreden. Virussen en microbiële toxines zijn na binding van een antilichaam niet meer in staat om aan een gastheercel te hechten. Uitschakeling van virussen met behulp van antilichamen wordt neutralisatie genoemd. Het induceren van neutraliserende antilichamen is een belangrijk focuspunt bij de ontwikkeling van nieuwe vaccins. Naast hun neutralisatiefunctie zorgen antilichamen er ook voor dat pathogenen sneller worden opgeruimd door het aangeboren immuunsysteem. Een antilichaam-beladen bacterie wordt bijvoorbeeld efficiënter gefagocyteerd (opsonisatie) en makkelijker vernietigd door het complementsysteem.[35]
Immuniteit en geheugen
Als het lichaam een infectie heeft doorgemaakt en hiervan hersteld is, zijn er vele miljoenen antigeenspecifieke T-cellen en B-cellen aanwezig in de circulatie. Hoewel de meeste van deze lymfocyten na verloop van tijd verdwijnen, is er een subgroep die nog vele jaren aanwezig blijft: de geheugencellen. Zij zetten een zeer snelle en efficiënte immuunrespons in gang wanneer dezelfde ziekteverwekker opnieuw het lichaam binnendringt. De respons is vaak zo efficiënt, dat schade door de ziekteverwekker ongemerkt binnen de perken wordt gehouden. Dit principe, het zogeheten immunologisch geheugen, is de basis van vaccinatie. Geheugencellen zorgen ervoor dat een individu beschermd of immuun is voor een ziekte die in het verleden is doorgemaakt. Voor sommige infectieziekten, zoals mazelen of waterpokken, is de bescherming levenslang. Voor snelmuterende pathogenen, zoals influenzavirussen, is de bescherming meestal vergankelijk.

De geheugenrespons is relatief eenvoudig te bestuderen in diermodellen. Wanneer een proefdier geïmmuniseerd wordt met een antigeen, kan na enkele dagen een primaire immuunrespons worden gedetecteerd – gemeten aan de hoeveelheid en de soort antilichamen het bloed. Tijdens de primaire respons wordt (bij zoogdieren) eerst IgM gemaakt, en na ongeveer een week verschijnen er antilichamen van een andere klasse, IgG.[h] Als het dier na enkele weken, maanden of zelfs jaren opnieuw wordt geïmmuniseerd met hetzelfde antigeen, zal een secundaire immuunrespons optreden die verschilt van de primaire respons: de opstartcurve is steiler, omdat er veel meer reeds aanwezige B- of T-cellen (geheugencellen) aanwezig zijn. De secundaire respons kenmerkt zich door de snelle productie van vooral de IgG-klasse.
Fysiologische regulatie
Het immuunsysteem kent een nauwe verwevenheid met andere orgaansystemen in het lichaam. Voornamelijk het zenuwstelsel en endocrien systeem (hormoonstelsel) kunnen de immuunrespons reguleren. Fysiologische signalen als hormonen en neurotransmitters bepalen hoe snel en efficiënt het immuunsysteem op gang komt om infecties te bestrijden. Leefstijlvariabelen als slaap, beweging en voeding zijn een aantal belangrijke externe determinanten van de immuunfunctie.
Hormonen
Vrijwel alle immuuncellen bezitten hormoonreceptoren op hun membraan, en zijn gevoelig voor diverse endocriene signalen. Van geslachtshormonen is duidelijk dat ze een grote invloed uitoefenen op de immuunfunctie.[36][37] Oestrogenen, de vrouwelijke geslachtshormonen, hebben bijvoorbeeld een uitgesproken stimulerend effect op zowel aangeboren als verworven immuuncellen. Dit wordt geïllustreerd door het feit dat vrouwen over het algemeen een sterkere immuunrespons vertonen tegen infecties, en ook een grotere incidentie van auto-immuunziekten kennen.[38] Mannelijke geslachtshormonen, zoals testosteron, werken veelal juist immunosuppressief: ze hebben een remmende invloed op de afweer.[39] Het mechanisme hierachter is nog niet geheel opgehelderd. Ook andere hormonen, zoals groeihormonen, prolactine en vitamine D (een pro-hormoon) kunnen de immuunrespons sturen.
Slaap en voeding
De werking van het menselijk immuunsysteem wordt in belangrijke mate beïnvloed door leefstijlfactoren als slaap, lichaamsbeweging en voeding. Er is nog veel onduidelijk over de manier waarop dergelijke externe factoren de aangeboren en verworven immuuncellen precies moduleren. Wel is helder dat de juiste leefgewoontes, zoals voldoende slaap en gezonde voeding, van wezenlijk belang zijn voor een robuuste en goed functionerende afweer.[40][41]
Veel processen van het immuunsysteem volgen een circadiaan ritme, wat suggereert dat ze nauw verbonden zijn met de slaap-waakcyclus. Dit ritme komt tot stand doordat cytokinen en andere signaalstoffen in een met de tijd van dag variërende hoeveelheid worden afgegeven. Effectorcellen van de afweer, zoals NK-cellen of cytotoxische T-cellen, vertonen een piek in hun activiteit overdag: ze zijn dan hard bezig met de bestrijding van indringers die de gastheer gedurende de daguren meestal tegenkomt.[40] Minder gedifferentieerde immuuncellen, zoals naïeve T-cellen of geheugencellen, hebben hun piek juist 's nachts. Onderzoeken in muismodellen laten zien dat er tijdens de nachtelijke rust een sterkere interactie is tussen antigeenpresenterende cellen en (naïeve) T-cellen, en een hoger delingspotentieel van helper T-cellen.[40] Langdurige slaaponthouding is bij de mens in verband gebracht met een verstoorde cytokineproductie, sluipende ontstekingswaarden in het bloed, en immuundeficiënties die resulteren in een hoger infectierisico.[42][43][44]
Een gezonde voeding is noodzakelijk om alle cellen van het lichaam optimaal te laten functioneren, ook die van het immuunsysteem. Sommige nutriënten uit voeding spelen een directe rol in de afweer: het aminozuur arginine is bijvoorbeeld nodig voor de aanmaak van stikstofmonoxide in macrofagen, en vitamine A en zink hebben een regulerende rol op de celdeling, en zijn daarom van belang bij de proliferatie van lymfocyten.[41] Voedingsvezels kunnen invloed hebben op de immuunfunctie door in te spelen op het darm-microbioom.[i] De impact van voeding op immunologische aandoeningen (infectie, chronische ontstekingsziekten, allergieën) is – ondanks veel onderzoek – slechts beperkt in kaart gebracht.[46] Eenduidige voedingsadviezen om de weerstand te verbeteren zijn dan ook lastig te formuleren.
Verstoringen van het menselijk immuunsysteem
Immuundeficiënties
Het immuunsysteem werkt niet altijd perfect. Het kan bijvoorbeeld een aangeboren afwijking hebben, of in de loop van het leven minder goed gaan functioneren door tal van omstandigheden, variërend van medicijngebruik tot ondervoeding. Een tekortschietend immuunsysteem is gevaarlijk. Er bestaat immers een verhoogde gevoeligheid voor infecties, zelfs voor micro-organismen die gewoonlijk geen ziekte kunnen veroorzaken.[47] Men spreekt van opportunistische infecties.
Severe combined immunodeficiency (SCID) is een zeldzame aangeboren afwijking van het immuunsysteem. Kinderen die geboren worden met SCID hebben geen of weinig T- en B-lymfocyten in hun bloed, waardoor zij zich niet of nauwelijks kunnen verweren tegen micro-organismen. De oorzaak van SCID ligt in mutaties van receptoren op de lymfocyten.[48] Ook mensen die met een goed functionerend immuunsysteem worden geboren, kunnen later in hun leven te maken krijgen met een verminderde afweer. Misschien wel het sprekendste voorbeeld hiervan is infectie met het humaan immunodeficiëntievirus (hiv). Dit virus infecteert helper T-cellen, waardoor de verworven afweer dermate ontregeld raakt dat zich levensbedreigende infecties kunnen ontwikkelen.[49][50]
Auto-immuunziekten

Onder normale omstandigheden wordt een immuunrespons tegen het eigen lichaam grotendeels voorkomen (en actief onderdrukt), door tolerantiemechanismen als klonale deletie en de werking van regulerende immuuncellen.[51] Wanneer deze tolerantie faalt of doorbroken wordt, en er antilichamen of effector T-cellen worden aangemaakt die tegen de eigen lichaamsweefsels actief zijn, kan dit leiden tot een auto-immuunziekte.[51]
Auto-immuunziekten kunnen vrijwel ieder orgaan treffen en de klinische symptomen lopen dan ook ver uiteen. Sommige auto-immuunziekten zijn orgaanspecifiek, zoals de huidziekte psoriasis. Andere hebben een systemisch karakter, zoals systemische lupus erythematodes (SLE), waarbij vrijwel elk deel van het lichaam kan worden aangedaan. Bij SLE worden er antilichamen gevormd tegen het eigen dubbelstrengse DNA. Een ziekte als SLE kan zeer ernstig en zelfs fataal verlopen indien niet tijdig de diagnose wordt gesteld en een behandeling wordt gestart.[52]
In veel geïndustrieerde landen zoals Nederland en België vormen reumatoïde artritis, de ziekte van Hashimoto en diabetes type 1 de top drie van auto-immuunziekten.[53] Chronisch verlopende auto-immuunziekten zoals reumatoïde artritis kunnen leiden tot blijvende invaliditeit en vormen een zware ziektelast voor de patiënt en zijn omgeving.
Allergie en overgevoeligheid

Het lichaam staat voortdurend bloot aan onschuldige prikkels van buitenaf, zoals huisstofmijten, voedingsbestanddelen en pollen. Normaal gesproken komt het immuunsysteem niet in actie tegen deze prikkels omdat tolerantiemechanismen voorkomen dat een reactie optreedt. Sommige individuen vertonen echter wél een hevige respons, vaak met nare lichamelijke klachten tot gevolg.[54] Een overmatige reactie op een onschuldige prikkel ligt ten grondslag aan een allergie. De bekendste manifestaties van allergieën zijn eczeem, voedselallergie (bijvoorbeeld tegen gluten, noten of lactose), hooikoorts en astma.
Bij een allergische reactie spelen de cytokinen IL-4 en IL-5 een belangrijke rol. Deze cytokinen zetten onder andere B-lymfocyten aan tot de productie van IgE-antilichamen. IgE's die zich binden aan mestcellen, die na activatie krachtige ontstekingsmoleculen vrijgeven, zoals histaminen. Veel allergieremmende medicijnen gaan de overmatige werking van histamine tegen, de antihistaminica.[55]
Vanaf het eind van de 20ste eeuw is het aantal mensen met een allergische ziekte sterk toegenomen, mogelijk als gevolg van toegenomen hygiëne en veranderingen in de omgeving. Het Rijksinstituut voor Volksgezondheid en Milieu (RIVM) heeft alle aandoeningen waarbij het immuunsysteem betrokken is voor Nederland in kaart gebracht. Het blijkt, exclusief infectieziekten, om drie miljoen patiënten te gaan.[53]
Immuunsysteem in de plant
Bij zelfbestuivende planten zal een stuifmeelkorrel die op het stigma van een bloem landt een stuifmeelbuisje onderaan de steel naar de stempel voor bevruchting verzenden. Een stuifmeelkorrel van een genetisch verschillende plant zal niet ontkiemen of het stuifmeelbuisje zal, zodra gevormd, in de steel desintegreren. In kruisbestuivende soorten desintegreren de eigen stuifmeelkorrels, terwijl de niet-eigen korrels ontkiemen en bevruchten.
Toch moeten niet alle cellen van buiten worden vernietigd, aangezien sommige voor voeding moet worden geassimileerd. Daarom moet het immuunsysteem de capaciteit hebben om eigen en niet-eigen te ontdekken. Het afweerstelsel moet de capaciteit hebben om toekomstige gevaren te behandelen.
Zie ook
Noten
Referenties
Literatuur
|
